Clear Sky Science · ru
Овариально-ооцитовоспецифическое удаление субъединиц eIF2 вызывает апоптоз ооцитов мышей в ранних растущих фолликулах через митохондриальные дисфункции и повреждение ДНК
Почему важна жизнь яйцеклеток
Женщины рождаются со всеми яйцеклетками, которые у них когда-либо будут, хранящимися в крошечных структурах в яичнике, называемых фолликулами. Если эти фолликулы теряются слишком быстро, у женщин может развиться преждевременная недостаточность яичников (ПНЯ), состояние, которое ведёт к раннему бесплодию и часто сопровождается симптомами, похожими на менопаузу, в молодом возрасте. Это исследование на мышах задаёт простой, но ключевой вопрос: что происходит в яйцеклетках, когда нарушается важный этап запуска синтеза белка, и как это может привести к ранней потере фертильности?
Переключатель запуска белка в клетке
Чтобы оставаться здоровыми, яйцеклетки должны постоянно синтезировать правильные белки в нужное время. Центральную роль в этом процессе играет трёхкомпонентный молекулярный комплекс eIF2, который помогает запускать синтез белка с информационной РНК. Исследователи выборочно выключили две субъединицы eIF2, называемые eIF2α и eIF2β, только в ооцитах мышей на ранних стадиях роста фолликулов. Когда отсутствовала любая из этих субъединиц, самки мышей становились полностью бесплодными. Их яичники уменьшались в размере, а нормальный переход от ранних фолликулов к зрелым, готовым к овуляции, во многом останавливался: на каждой более поздней стадии обнаруживалось значительно меньше фолликулов. Со временем фактически все фолликулы истощались, воспроизводя тяжёлую форму ранней ПНЯ-подобной патологии.
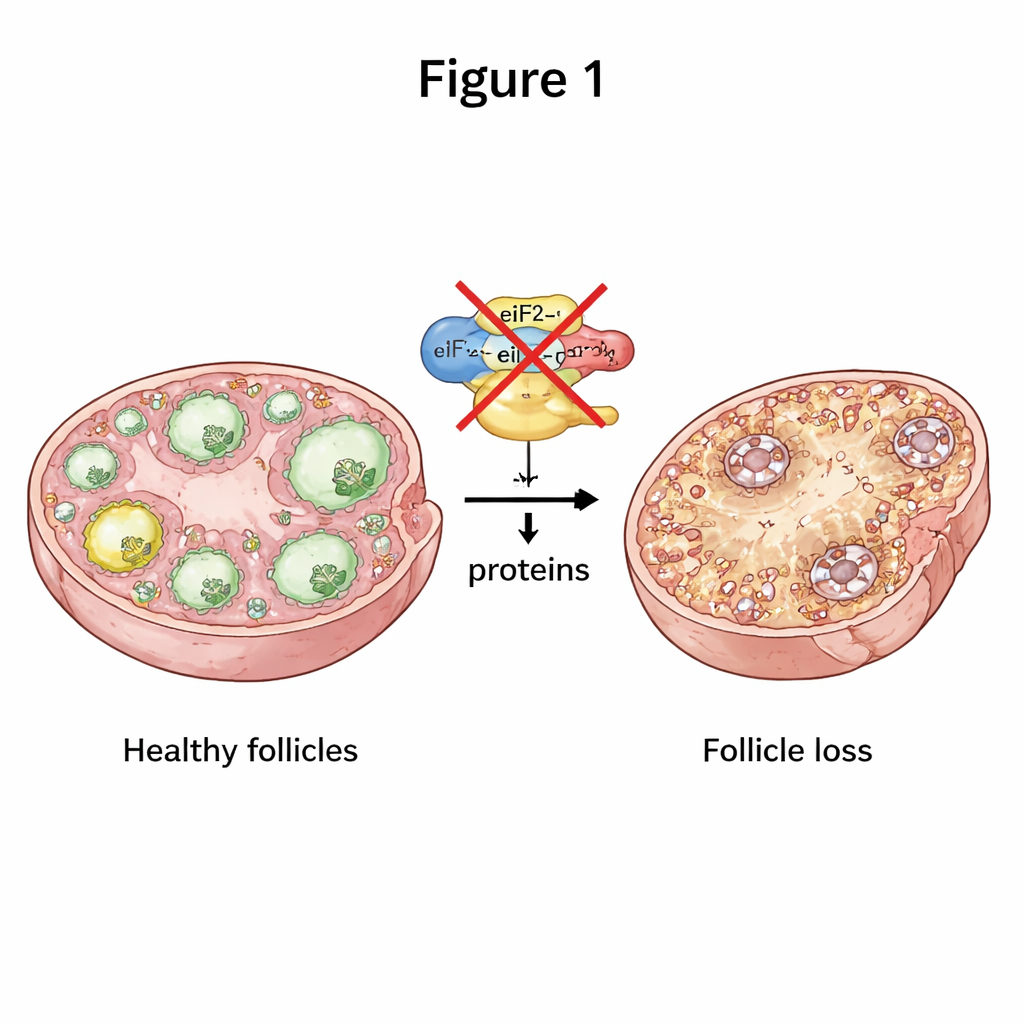
Когда связь в яичнике нарушается
Фолликулы — это не просто отдельно плавающие яйцеклетки; это тесные партнёрства между яйцеклеткой и окружающими «помогающими» клетками — гранулёзными клетками. Команда обнаружила, что при отсутствии eIF2β ооциты вырабатывали значительно меньше нескольких ключевых сигнальных белков, которые обычно поддерживают рост гранулёзных клеток и доставку питательных веществ. Физические мостики между ооцитами и гранулёзными клетками были дезорганизованы и укорочены, а микроворсинки на поверхности ооцитов выглядели стёртыми и повреждёнными в электронном микроскопе. Гранулёзные клетки в таких фолликулах делились реже и чаще умирали. Этот сбой двусторонней коммуникации означал, что фолликулы не могли правильно расти, что приводило к их потере и истощению яичника.
Отказ «батарей» яйцеклетки
Митохондрии, часто называемые энергетическими станциями клетки, особенно важны в яйцеклетках, потому что они обеспечивают энергию, необходимую для роста и дальнейшего развития эмбриона. В ооцитах, лишённых eIF2β, общий уровень нового синтеза белка снизился, и многие белки, связанные с митохондриями, оказались уменьшены. Митохондрии становились аномально вытянутыми, слипались у поверхности клетки и демонстрировали ослабленный мембранный потенциал, более низкий уровень АТФ и меньше копий митохондриальной ДНК. Одновременно в клетках накапливались высокие уровни реактивных форм кислорода (ROS) — агрессивных кислородсодержащих молекул, которые могут повреждать клеточные компоненты. В совокупности эти изменения указывали на глубокий коллапс митохондриальной динамики и функции.
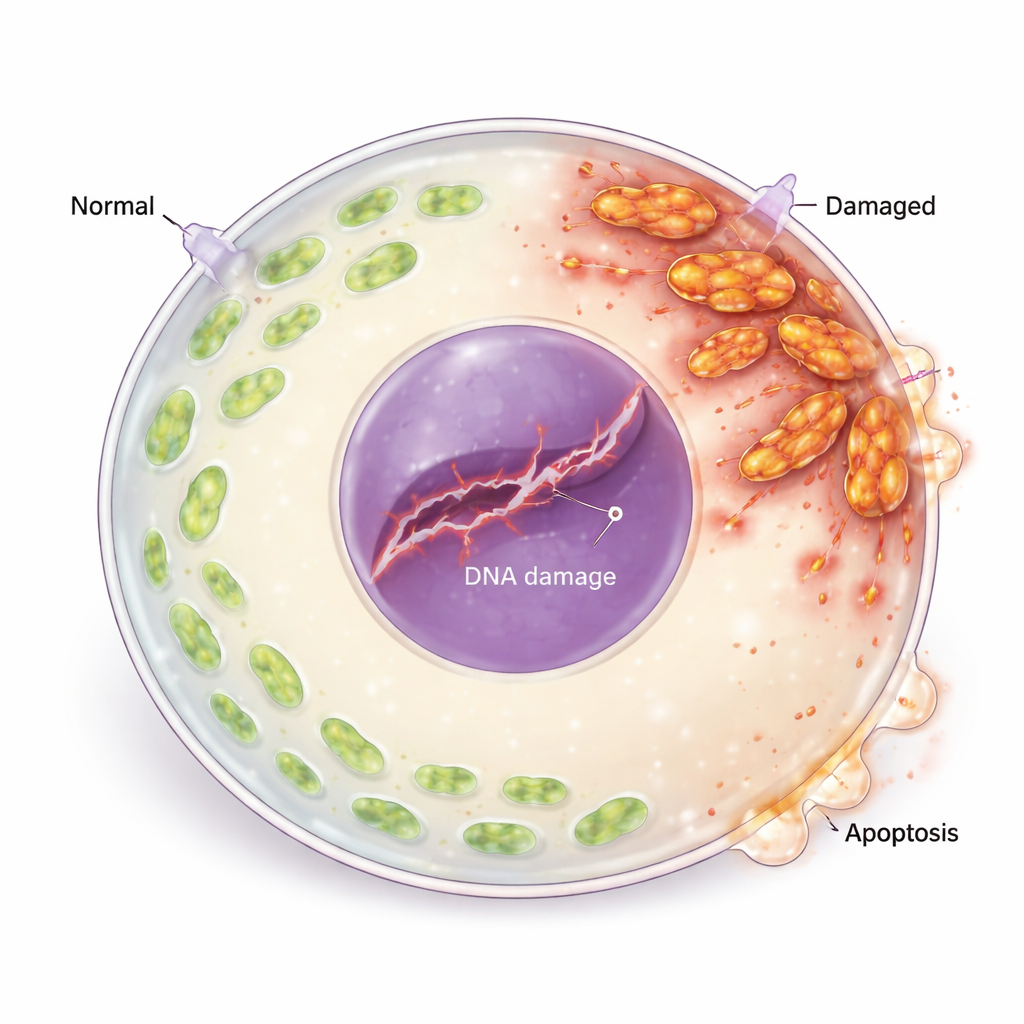
От окислительного стресса до повреждения ДНК и гибели клетки
Избыточные ROS вредили не только митохондриям; они также повреждали генетический материал яйцеклетки. Исследователи наблюдали увеличение маркёров разрывов цепей ДНК и активацию системы ответа клетки на повреждение ДНК, включая белки, которые обнаруживают и сигнализируют о генетическом повреждении. Один ключевой белок репарации оказался снижен, что указывает на неэффективный ремонт повреждений. Впоследствии баланс регуляторов жизни и смерти сместился: возросли проапоптотические белки, тогда как защитные антиапоптотические белки упали, и ооциты демонстрировали явные признаки программируемой клеточной гибели (апоптоза). Когда командa обработала ооциты антиоксидантом (N-ацетилцистеином), уровни ROS снизились, маркёры повреждения ДНК и апоптоза уменьшились, а созревание яйцеклеток улучшилось, что прямо связало окислительный стресс с потерей ооцитов.
Что это значит для ранней недостаточности яичников
Проследив события от одного молекулярного комплекса (eIF2) до дефектного синтеза белка, распада митохондрий, окислительного стресса, повреждения ДНК и, в конечном итоге, гибели яйцеклеток, эта работа описывает детальную цепочку событий, которая может разрушить овариальный резерв. Исследование подкрепляет идею о том, что мутации в факторах запуска трансляции, уже обнаруженные у некоторых женщин с ПНЯ, могут напрямую повреждать ооциты через этот путь. Также это указывает на потенциальные подходы для помощи: антиоксиданты, модуляторы стресс-ответа или методы защиты ранних фолликулов (например, антимиуллеров гормон, который частично сохранил дремлющие фолликулы у этих мышей) могут в будущем поддержать фертильность у пациентов с уязвимыми яичниками.
Цитирование: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Ключевые слова: преждевременная недостаточность яичников, апоптоз ооцитов, митохондриальная дисфункция, синтез белка, реактивные формы кислорода