Clear Sky Science · ru
Транглутаминаза 2 усугубляет выживаемость при раке яичников, напрямую инактивируя GSK3β
Почему это исследование важно для женского здоровья
Рак яичников — один из самых смертельных видов рака у женщин, поскольку его обычно обнаруживают на поздних стадиях, и он часто возвращается даже после интенсивной химиотерапии. В этом исследовании показано, как малоизвестный белок — транглутаминаза 2 (TGase 2) — помогает клеткам рака яичников выживать при лечении и распространяться по организму. Выявление этого скрытого помощника опухоли указывает на новые способы повысить эффективность имеющихся препаратов и замедлить или остановить фатальное метастазирование.
Скрытый драйвер в агрессивных опухолях
Врачи давно замечают, что многие опухоли яичников становятся резистентными к химиотерапии и широко распространяются в брюшной полости. Одним из ключевых факторов является процесс, называемый эпителиально-мезенхимальным переходом (EMT), при котором раковые клетки ослабляют межклеточные связи, становятся более подвижными и ведут себя скорее как агрессивные «бродяги», чем как упорядоченные клетки ткани. Авторы показывают, что TGase 2, который в норме присутствует в яичнике на очень низком уровне, а в опухолях — значительно чаще, тесно связан с этим переходом. В большой серии образцов человеческих тканей уровень TGase 2 постепенно повышался от ранних стадий до продвинутой и метастатической болезни, и его содержание хорошо коррелировало с активностью многих генов, связанных с EMT, которые управляют движением клеток, их ростом и ангиогенезом. 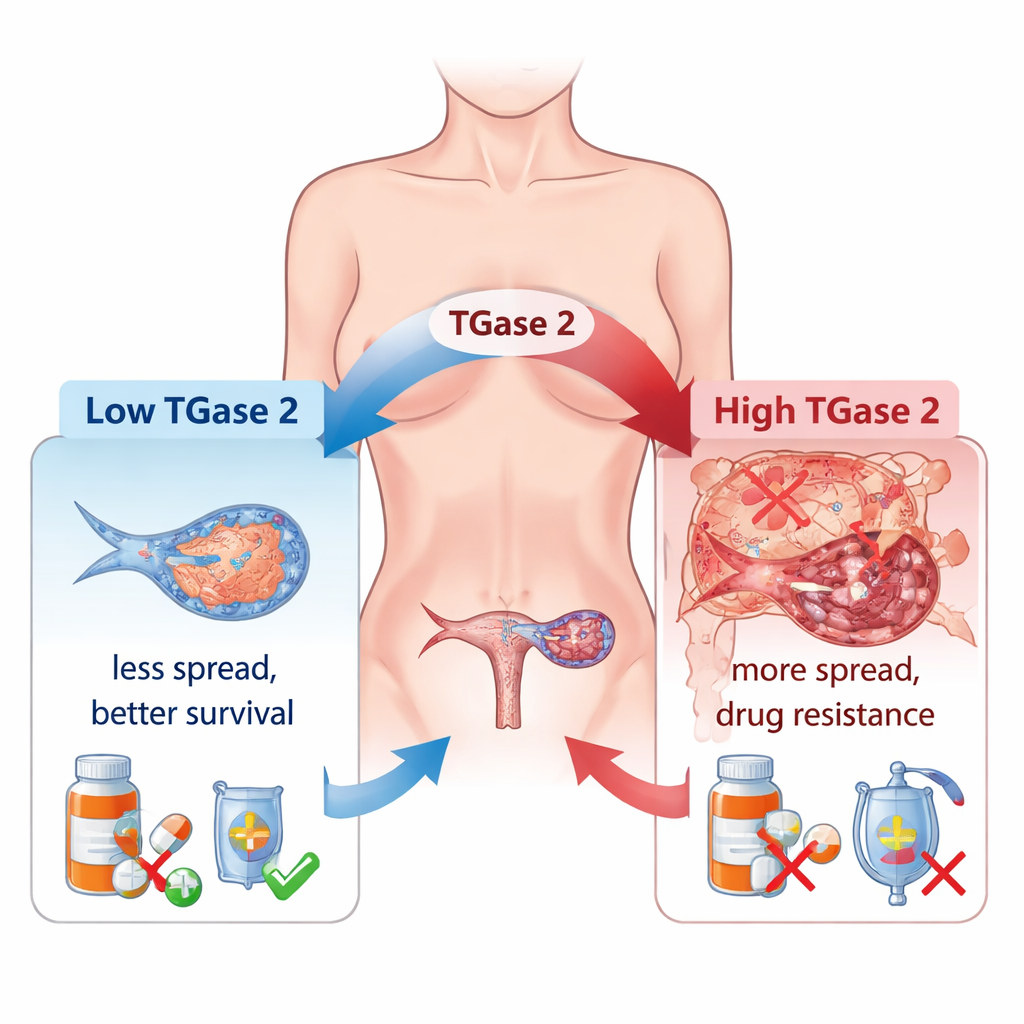
Как TGase 2 отключает важный предохранитель
Чтобы понять, что именно делает TGase 2 внутри раковых клеток, исследователи сосредоточились на его взаимодействии с другим белком, GSK3β. В норме GSK3β действует как тормоз инвазии: он удерживает уровень сигнальной молекулы β-катенина низким, что, в свою очередь, сдерживает гены, запускающие EMT. Команда обнаружила, что TGase 2 физически связывается с GSK3β, ослабляет его активность и способствует направлению белка на разрушение через клеточную систему утилизации — аутофагию. При высокой экспрессии TGase 2 клетки рака яичников активнее мигрировали и демонстрировали повышенные уровни классических маркеров EMT, таких как фибронектин, виментин и β-катенин. При снижении TGase 2 с помощью генетических методов эти инвазивные признаки уменьшались, а сигнальный путь β-катенина затухал, что доказывает: TGase 2 отключает ключевой предохранитель против метастазирования.
От клеток в культуре до живых животных
Далее команда проверила, может ли блокировка TGase 2 замедлить рост опухоли в живых организмах. Они создали линии раковых клеток яичников без гена TGase 2 и имплантировали их мышам. По сравнению с животными, получившими обычные раковые клетки, у мышей, получивших клетки с дефицитом TGase 2, формировалась меньшая опухолевая нагрузка, и они жили дольше. В отдельной модели, имитирующей распространение рака через кровоток, у мышей, которым вводили клетки без TGase 2, развивалось намного меньше и меньшие по размеру метастазов в легких. Важно, что в этих метастатических очагах наблюдались более высокие уровни GSK3β, что согласуется с идеей о том, что удаление TGase 2 восстанавливает природный тормоз инвазии и помогает сдерживать болезнь.
От лабораторной подсказки к лекарственной стратегии
Поскольку удаление гена непрактично у пациентов, авторы протестировали малое молекулярное соединение стрептонигрин, ранее известное способностью связываться с тем же концом TGase 2, который использует белок для захвата партнеров. Они обнаружили, что стрептонигрин может разрушать взаимодействие TGase 2 и GSK3β в клетках, снижать их ко-локализацию и ограничивать миграцию раковых клеток. В модельных исследованиях на мышах пероральное лечение стрептонигрином замедляло рост опухоли, уменьшало метастатические очаги и продлевало выживаемость. Самое примечательное: при комбинировании стрептонигрина со стандартными препаратами химиотерапии, такими как цисплатин или паклитаксел, мыши жили на недели дольше, чем при одной химиотерапии. Сама по себе химиотерапия склонна повышать уровень TGase 2 и снижать GSK3β, что косвенно сдвигает клетки в сторону EMT, тогда как добавление блока TGase 2 обращало этот тренд и ограничивало возросшую подвижность клеток. 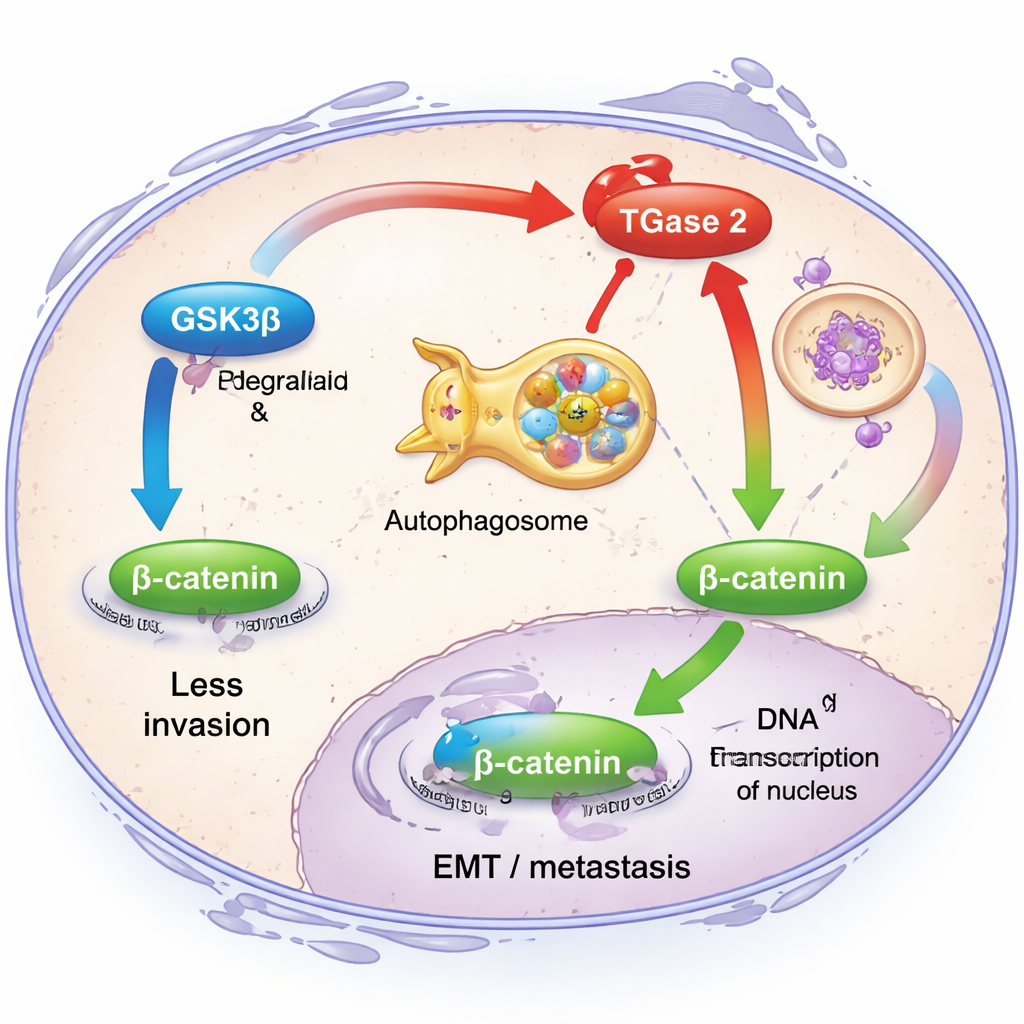
Что это может означать для будущего лечения
Для неспециалиста ключевая мысль такова: клетки рака яичников эксплуатируют TGase 2, чтобы отключить встроенный тормоз против метастазирования и пережить удар химиотерапии. Напрямую инактивируя GSK3β и стабилизируя β-катенин, TGase 2 делает опухоли более инвазивными и устойчивыми к лекарствам. Эта работа предполагает, что препараты, нацеленные на N-концевую область TGase 2 — такие как стрептонигрин или будущие, более безопасные соединения по его образцу — могут повысить эффективность существующей химиотерапии, снизить вероятность рецидива и улучшить выживаемость. Проще говоря, таргетинг TGase 2 может перекрыть «маршрут побега» рака, делая опухоли яичников более чувствительными к лечению и менее способными распространяться.
Цитирование: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Ключевые слова: рак яичников, устойчивость к препаратам, метастазирование, эпителиально-мезенхимальный переход, таргетная терапия