Clear Sky Science · ru
Ингибирование внутренней переработки B‑клеточного рецептора (BCR), индуцированной автоантигеном, как терапевтическая стратегия при диффузной крупноклеточной В‑клеточной лимфоме (DLBCL)
Почему это важно для пациентов
Диффузная крупноклеточная В‑клеточная лимфома (DLBCL) — самая распространённая быстрорастущая злокачественная опухоль крови у взрослых, и многие пациенты всё ещё испытывают рецидивы после стандартной химио‑иммунотерапии. В этом исследовании изучается неожиданный уязвимый пункт в крупном подтипе этих опухолей: их зависимость от клеточной «антенны» на поверхности — B‑клеточного рецептора (BCR). Показав, что блокирование захвата этой «антенны» внутрь клетки может подорвать выживание раковых клеток, работа открывает возможность перепрофилирования давно используемых противорвотных и антипсихотических препаратов в качестве целевых вспомогательных средств против лимфомы.
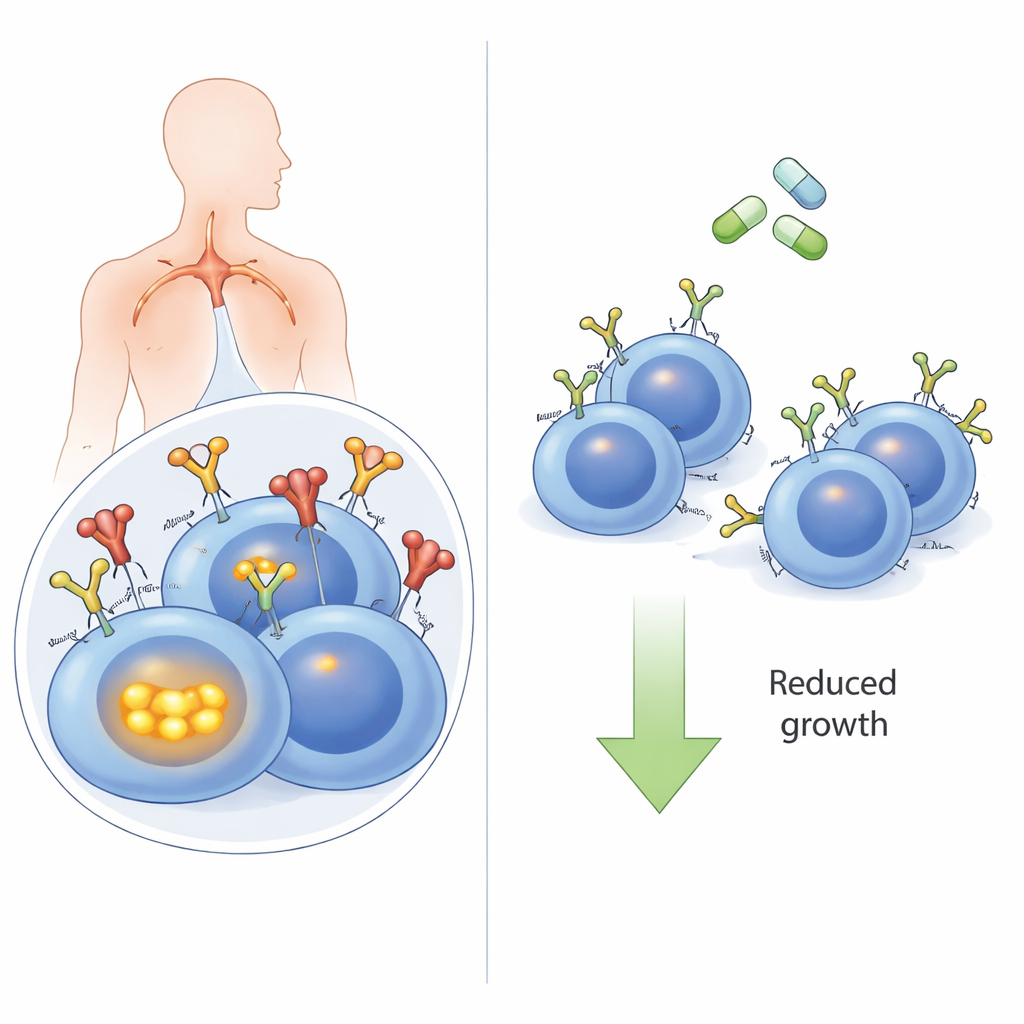
Антенна раковой клетки
В‑клетки, вид белых кровяных клеток, используют B‑клеточный рецептор на своей поверхности для распознавания угроз. Во многих DLBCL, особенно в высоко‑рисковом подтипе «активированных В‑клеток» (ABC), этот же рецептор используется в корыстных целях для постоянной передачи сигналов «выживай и делись». Часто эти BCR распознают собственные молекулы организма (аутоантигены), действующие как заевший дверной звонок. Когда аутоантигены связываются, BCR делает не только поверхностную сигнализацию: он втягивается внутрь клетки и объединяется во внутренний белковый кластер с сенсорами, называемыми TLR9 и MYD88. Этот суперкомплекс затем включает NFκB — мощный путь, стимулирующий рост. До сих пор оставалось неясным, действительно ли внутренняя транспортировка рецептора необходима для сигнала, приводящего к опухолевому росту.
Перенастройка «антенны», чтобы проверить её роль
Чтобы ответить на этот вопрос, исследователи использовали CRISPR‑редактирование генов для точечной замены «кончиков» BCR в линиях лимфомных клеток. Они заменили естественные, самореактивные участки распознавания на варианты, которые узнают овальбумин — безвредный яичный белок, используемый в лабораторных экспериментах. Эти модифицированные рецепторы больше не захватывали обычные аутоантигены, но могли быть активированы контролируемо добавлением овальбумина. В клетках лимфомы типа ABC, которые обычно зависят от связывания с собственными антигенами, такая замена резко снизила активность многих ключевых сигнальных ферментов и подавила гены, реагирующие на NFκB. Клетки росли медленнее, несмотря на то, что на их поверхности фактически оказалось больше BCR, что показывает: непрерывное взаимодействие с аутоантигенами и последующая внутренняя сигнализация критически важны для их выживания.
Втягивание рецепторов внутрь: критический этап
Затем команда напрямую изучила, что происходит с BCR после встречи с антигеном. В их смоделированных системах как антителоподобные триггеры, так и овальбумин вызывали исчезновение рецептора с поверхности клетки в течение нескольких минут, подтверждая быструю эндоцитоз. Это происходило не только когда антиген находился вне клетки, но и когда он был искусственно представлен на мембране той же клетки, моделируя некоторые реальные опухолевые ситуации. Генетическое блокирование этого внутреннего транспорта, с помощью доминант‑негативной формы белка динамина‑2, который необходим для клатрин‑зависимого эндоцитоза, сохраняло BCR на поверхности, уменьшало внутренние комплексы BCR–TLR9–NFκB, снижало экспрессию генов‑мишеней NFκB и замедляло рост клеток. Что интересно, при блокировании эндоцитоза некоторые «фоновые» сигналы BCR на поверхности увеличивались, что указывает на попытку раковых клеток компенсировать утрату путем усиления более слабого, «тонического» режима сигнализации.
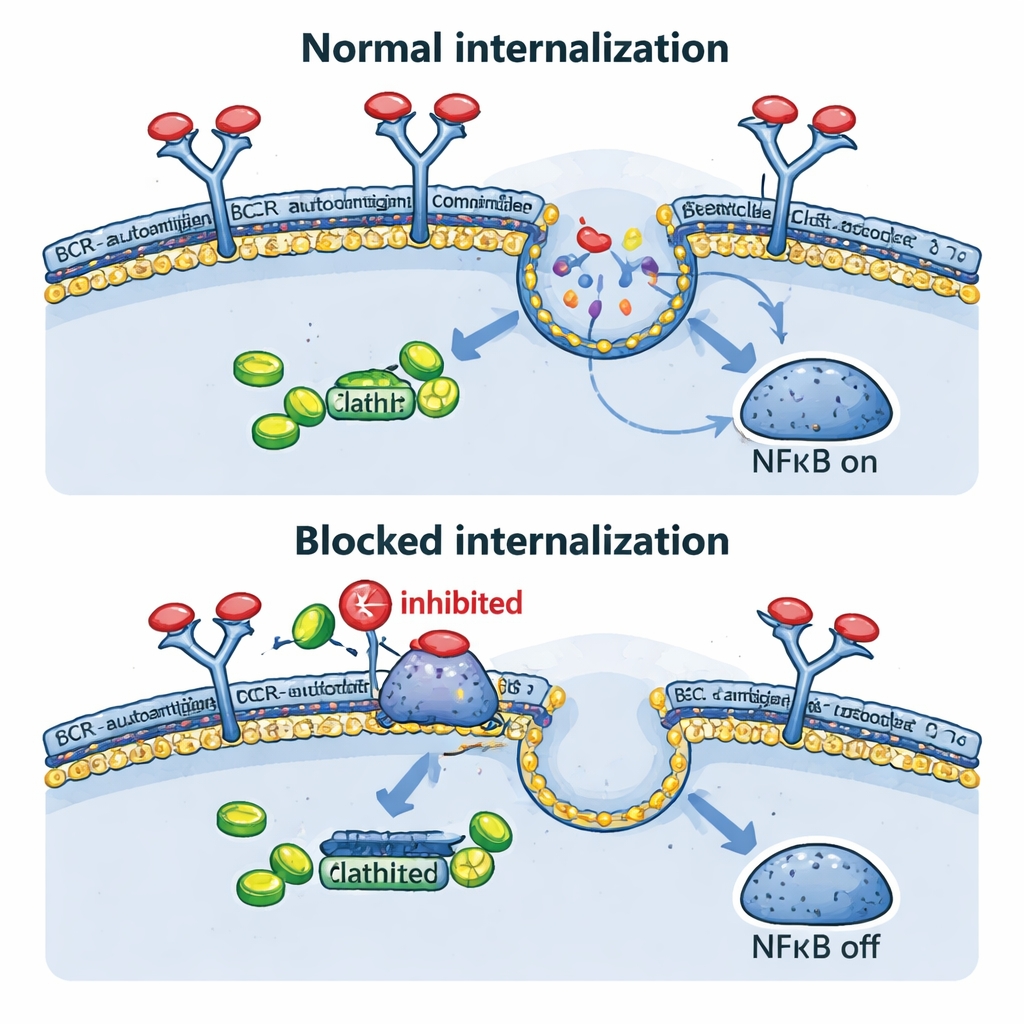
Старые препараты — новые приемы
Поскольку разработка новых лекарств медленна и дорога, авторы проверили, могут ли существующие препараты, блокирующие эндоцитоз, имитировать генетические эксперименты. Фенотиазины, семья антипсихотических и противорвотных веществ, известны своим ингибирующим действием на динамин‑2 и на клатрин‑зависимый захват рецепторов. В лимфомных клетках такие соединения, как прохлорперазин и хлорпромазин, повышали уровни BCR на поверхности и значительно снижали антиген‑индуцированный эндоцитоз. Это приводило к уменьшению активности генов, управляемых NFκB, и снижению жизнеспособности клеток DLBCL типа ABC, особенно у тех, у кого компоненты BCR оставались интактными. У мышей с трансплантатами человеческой лимфомы прохлорперазин в клинически достижимых дозах существенно замедлял рост опухолей. Кроме того, сочетание фенотиазинов с препаратами, блокирующими другие связанные с BCR ферменты, такие как SYK и PI3Kδ, давало более сильный противоопухолевый эффект, чем каждая терапия по‑отдельности.
Что это может значить для лечения
В целом исследование показывает, что для существенной подгруппы DLBCL опухолеобразующие сигналы идут не просто от рецепторов на поверхности клетки; они критически зависят от втягивания комплекса BCR–антиген внутрь через специфический путь эндоцитоза. Прерывание этого шага — либо генетически, либо при помощи фенотиазинов — ослабляет сигналы NFκB и нарушает выживание опухолевых клеток, одновременно потенциально повышая чувствительность к существующим ингибиторам BCR‑пути. Поскольку фенотиазины уже имеют хорошо изученные режимы дозирования и профиль безопасности как противорвотные препараты, эта работа предоставляет реалистичную основу для клинических испытаний, в которых их можно проверить в монорежиме или в комбинации у пациентов с лимфомами, демонстрирующими автоантиген‑зависимую активность BCR.
Цитирование: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Ключевые слова: диффузная крупноклеточная В‑клеточная лимфома, B‑клеточный рецептор, эндоцитоз, фенотиазины, сигнализация NFkB