Clear Sky Science · ru
Временное мультиомное исследование воздействия паклитаксела на сенсорные нейроны человека, полученные из iPSC, выявляет механизмы химиотерапевтически-индуцированной периферической невропатии
Почему некоторые противораковые препараты повреждают нервы
Химиотерапия помогла миллионам людей выжить после рака, но многие пациенты расплачиваются скрытой ценой: месяцами или годами их мучит жгучая боль, покалывание и онемение в руках и ногах. В этом исследовании ставится простой, но важный вопрос: что именно делает широко используемый противораковый препарат паклитаксел с человеческими сенсорными нейронами, и может ли понимание этих изменений указать путь к лучшей профилактике и лечению такого повреждения нервов?
От клеток пациентов до лабораторно выращенных нервов, чувствующих боль
Вместо того чтобы полагаться на эксперименты на животных, исследователи начали с клеток пяти доноров человека, в том числе пациентов с раком молочной железы, получавших паклитаксел. Они перепрограммировали эти клетки в индуцированные плюрипотентные стволовые клетки, а затем направили их дифференцировку в сенсорные нейроны — тот же тип нервных клеток, который передаёт тактильные и болевые сигналы от кожи к спинному мозгу. Эти лабораторно выращенные нейроны образовали длинные тонкие волокна и проявляли электрическую активность, похожую на настоящие болевые нервы в организме. Команда подвергла их воздействию возрастающих доз паклитаксела, имитируя уровни препарата, наблюдаемые у пациентов, и отслеживала состояние клеток в течение нескольких дней. При низких концентрациях нейроны справлялись, но при клинически релевантной дозе (100 нМ) их выживаемость начала снижаться примерно через два дня, что отметило начало токсического повреждения нервов.
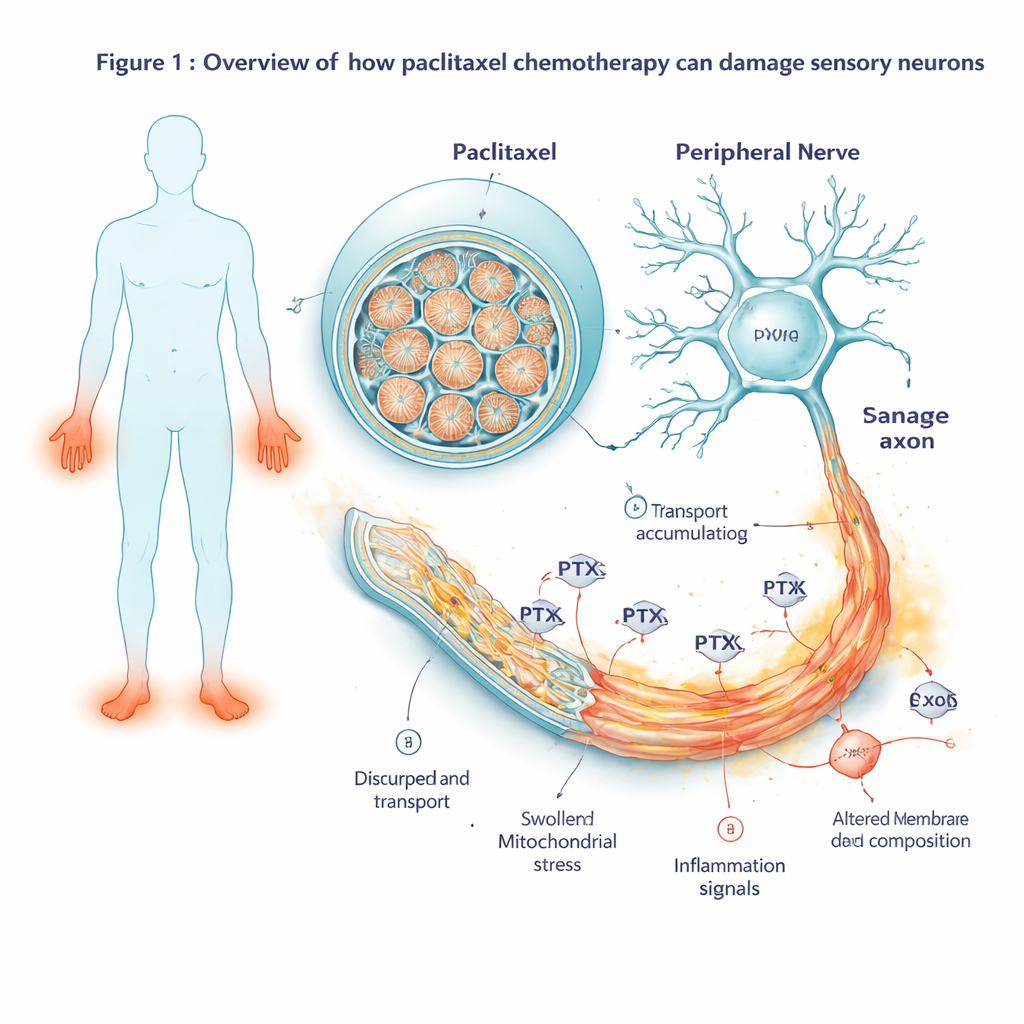
Наблюдение за изменением активности генов во времени
Чтобы увидеть, как клетки реагируют до того, как они начнут заметно деградировать, учёные измеряли, какие гены включаются или выключаются в нескольких временных точках — от двух часов после воздействия препарата до нескольких дней после его удаления. На ранних этапах они обнаружили активацию классической программы клеточного стресса, в центре которой стоит ген JUN. По мере продолжения воздействия этот стрессовый сигнал развернулся в полноценную каскаду самоуничтожения: гены, продвигающие программируемую смерть клетки, оказались сильно включёнными, в то время как защитные компоненты были подавлены. Одновременно усилилась активность генов, связанных с воспалением и болевой сигнализацией. Нейроны начали производить больше провоспалительных молекул, пептидов, связанных с болью, и рецепторов, повышающих чувствительность клеток к вредным стимулам — изменения, которые соответствуют тем, что наблюдаются при болевых нейропатиях.
Глубокое изучение белков и липидов внутри нейронов
Поскольку гены — лишь чертежи, команда также исследовала белки, фактически присутствующие в нейронах, а также их липидный (жировой) состав. Через 48 часов воздействия паклитаксела многие из тех же стрессовых и провоспалительных сигналов, обнаруженных на уровне РНК, проявились и как повышенные уровни белков, что подтвердило, что нейроны реализуют эти вредные программы. Поразительно, что белки, необходимые для аксоплазматического транспорта — молекулярные моторы и каркасные компоненты, перемещающие грузы вдоль длинных нервных волокон — были резко снижены. Сюда входили кинезины и регуляторные белки, поддерживающие стабильность микротубулов. На уровне липидов нейроны демонстрировали падение ключевых строительных блоков для холестерина и мембранных липидов, одновременно с ростом запасённых жиров — триацилглицеролов. В совокупности эти изменения указывают на то, что паклитаксел не только запускает пути клеточной гибели, но и ослабляет физическую структуру и энергетический баланс нервных волокон.
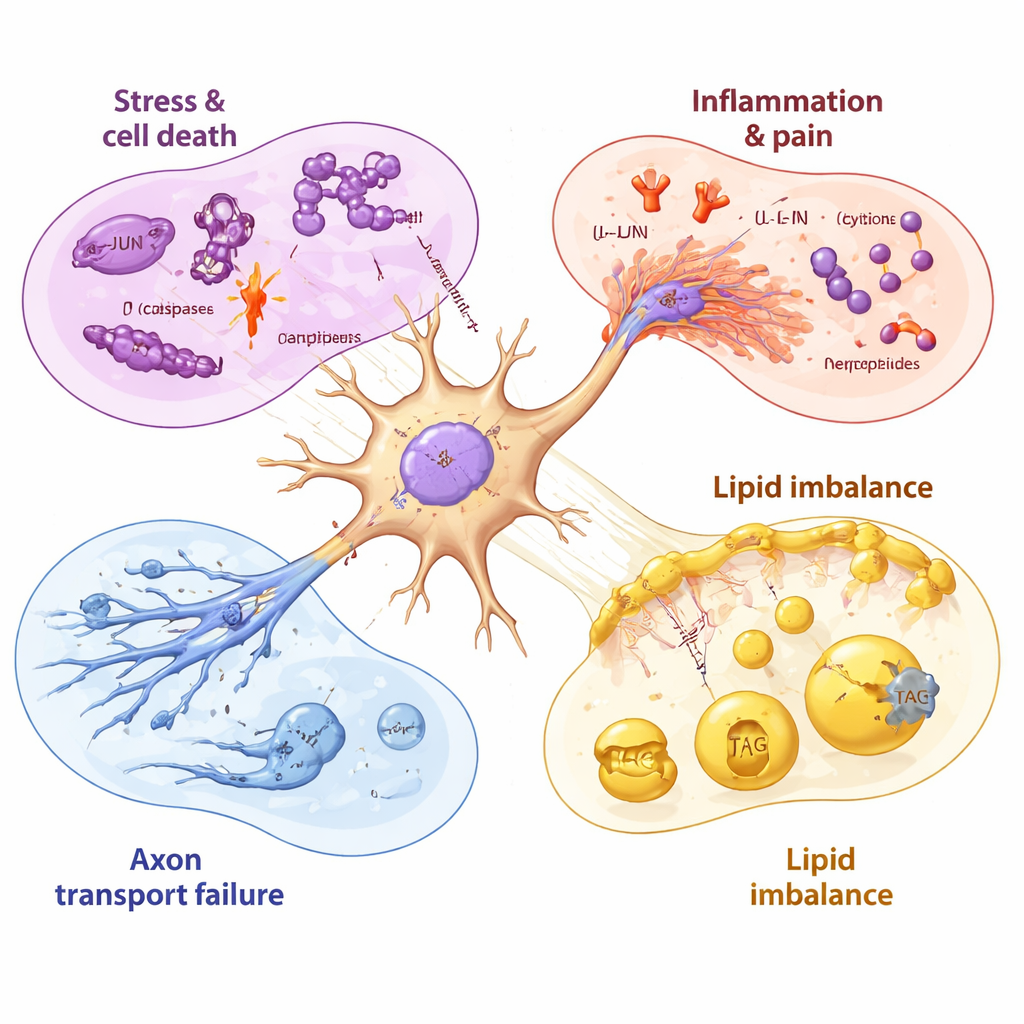
Хронология повреждения нервов и неполного восстановления
Благодаря взятиям проб до, во время и после воздействия препарата исследователи смогли упорядочить эти события во времени. Митохондриальные (энергетические) гены нарушались в течение нескольких часов, за ними следовал стрессовый ген JUN, затем — более сильная активация программ клеточной гибели и воспаления по мере снижения жизнеспособности. Даже после удаления паклитаксела многие вредные сигналы оставались повышенными в течение дней, тогда как гены, необходимые для синтеза здоровых мембранных липидов, продолжали снижаться. Некоторые молекулы, появляющиеся на поздних стадиях, такие как насос выведения лекарств, способный удалять паклитаксел, и определённые факторы роста, указывали на попытки нейронов защититься и восстановиться — но эти реакции выглядели относительно медленными и неполными по сравнению с быстрым ранним сдвигом в сторону повреждения.
Что это значит для пациентов, живущих с нервной болью
Для неспециалиста вывод таков: паклитаксел повреждает сенсорные нервы серией скоординированных ударов — он нарушает их энергетические системы, переключает генетические программы в сторону гибели клеток, вызывает воспаление и усиление болевой сигнализации, нарушает внутренние «транспортные магистрали» в нервных волокнах и изменяет липиды, поддерживающие стабильность мембран. Картирование этих изменений в нейронах, полученных от человека, с высокой степенью детализации выделяет конкретные, «лекарственно-удобные» мишени — такие как специфические регуляторы стресса, воспалительные рецепторы и ферменты липидного синтеза — которые можно было бы либо блокировать, либо поддерживать, чтобы защитить нервы, не ослабляя противораковую терапию. Хотя новые подходы потребуют дальнейших испытаний, эта работа даёт более чёткую дорожную карту для предотвращения или смягчения химиотерапевтически-индуцированного повреждения нервов, улучшая качество жизни выживших после рака.
Цитирование: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Ключевые слова: химиотерапевтически-индуцированная периферическая невропатия, паклитаксел, сенсорные нейроны, нейровоспаление, дегенерация аксонов