Clear Sky Science · ru
Обратимая метилирование аргинина регулирует активность митохондриального IDH2: скоординированный контроль со стороны CARM1 и KDM3A/4A
Тонкая настройка энергетических центров клетки
Митохондрии, часто называемые энергетическими станциями наших клеток, выполняют гораздо больше функций, чем просто вырабатывают энергию. Они постоянно подстраивают способы сжигания топлива под потребности организма, и сбои в этой регулировке могут способствовать развитию таких заболеваний, как диабет, сердечная недостаточность и рак. В этом исследовании раскрыт скрытый «диммер» внутри митохондрий: небольшая химическая метка на одном строительном блоке ключевого фермента IDH2, которая помогает решать, будут ли митохондрии работать в режиме покоя или увеличивать выработку энергии.
Маленькая метка — большие последствия
Белки в наших клетках не статичны; их часто модифицируют малыми химическими группами, что меняет их поведение. Хотя многие такие модификации в ядре и цитоплазме хорошо изучены, модификации внутри митохондрий исследованы меньше. Авторы сосредоточились на одном конкретном виде метки — метилировании аргинина — и спросили, не управляет ли она работой митохондриальных ферментов. Они сосредоточились на ферменте IDH2, ключевом элементе цикла трикарбоновых кислот (ЦТК), который помогает превращать питательные вещества в энергию и важные метаболические компоненты. С помощью биохимических методов и масс-спектрометрии они обнаружили, что IDH2 несет специфическую метильную метку на одном аминокислотном остатке — аргинине 188, и что эту метку наносит фермент CARM1, который, как ни удивительно, действует внутри митохондрий.
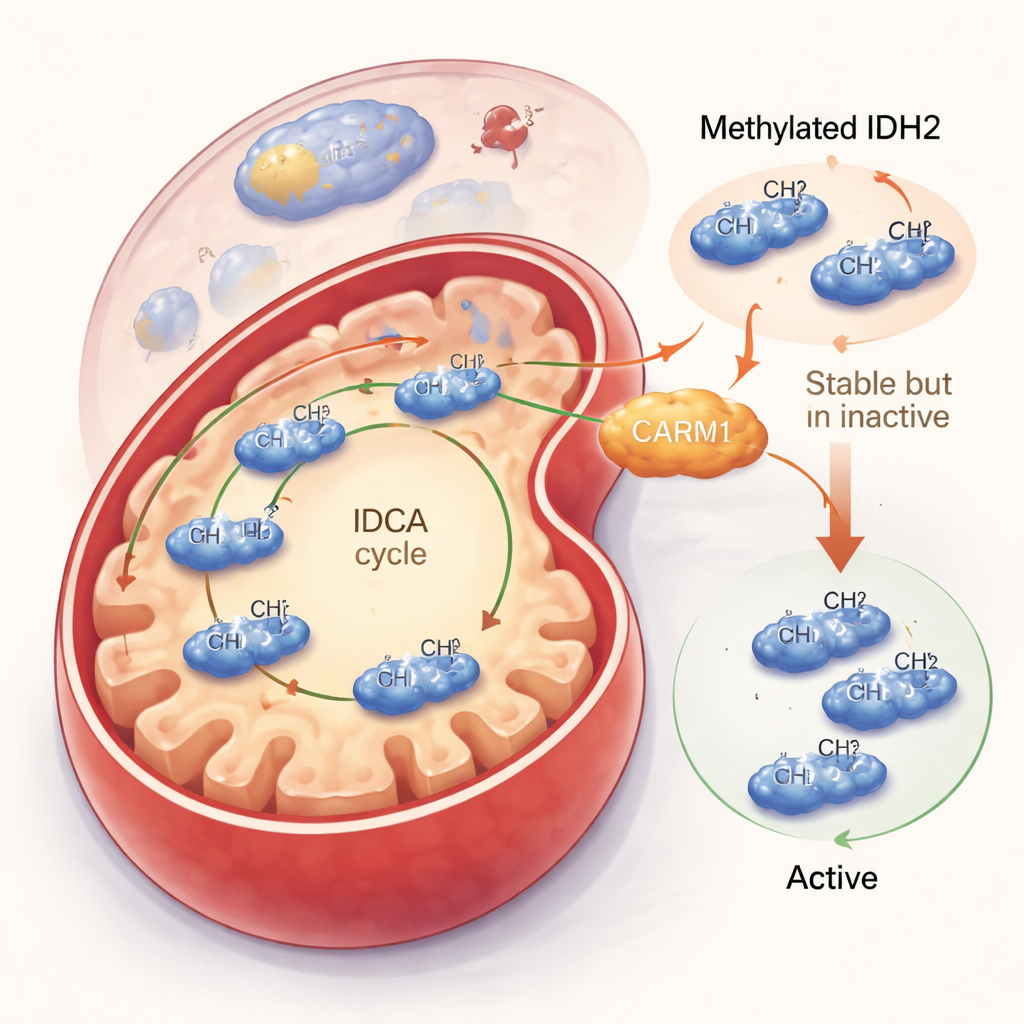
Понижая активность IDH2, но увеличивая его устойчивость
Далее команда выясняла, что делает эта метильная метка. Когда CARM1 был активен и мог метилировать IDH2, белок IDH2 становился более стабильным и дольше сохранялся в клетке. Но это «плюс» имел обратную сторону: метилированный IDH2 был менее активен. В клеточных экспериментах и на очищенном белке метилированный IDH2 вырабатывал меньше своего основного продукта — α-кетоглутарата — и производил меньше защитного молекулы NADPH. Напротив, версия IDH2, которая не могла быть метилирована в аргинине 188, формировала больше активного димерного состояния, работала быстрее и повышала уровни как α-кетоглутарата, так и NADPH. Несмотря на то что общей суммы такого неметилированного IDH2 было меньше, каждая молекула выполняла больше работы, что приводило к чистому увеличению митохондриальной активности.
Обратимый переключатель с двумя «стерками»
Критично, что эта метильная метка не является постоянной. Исследователи показали, что два фермента, обычно известные как дезметилазы лизина — KDM3A и KDM4A — также могут удалять метильную метку с аргинина IDH2. В присутствии этих деметилаз метилированный аргинин на позиции 188 терял свои дополнительные химические группы, IDH2 становился менее стабильным, но более активным, а его димерная форма увеличивалась. Клетки с повышенной активностью KDM3A или KDM4A демонстрировали более высокий митохондриальный мембранный потенциал и потребляли больше кислорода — признаки того, что их митохондрии работали активнее в режиме окислительного метаболизма. Когда эти ферменты уменьшали, происходило обратное: активность IDH2 падала и митохондриальная функция снижалась, что подчеркивает, что это обратимая система контроля, а не однонаправленное изменение.
Связь между метаболизмом и болезнями
Поскольку IDH2 связывают с раком и другими нарушениями, авторы изучили, как этот метиловый переключатель может влиять в условиях, сходных с болезнью. В различных нормальных и раковых клеточных линиях они наблюдали, что повышенные уровни белка IDH2 часто сопровождались большей степенью метилирования и, что немаловажно, сниженной активностью фермента, что указывает на то, что «больше белка» не всегда означает «больше функции». В наборах данных по раку молочной железы пациенты с более высоким уровнем белка IDH2 обычно имели худший прогноз выживаемости, хотя активность гена IDH2 не коррелировала с исходом. Результаты поддерживают модель, в которой метилирование, направляемое CARM1, замедляет цикл ЦТК и смещает клетки в сторону альтернативных путей использования питательных веществ, благоприятствующих раку, тогда как деметилазы, такие как KDM3A и KDM4A, могут вернуть клетки к более эффективному производству энергии.
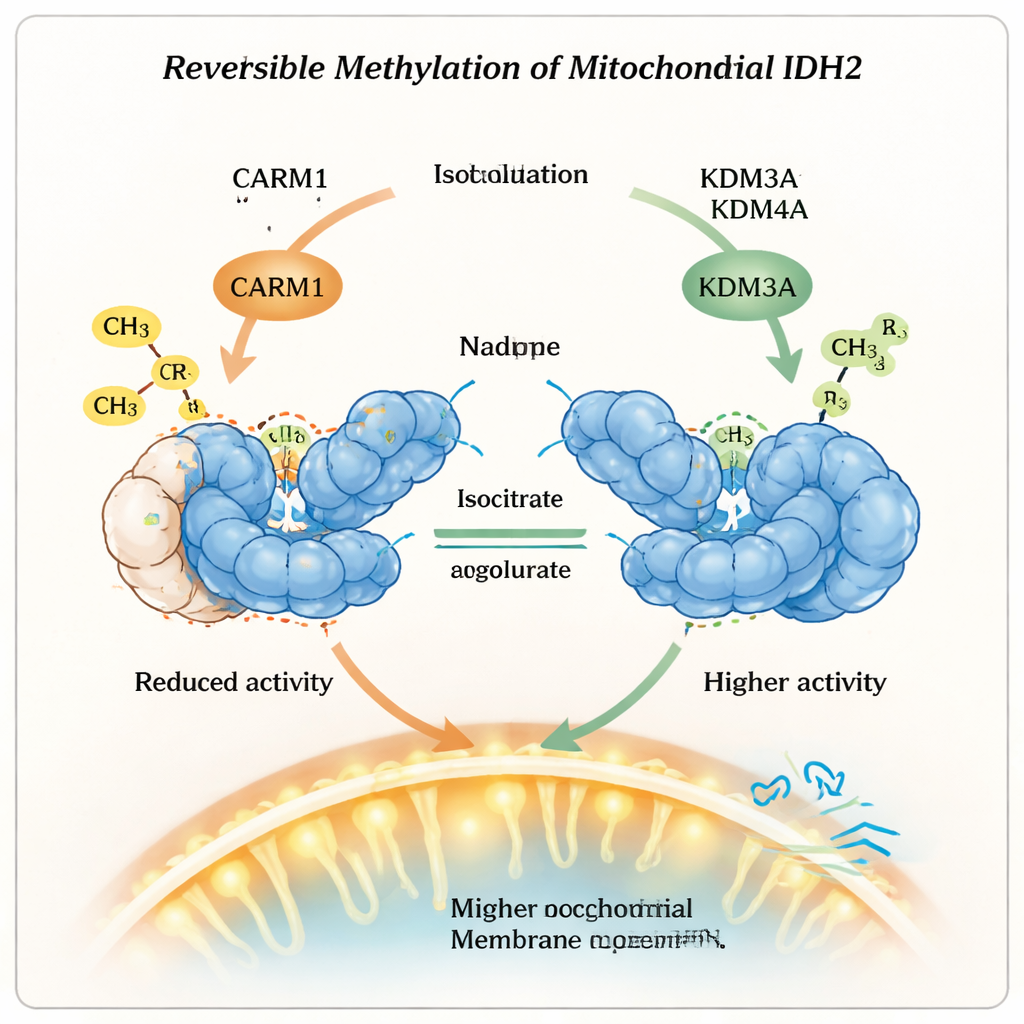
Что это значит для здоровья и терапии
Проще говоря, эта работа показывает, что митохондрии не просто включают или выключают ферменты, а используют обратимые химические метки как тонкие регуляторы. Добавляя метильную группу, CARM1 превращает IDH2 в более долговечную, но менее активную форму; удаляя эту метку, KDM3A и KDM4A жертвуют частью стабильности ради большего энергетического выхода. Этот баланс влияет на то, как клетки выбирают между быстрым, но неэффективным сжиганием сахара и медленным, но более эффективным производством энергии. Понимание этого метилового «диммера» на IDH2 открывает новые возможности для терапий, направленных на исправление нарушенного митохондриального метаболизма при таких состояниях, как рак и метаболические заболевания, путем нацеливания на ферменты, которые пишут и стирают эти маленькие, но мощные химические метки.
Цитирование: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Ключевые слова: митохондрии, IDH2, метилирование аргинина, клеточный метаболизм, CARM1