Clear Sky Science · ru
Воспалительный контур MIF–p38–GSDMD в кератиноцитах лежит в основе UVB‑индуцированной кожной волчанки
Почему солнечный свет может представлять серьёзную проблему при волчанке
Для большинства людей солнце вызывает лишь загар или, в худшем случае, солнечный ожог. Но у многих пациентов с волчанкой несколько минут облучения ультрафиолетом B (UVB) могут спровоцировать болезненные, длительно сохраняющиеся высыпания и даже усугубить общее течение болезни. В этом исследовании раскрыт скрытый «петлевой» механизм внутри клеток кожи, который помогает объяснить их повышенную светочувствительность — и указывает на новые местные подходы к лечению, которые могли бы усмирить реакцию, не подавляя всю иммунную систему.
Клетки кожи как неожиданные нарушители
Врачи давно знали, что при кожном первичном системном заболевании—эритематозной волчанке (CLE) наблюдаются хроническое воспаление и рубцевание кожи, но внимание часто сосредотачивалось на вторгающихся иммунных клетках. Используя секвенирование РНК по одиночным клеткам, авторы вместо этого сосредоточились на собственных клетках кожи — кератиноцитах в наружном слое и фибробластах в глубине. Они обнаружили, что у пациентов с волчанкой определённые подтипы кератиноцитов расширены и демонстрируют выраженный «интерфероновый сигнатурный» профиль, то есть набор антивирусных генов, постоянно включённых. Среди этих аномальных кератиноцитов выделялся один сигнальный белок: фактор ингибирования миграции макрофагов (MIF), который продуцировался в значительно больших количествах, чем более знакомые воспалительные молекулы, такие как TNF или IL‑6.
Скрытый посредник, выпускаемый под воздействием света
Обнаружение высокого уровня MIF внутри кератиноцитов само по себе не объясняло, почему свет так опасен. При облучении культивируемых кератиноцитов UVB исследователи обнаружили, что общий внутриклеточный уровень MIF почти не меняется — но белок выделялся в окружающую жидкость в дозозависимом режиме. Чем больше UVB, тем больше MIF просачивалось наружу, что тесно коррелировало с маркером повреждения мембран. Когда эта MIF‑богатая жидкость наносилась на свежие кератиноциты и фибробласты, она вызывала характерные для CLE изменения: рост воспалительных цитокинов и ферментов, разрушающих и перестраивающих опорный матрикс кожи. Подавление MIF генетическими средствами или блокада небольшим молекулярным препаратом резко снижали эти вредные реакции, показывая, что MIF, происходящий из кератиноцитов, — не просто попутчик, а ключевой усилитель UVB‑опосредованного повреждения. 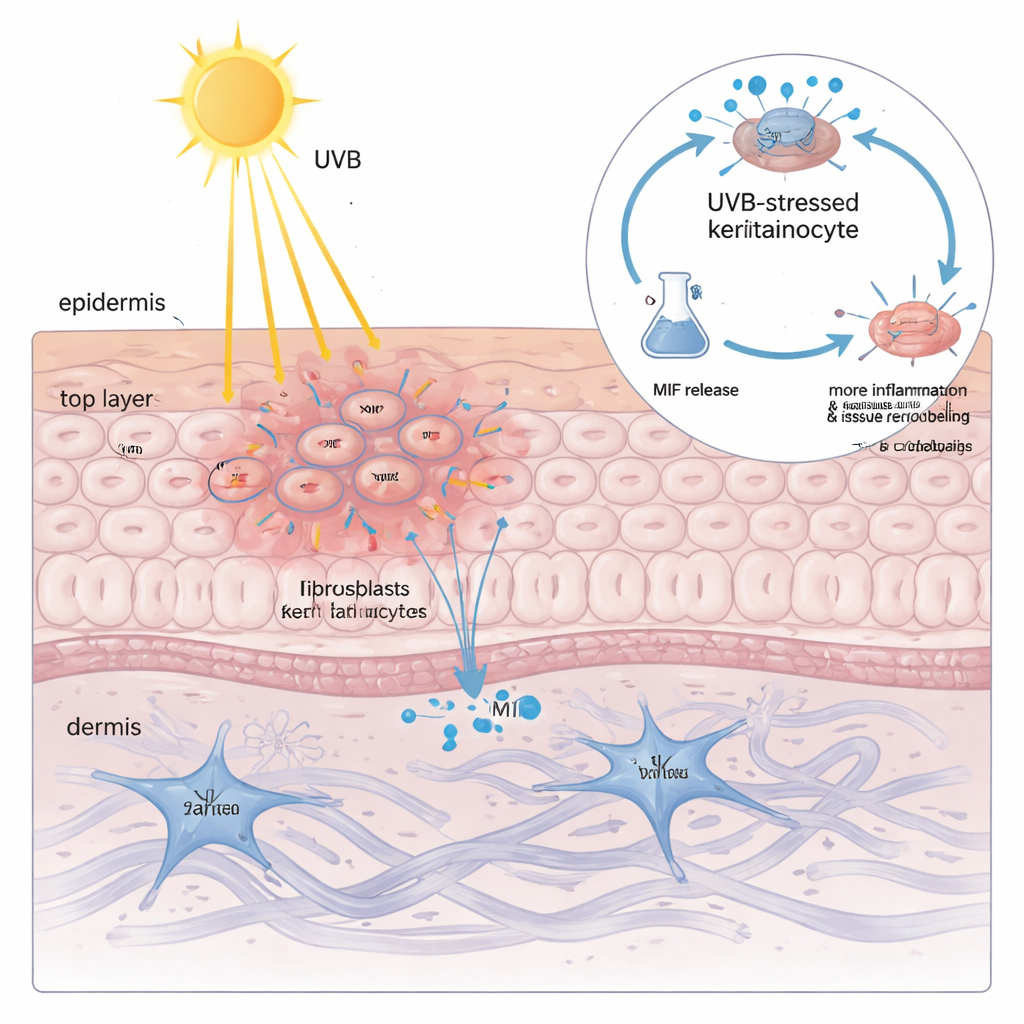
Самоподдерживающийся воспалительный контур внутри кератиноцитов
Чтобы понять, как UVB заставляет кератиноциты выделять MIF, исследователи создали «волчанко‑подобную» модель кератиноцита, нагружая клетки их собственной ДНК и РНК, имитируя плохо утилизируемые генетические обломки, характерные для волчанки. В этом предварительно подготовленном состоянии UVB активировал так называемый риботоксический стресс‑ответ: сигнал повреждения от рибосом, который включал киназу ZAKα и, в свою очередь, стресс‑фермент p38. Этот путь усиливал другой белок — транскрипционный фактор C/EBPβ, который связывался с регуляторной областью гена NLRP3 и активировал его. NLRP3 затем приводил к расщеплению GSDMD, порообразующего белка, который пробивает отверстия в клеточной мембране и вызывает воспалительную форму гибели клетки, известную как пироптоз. Существенно, MIF выходил преимущественно через эти поры GSDMD — не через обычные секреторные везикулы. Оказавшись снаружи, MIF связывался с поверхностным рецептором CD74 на кератиноцитах, повторно активируя p38, NLRP3 и GSDMD и тем самым замыкая порочный круг: UVB → p38 → NLRP3 → поры GSDMD → выделение MIF → усиление активации p38.
От молекулярного понимания к новым местным лечебным подходам
Этот контур оказался не просто лабораторным курьёзом. У мышей, предрасположенных к волчанке, облучение UVB вызвало тяжёлые кожные поражения с высокими уровнями MIF, активацией p38, NLRP3 и расщеплённого GSDMD в эпидермисе. Когда исследователи использовали вирус для генной терапии с целью избирательного заглушения гена Mif в коже, UVB‑индуцированные высыпания становились гораздо мягче, а маркёры воспаления и ремоделирования тканей снижались как в кератиноцитах, так и во фибробластах. Чтобы избежать системных побочных эффектов лекарств, они также разработали растворимые микроигольные пластыри, загруженные ингибитором MIF ISO‑1. Короткое нажатие таких крошечных игл на кожу безболезненно доставляло препарат в верхние слои. Леченные мыши с предрасположенностью к волчанке после UVB развивали значительно меньше и менее тяжёлых поражений, а молекулярный след контура MIF–p38–GSDMD был заметно ослаблен. 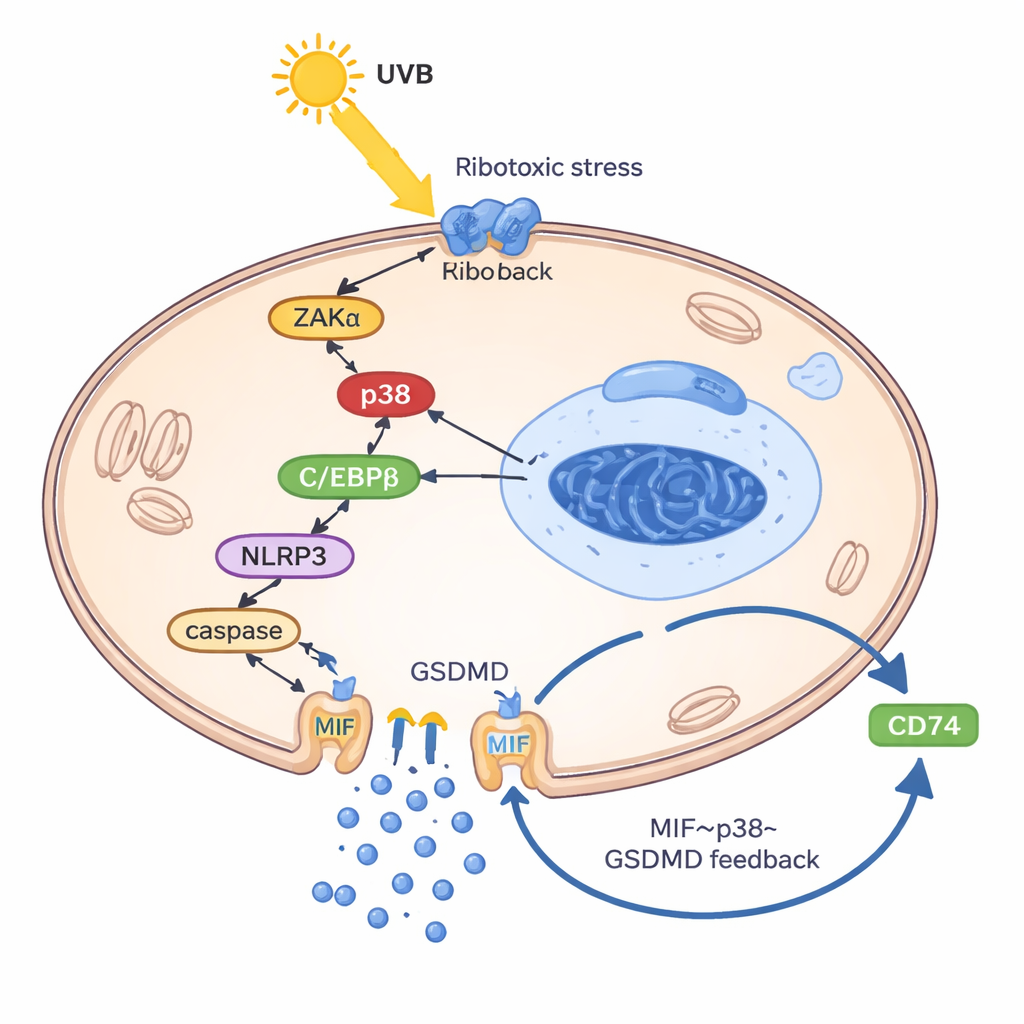
Что это значит для людей с волчанкой
Проще говоря, работа показывает, что при волчанке определённые клетки кожи склонны чрезмерно реагировать на UVB, выпуская мощную «усиливающую» молекулу MIF через самоповреждённые мембранные поры. Это усиление затем подпитывает воспалительный механизм, который может поддерживаться даже после окончания первоначального облучения. Поэтапная карта этого контура указывает на то, что блокада MIF непосредственно в коже — с помощью генетического подавления или умных систем доставки вроде микроигольных пластырей — может разорвать цикл фоточувствительных обострений, не требуя широкого подавления иммунной системы. Если подобные стратегии окажутся безопасными и эффективными у людей, они могут дать пациентам с волчанкой новые способы комфортнее жить на свету.
Цитирование: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Ключевые слова: кожная волчанка, фоточувствительность, кератиноциты, воспалительный контур, микроигольная терапия