Clear Sky Science · ru
Хонокинол блокирует развитие опухолей и метастазирование через направленные на митохондрии эффекты
Превращение вещества из коры дерева в противораковый агент
Многие противораковые препараты происходят из растений, и учёные продолжают выяснять, как некоторые из этих природных молекул действуют внутри наших клеток. В этом исследовании уделено внимание хонокинолу — веществу, обнаруженному в коре магнолии и давно используемому в традиционной медицине. Показано, что он может напрямую нацеливаться на крошечные «электростанции» внутри раковых клеток, замедляя рост опухолей и блокируя их распространение, при этом в значительной степени не затрагивая нормальные клетки.
Электростанции внутри наших клеток
Каждая клетка зависит от митохондрий, часто называемых «электростанциями» клетки, которые генерируют энергетическую молекулу АТФ. В раке митохондрии выполняют не только роль производства топлива — они помогают решать, выживет клетка или погибнет. Один крупный молекулярный комплекс, АТФ‑синтаза, расположен во внутренней мембране митохондрий и синтезирует АТФ. Раковые клетки часто сверхэкспрессируют белок‑партнёр IF1, который прикрепляется к АТФ‑синтазе и действует как предохранительный замок, помогая опухолям сопротивляться процессу, известному как митохондриальный переход проницаемости, и последующей гибели клетки.
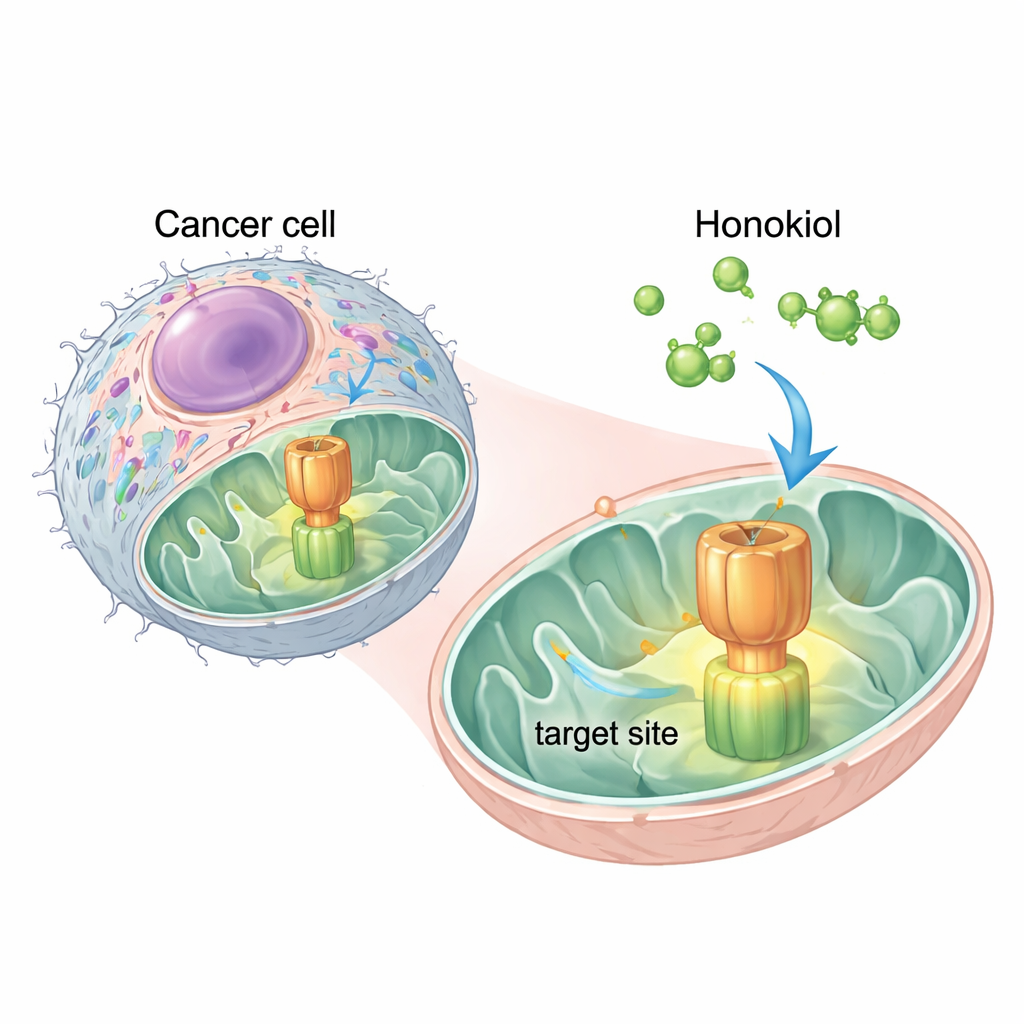
Природная молекула находит критический переключатель
Исследователи использовали компьютерное моделирование, чтобы увидеть, где хонокинол может взаимодействовать с АТФ‑синтазой. Они выявили два перспективных «доковых» участка на одном из её компонентов, области, называемой OSCP. Самый сильный из участков перекрывался с той же площадкой, которой пользуется IF1 для связывания с АТФ‑синтазой. Это наводило на мысль, что хонокинол может действовать как молекулярная клин‑пластина, проникая в OSCP и вытесняя IF1. Эксперименты на человеческих клетках шейки матки HeLa подтвердили эту идею: добавление хонокинола уменьшало физический контакт между IF1 и OSCP, не нарушая другие части фермента, что указывает на специфичность эффекта.
От клеток к живым животным: меньше опухолей, меньше распространения
Чтобы выяснить, оказывает ли это молекулярное вмешательство реальное биологическое влияние, команда имплантировала светящиеся человеческие раковые клетки в эмбрионы маленьких зебровых рыбок — устоявшуюся модель целого организма для отслеживания роста опухолей и метастазирования. У рыбок, получивших обычные HeLa‑клетки с высоким содержанием IF1, лечение хонокинолом значительно уменьшало массу опухолей и сокращало число раковых клеток, распространявшихся в отдалённые области, делая картину похожей на таковую у рыбок, инъецированных IF1‑нокаутными клетками, лишёнными защитного белка. Интересно, что хонокинол также снижал число метастазирующих клеток даже при отсутствии IF1, что указывает на вторичный, независимый от IF1 механизм ограничения распространения рака.
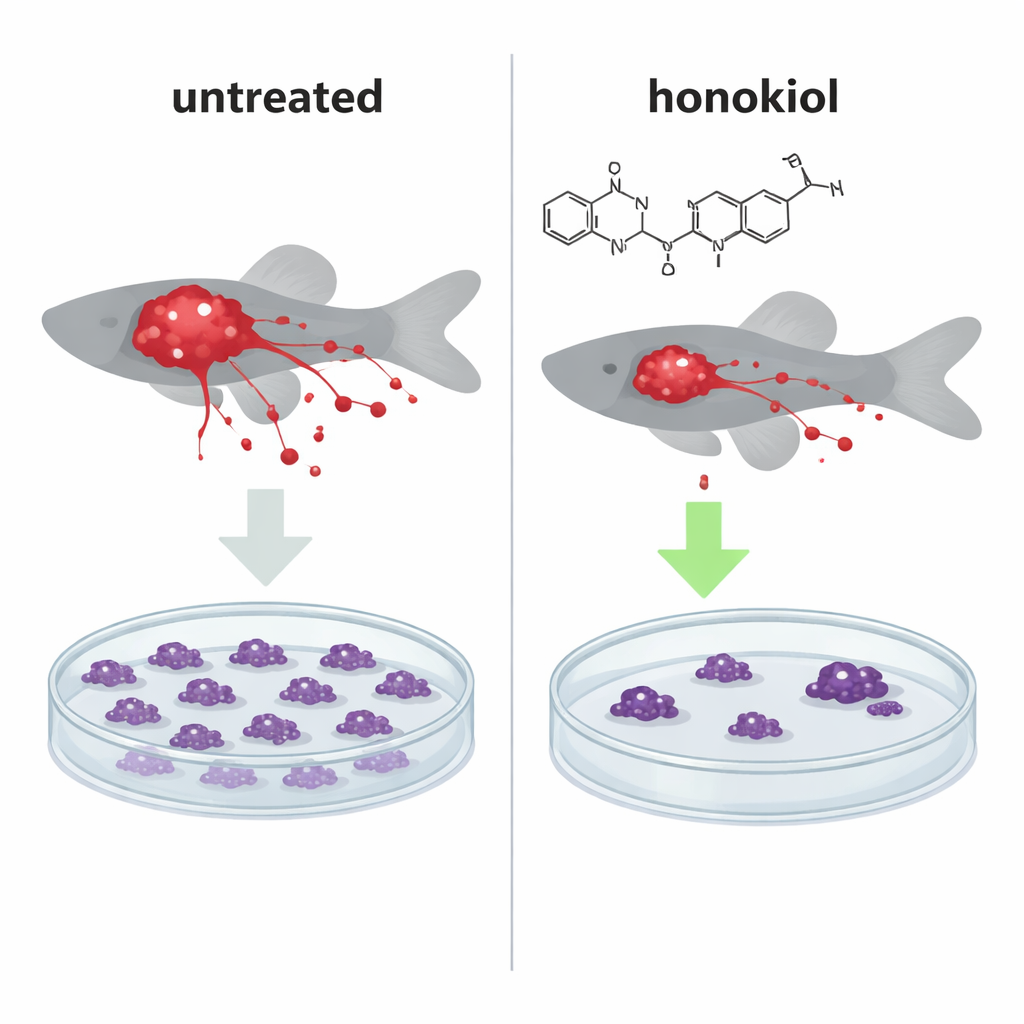
Вынуждая повреждённые «электростанции» запускать самоуничтожение
В культивировании хонокинол снижал способность раковых клеток образовывать крупные колонии в мягком агаре — тесте, имитирующем стрессовые, с низким содержанием кислорода условия внутри солидных опухолей. Это происходило без значительного замедления обычного деления клеток или базального митохондриального дыхания, указывая вместо этого на изменение в том, как митохондрии принимают решение между жизнью и смертью. Измерения обращения с кальцием показали, что хонокинол заставляет митохондрии открывать пору перехода проницаемости при более низких уровнях кальция — известный триггер для отёка и выброса факторов, способствующих смерти. При умеренных дозах этот эффект зависел от вытеснения IF1; при более высоких дозах хонокинол действовал через вторую площадку связывания в OSCP и через увеличение реактивных форм кислорода, делая даже IF1‑дефицитные клетки более чувствительными к программируемой гибели.
Остановка «путешествия» раковых клеток
Рак становится особенно опасным, когда клетки отрываются и мигрируют в новые органы. В «царапающих» тестах на заживление ран хонокинол сильно замедлял коллективную миграцию листов клеток и снижал маркеры эпителиально‑мезенхимального перехода — процесса, который даёт опухолевым клеткам способности к передвижению и инвазии. Детальные изображения электронного микроскопа показали, что мигрирующие клетки обычно увеличивают и перестраивают митохондрии, добавляя внутренние складки, чтобы удовлетворить высокие энергетические потребности на переднем крае. Под действием хонокинола эти «передовые» митохондрии вместо этого становились вздутыми и структурно повреждёнными — признаки открытия поры перехода проницаемости — в то время как митохондрии в немигрирующих областях были менее затронуты или даже увеличивались в числе, в зависимости от присутствия IF1.
Что это значит для будущих противораковых терапий
Проще говоря, работа показывает, что хонокинол может нацеливаться на небольшую регуляторную область митохондриального комплекса по производству АТФ и переключать встроенный предохранитель, который раковые клетки часто держат заблокированным. Вытесняя IF1 и напрямую смещая равновесие в сторону открытия поры, хонокинол побуждает опухолевые клетки к самоуничтожению и затрудняет их миграцию и образование метастазов. Поскольку эти эффекты опираются на характеристики, общие для многих типов рака, а не на единичную поверхностную мишень, нацеливание на область OSCP АТФ‑синтазы может вдохновить создание нового класса терапий, эксплуатирующих уязвимости «электростанций» раковых клеток при минимальном вреде для здоровых тканей.
Цитирование: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Ключевые слова: хонокинол, митохондрии, АТФ‑синтаза, апоптоз, метастазирование