Clear Sky Science · ru
c-Myc/GRPEL1 поддерживает синтез жирных кислот через FASN для поддержки пролиферации клеток ПДАК
Почему «жирные» потребности раковых клеток важны
Рак поджелудочной железы — один из самых смертоносных видов рака, отчасти потому, что его клетки прекрасно умеют перенастраивать собственный метаболизм, чтобы выживать и размножаться. В этом исследовании изучается неожиданная часть этой истории: как клетки опухоли поджелудочной железы усиливают свои внутриклеточные «жировые фабрики», чтобы подпитывать неумолимый рост, и как блокирование этого процесса может открыть новые варианты лечения для пациентов.
Сложная опухоль с метаболическим преимуществом
Большинство опухолей поджелудочной железы относятся к типу аденокарциномы панкреатического протока (ПДАК), который обычно выявляют на поздних стадиях и который плохо отвечает на существующие терапии. Клетки ПДАК живут в суровой среде с недостатком кислорода и ограниченными питательными веществами, но они процветают, перенастраивая использование сахаров, жиров и других топлив. Их митохондрии — крошечные «электростанции» внутри клеток — занимают центральное место в этой перенастройке. Чтобы поддерживать работу этих «станций», клетки постоянно контролируют и восстанавливают тысячи митохондриальных белков — процесс, известный как контроль качества митохондриальных белков. До настоящего времени было неясно, как эта система контроля качества связана с тем, как поджелудочные опухоли обеспечивают себя питательными веществами.
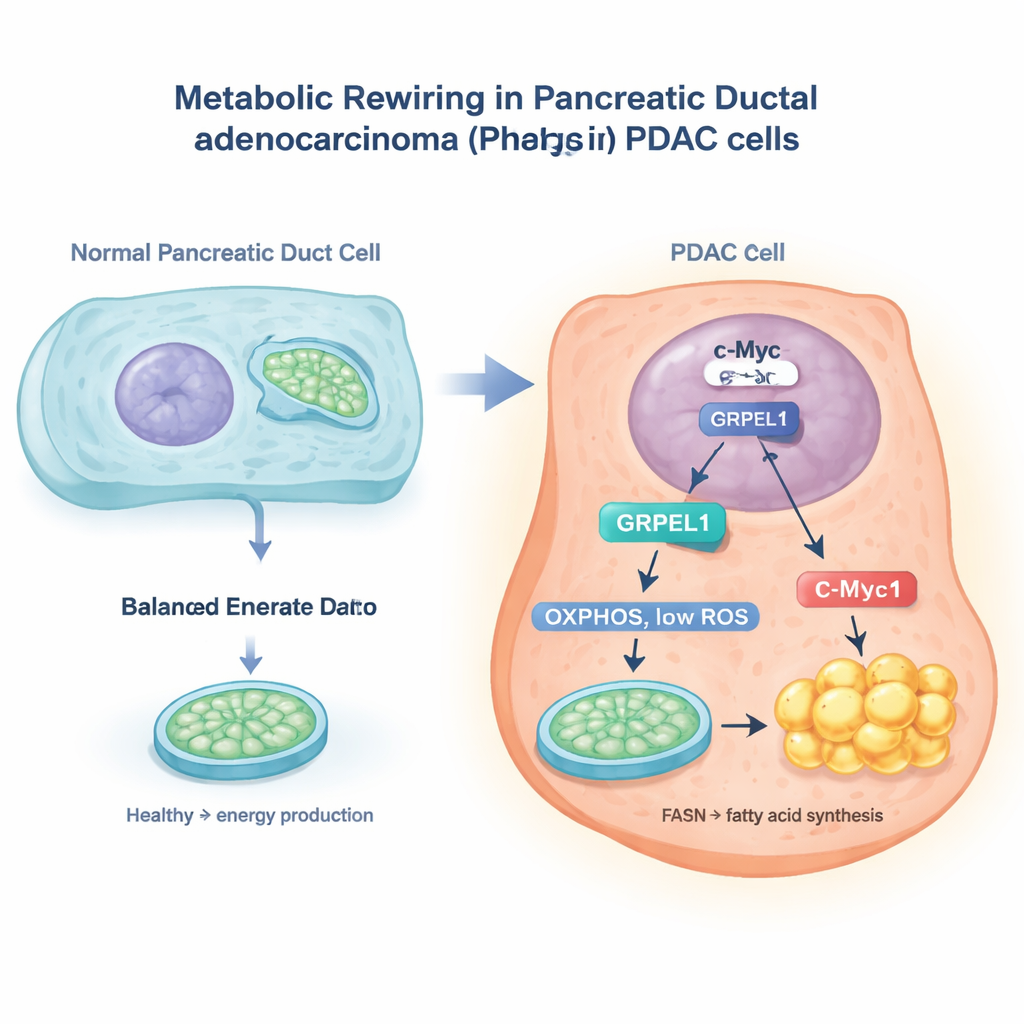
Переключатель c-Myc и митохондриальный помощник
Исследователи использовали крупные онкологические базы данных и эксперименты на клетках рака поджелудочной железы, чтобы сосредоточиться на белке GRPEL1, помощнике, участвующем в обработке митохондриальных белков. Они обнаружили, что известный онкоген c-Myc действует как молекулярный переключатель в ядре клетки, включающий ген GRPEL1. При снижении уровня c-Myc уровень GRPEL1 падал; при усилении c-Myc уровень GRPEL1 повышался. Образцы опухолей пациентов также показали, что c-Myc и GRPEL1 часто повышены одновременно, и оба были связаны с более неблагоприятным прогнозом. В культивируемых линиях ПДАК снижение GRPEL1 замедляло деление клеток и рост колоний, тогда как дополнительный GRPEL1 ускорял пролиферацию клеток, особенно когда c-Myc был заблокирован.
От митохондрий к синтезу жиров
Углубившись, команда выяснила, что GRPEL1 делает больше, чем просто поддерживает порядок с митохондриальными белками. При истощении GRPEL1 митохондрии в клетках ПДАК становились менее эффективными в производстве энергии, теряли нормальную форму и высвобождали больше реактивных форм кислорода (ROS) — химически реактивных побочных продуктов, которые иногда называют клеточной «ржавчиной». Этот всплеск ROS повлиял дальше: снизился уровень синтазы жирных кислот (FASN), ключевого фермента, создающего новые жирные кислоты внутри клетки. При понижении FASN клетки синтезировали меньше жиров, запасали меньше липидов, и их рост замедлялся. Когда исследователи нейтрализовали ROS с помощью антиоксиданта, уровни FASN восстановились, что показало: связь GRPEL1–FASN опосредована ROS. Любопытно, что сам c-Myc в этой системе не выглядел прямым активатором гена FASN, а влиял на FASN косвенно через GRPEL1 и митохондриальный стресс.
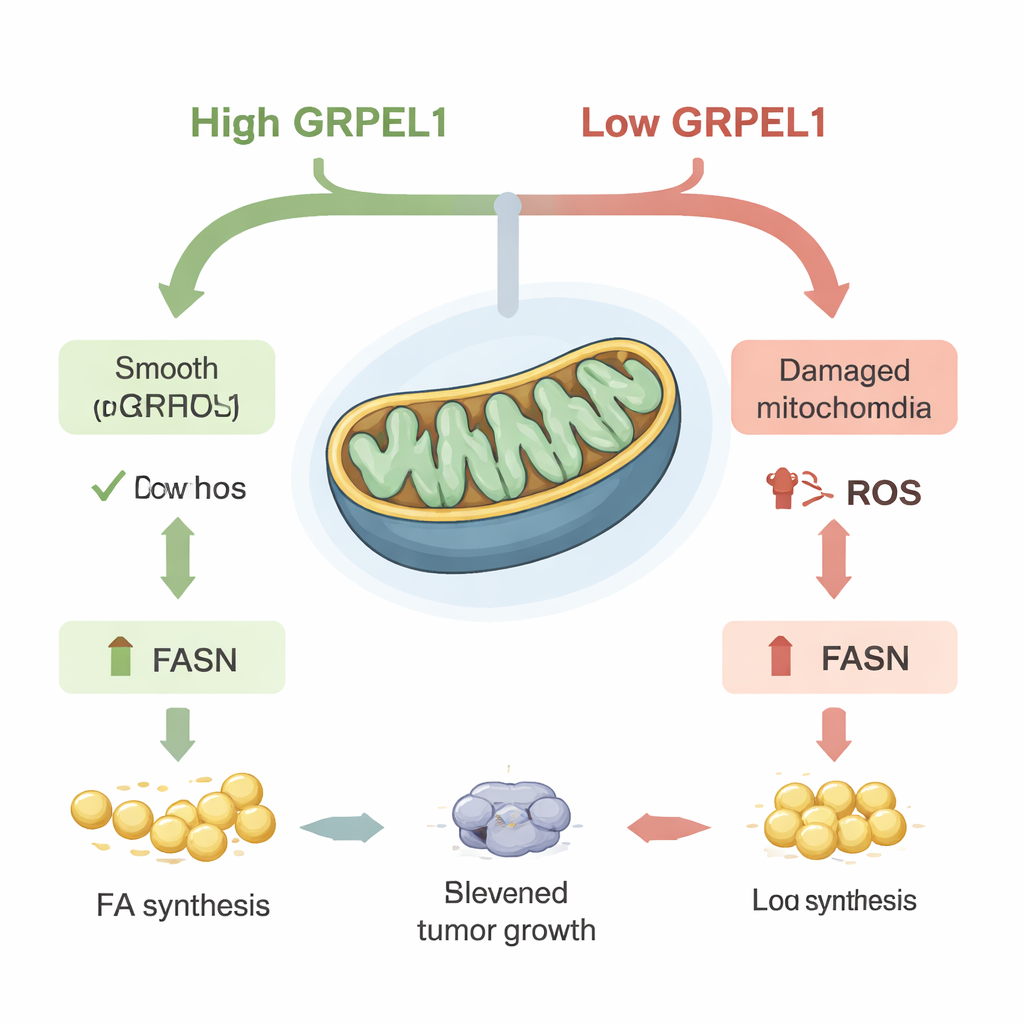
Жиры как топливо для роста опухоли
Поскольку FASN занимает центральное место в биосинтезе жиров, ученые спросили, сможет ли восстановление его уровня вернуть рост опухолевых клеток при низком GRPEL1. В культурах клеток принудительная экспрессия FASN частично компенсировала замедление роста и образования колоний, вызванное потерей GRPEL1. То же наблюдали и у мышей: опухоли, образованные клетками с дефицитом GRPEL1, росли медленнее, но повторное введение FASN восстановило и размер опухоли, и содержание жира. Подробный анализ метаболитов и липидов показал широкие снижения во многих жироподобных молекулах при уменьшении GRPEL1 или c-Myc. Важно, что добавление внешних жирных кислот или липидной смеси частично восстановило рост как в линиях раковых клеток, так и в органоидах поджелудочной железы, полученных от пациентов — мини-опухолях, выращенных в 3D-культивировании, — что указывает на то, что ключевая проблема заключалась в потере вновь синтезируемых жиров.
Преобразование уязвимости в терапию
В сумме работа рисует ясную картину: при раке поджелудочной железы c-Myc повышает уровень GRPEL1, который помогает митохондриям работать бесперебойно и удерживает ROS под контролем. Такая спокойная митохондриальная среда позволяет клеткам сохранять высокие уровни FASN и активно синтезировать новые жирные кислоты, которые служат строительными блоками для мембран, запасов энергии и сигналов роста. При блокировке GRPEL1 митохондрии дают сбой, ROS повышается, FASN снижается, и клетки опухоли испытывают трудности с ростом — эффект, который частично устраняется при поступлении жиров извне. Для общего читателя главная идея такова: опухоли поджелудочной железы зависят от внутренней «жировой фабрики», управляемой c-Myc, GRPEL1 и FASN. Препараты, нарушающие эту ось синтеза жирных кислот, особенно в опухолях с высокой активностью этого пути, могут предложить перспективный способ «истощить» раковые клетки поджелудочной железы, при этом в меньшей степени затрагивая нормальные ткани.
Цитирование: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Ключевые слова: рак поджелудочной железы, метаболизм опухоли, синтез жирных кислот, митохондрии, c-Myc