Clear Sky Science · ru
KDM5B взаимодействует с комплексом CRL4B, способствуя опухолеобразованию при ER+ раке молочной железы через регуляцию метаболизма холестерина
Почему это исследование важно для повседневного здоровья
Рак молочной железы — самое распространённое онкологическое заболевание у женщин, и многие опухоли растут в ответ на гормон эстроген. Эти опухоли делают не только то, что быстро делятся — они также перестраивают способы использования жиров, например холестерина. В работе показано, как белок, регулирующий экспрессию генов, KDM5B, объединяется с другим белковым комплексом CRL4B, чтобы повысить содержание холестерина в клетках рака молочной железы с рецептором эстрогена (ER+). Поняв это скрытое взаимодействие, учёные надеются найти новые способы замедлить рост опухоли и улучшить существующие методы лечения, такие как гормональная терапия и препараты, снижающие холестерин.
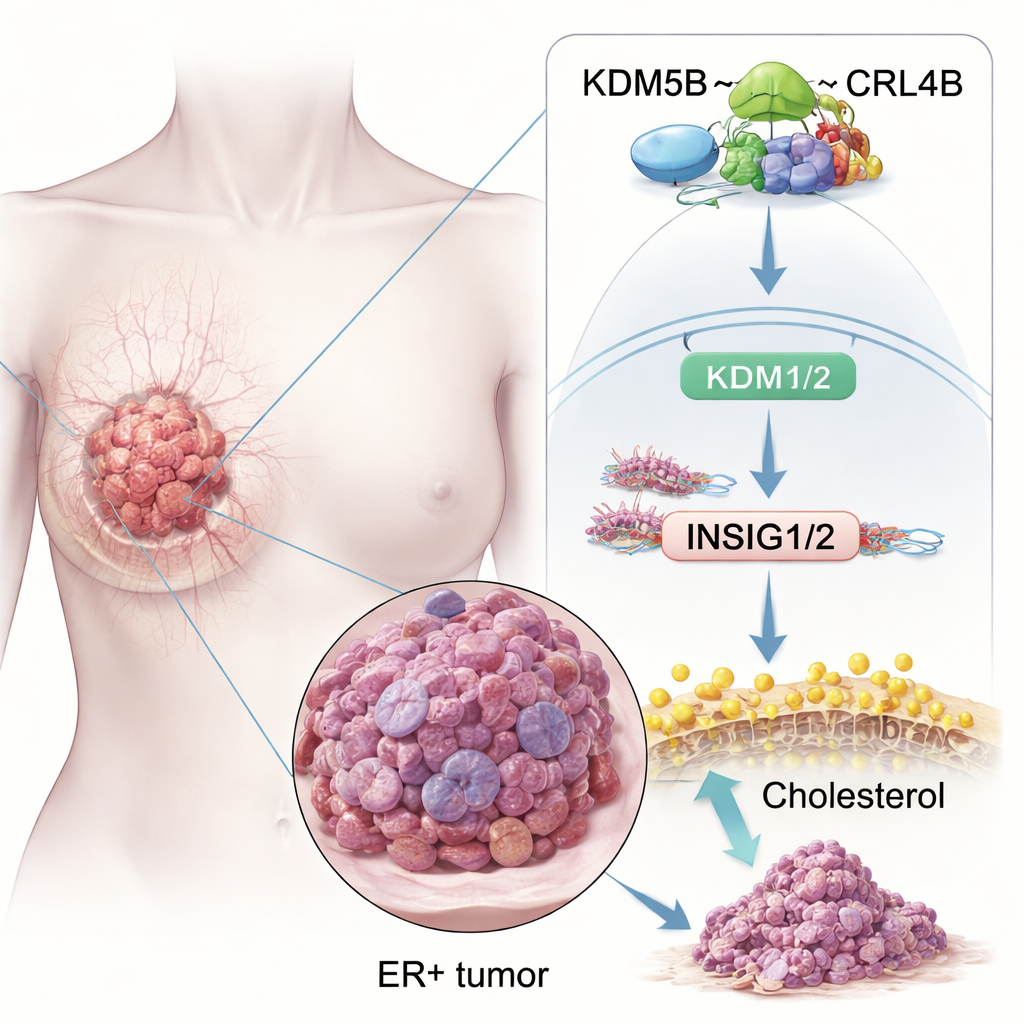
Белок, сдвигающий баланс в сторону рака
Исследователи сначала выяснили, присутствует ли KDM5B в ER+ раках молочной железы просто как маркер или действительно способствует заболеванию. Анализ больших онкологических баз данных и образцов тканей показал, что уровни KDM5B выше в опухолях по сравнению с нормальной тканью молочной железы и особенно высоки в ER+ опухолях. У пациентов с опухолями, экспрессирующими больше KDM5B, прогноз хуже, даже при стандартной химио- или гормональной терапии. В клеточных культурах повышение уровня KDM5B ускоряло рост ER+ раковых клеток, облегчало их инвазивность и способствовало образованию кластеров со стволовыми свойствами, которые, как считают, дают начало новым опухолям. Снижение уровня KDM5B давало противоположный эффект — уменьшение колоний в чашках Петри и размеров опухолей у мышей.
Мощное партнёрство внутри раковых клеток
Чтобы понять, как KDM5B реализует эти эффекты, команда искала его белковые партнёры. Они обнаружили, что KDM5B физически связывается с компонентами молекулярного комплекса CRL4B — ферментной системы, которая помечает белки и влияет на упаковку ДНК. Детальные биохимические тесты показали, что KDM5B напрямую взаимодействует с двумя компонентами CRL4B, CUL4B и DDB1, через определённые участки каждого белка. В клетках ER+ рака молочной железы комплекс KDM5B–CRL4B действует на многие гены на их «включателях». Геномное картирование показало, что KDM5B и CUL4B часто локализуются вместе в промоторах генов, где они изменяют химические метки на гистонах — катушках, вокруг которых намотана ДНК — и подавляют экспрессию этих генов.
Снятие тормозов с синтеза холестерина
Из множества затронутых путей особенно выделился метаболизм холестерина. Раковым клеткам требуется дополнительный холестерин для построения мембран и выживания при стрессах, а ER+ опухоли также используют производные холестерина, чтобы имитировать действие эстрогена. Исследование показывает, что комплекс KDM5B–CRL4B напрямую связывается с регуляторными участками двух ключевых «тормозных» генов — INSIG1 и INSIG2. Эти гены обычно сдерживают мастер‑регулятор синтеза холестерина, SREBP2. KDM5B–CRL4B добавляет репрессивную метку (H2AK119ub1) и удаляет активирующую метку (H3K4me3) на гистонах в промоторах INSIG1/2, подавляя их экспрессию. При уменьшении уровня белков INSIG1/2 SREBP2 высвобождается и включает гены синтеза холестерина, что повышает уровень холестерина в ER+ раковых клетках и усиливает их инвазивность. При нарушении работы KDM5B или CRL4B уровень INSIG1/2 повышается, активность SREBP2 падает, и общий холестерин в клетках снижается.
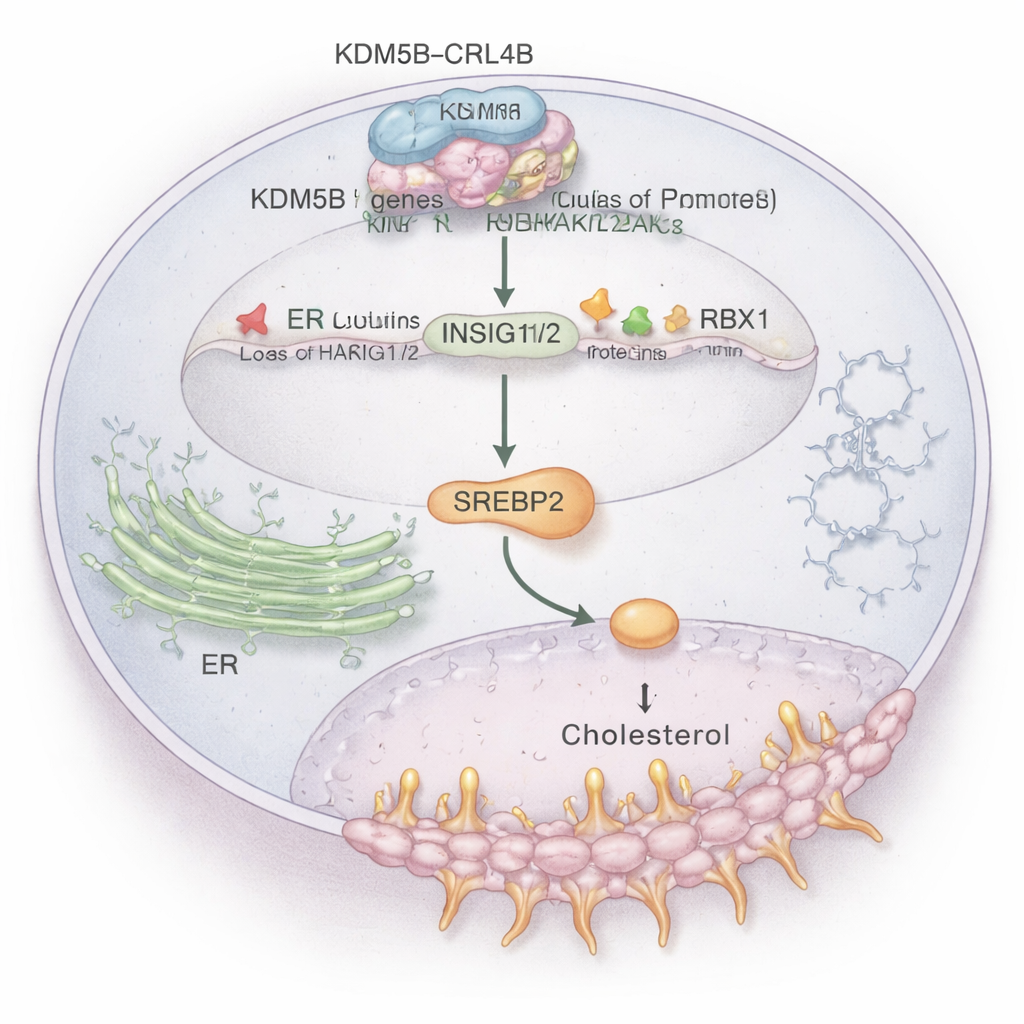
Пересечение сигналов холестерина и онкогенных путей
Работа также связывает этот путь с производным холестерина 27‑гидроксихолестерином (27‑HC), молекулой, уже известной как фактор, способствующий ER+ раку молочной железы. Обработка ER+ клеток 27‑HC повышала уровни KDM5B и ещё сильнее подавляла INSIG1/2, подталкивая клетки к росту и инвазии. Важно, что блокирование KDM5B или CRL4B ослабляло эти агрессивные эффекты, что указывает на то, что 27‑HC частично действует через ось KDM5B–CRL4B. Отдельно авторы показали, что симвастатин, широко применяемый статин для снижения холестерина, замедляет рост раковых клеток молочной железы, а в сочетании с ингибитором KDM5B антиопухолевый эффект усиливался. Это говорит о перспективе комбинирования препаратов, нацеленных на синтез холестерина, с лекарствами, влияющими на эпигенетическую регуляцию через KDM5B.
Что это означает для пациентов и будущих лечений
Исследование выявляет новую цепочку событий в ER+ раковых клетках молочной железы: сигнал, связанный с холестерином (27‑HC), повышает KDM5B; KDM5B объединяется с комплексом CRL4B и выключает INSIG1 и INSIG2; это освобождает SREBP2, усиливает синтез холестерина и помогает опухолям расти, проникать в ткани и поддерживать стволоподобные клетки. Поскольку KDM5B также повышен и связан с плохим прогнозом при нескольких других видах рака, блокирование этого белка — или восстановление работы «тормозов» INSIG1/2 — может дать новые способы контроля роста опухоли. Хотя требуется дополнительная работа до клинического применения, результаты подчёркивают, насколько поведение рака связано с обычными молекулами, такими как холестерин, и как существующие препараты, например статиновые лекарства, потенциально можно сочетать с эпигенетическими терапиями для улучшения исходов.
Цитирование: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Ключевые слова: рак молочной железы с рецептором эстрогена, метаболизм холестерина, KDM5B, INSIG1/INSIG2, эпигенетическая терапия