Clear Sky Science · ru
Сигналы TGFβ стимулируют прогрессирование клеточного цикла и устойчивость к ингибитору CDK4/6 пальбоциклибу через транскрипционную модуляцию SOX4 в клетках рака молочной железы
Когда раковые клетки захватывают полезный сигнал
Наш организм полагается на многочисленные химические сигналы, которые поддерживают деление клеток при необходимости и останавливают его в нужный момент. Один из таких сигналов, называемый трансформирующим фактором роста бета (TGFβ), обычно помогает предотвращать опухоли. В этом исследовании показано, как в некоторых формах рака молочной железы тот же сигнал TGFβ может быть искажен в пользу роста опухолевых клеток и их устойчивости к важному препарату — пальбоциклибу. Понимание этого переключения может помочь в подборе более эффективных комбинаций лекарств для пациентов, чьи опухоли перестают отвечать на терапию.
От тормоза роста к двусмысленному сигналу
В здоровой ткани TGFβ обычно действует как тормоз: он замедляет деление клеток и ограничивает воспаление, помогая предотвратить раннее образование опухолей. Но в сформировавшихся опухолях, особенно в опухолях молочной железы, которые уже приобрели онкогенные мутации, TGFβ может вести себя иначе — стимулировать миграцию, инвазию и метастазирование клеток. Чтобы изучить это двойное поведение, исследователи использовали 3D «мини-опухоли», выращенные из человеческих молочных клеток. Они сравнили клетки, похожие на нормальные, с идентичными клетками, несущими онкогенную мутацию HRAS, которая подталкивает их в сторону рака. Такая контролируемая модель позволила им выяснить, как тот же сигнал TGFβ реализуется в предраковой и в ракоподобной среде. 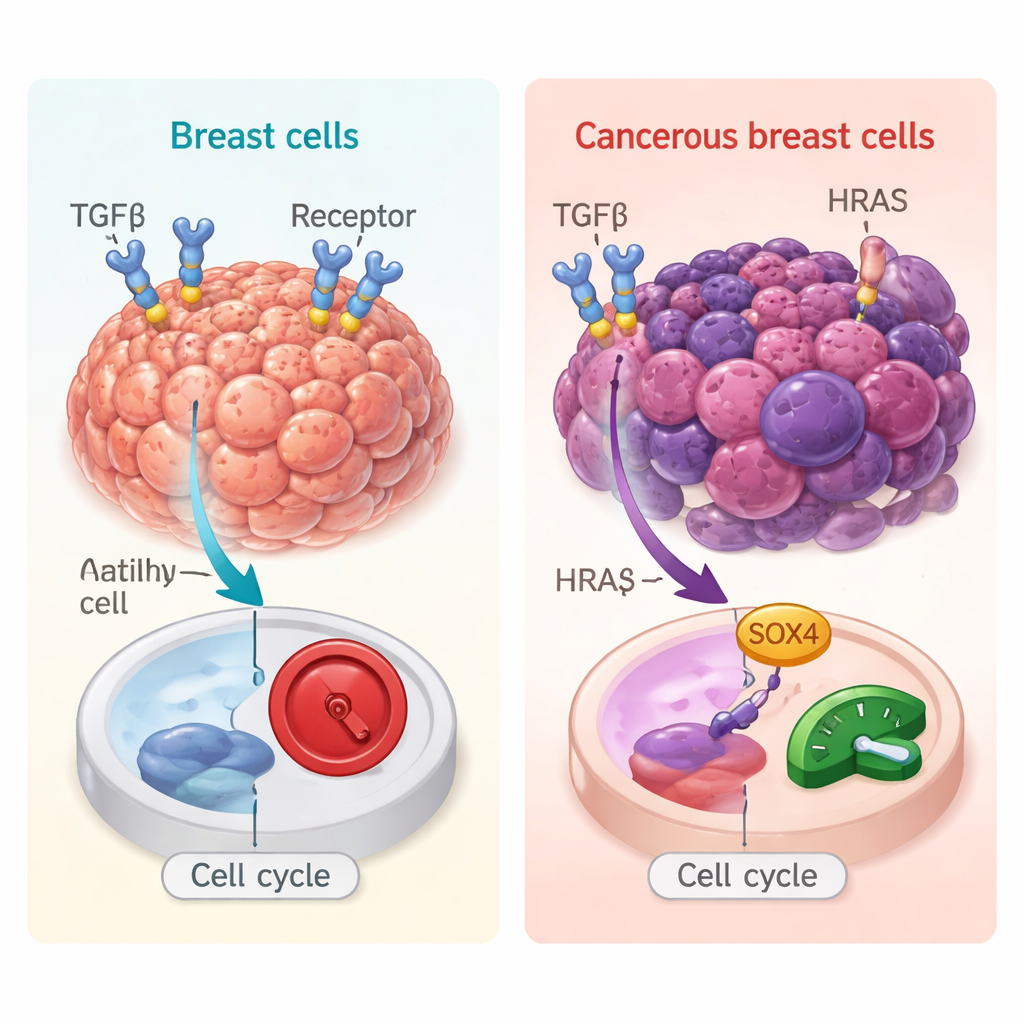
Перепрограммирование геномных переключателей вкл/выкл
Команда изучала хроматин — упаковку ДНК с белками, которая контролирует, какие гены доступны и могут быть включены. После обработки 3D-кластеров клеток TGFβ они обнаружили широкое открытие хроматина у стартовых участков генов и в отдалённых энхансерных регионах как в нормоподобных, так и в HRAS-мутационных клетках. Однако шаблон вновь доступных участков заметно различался между ними. В клетках, похожих на раковые, особенно обогащёнными оказались сайты связывания транскрипционного фактора SOX4. Параллельно анализ экспрессии генов показал, что TGFβ перестаёт лишь включать известные программы, такие как эпителиально-мезенхимальный переход (связанный с инвазией) и метаболические сдвиги; в HRAS-мутационных клетках он также усиливал гены, вовлечённые в репликацию ДНК, репарацию ДНК и прогрессирование через ключевые контрольные точки клеточного цикла.
SOX4 как молекулярный посредник
Углублённый анализ показал, что SOX4 находится в центре этого переключения. Данные одиночноклеточной РНК-секвенирования первичных опухолей молочной железы выявили, что SOX4 ко-экспрессируется с драйверами клеточного цикла, такими как CDK4, CDK6 и циклин D1 (CCND1), особенно в активно делящихся раковых клетках. В их 3D-моделях TGFβ увеличивал уровни SOX4, и SOX4 находили связанным рядом с регуляторными областями этих генов клеточного цикла, в особенности CDK4. При снижении уровня SOX4 с помощью генетических инструментов TGFβ уже не мог эффективно включать многие из своих целевых генов, в том числе связанные с делением клеток и ремоделированием ткани, а ракоподобные сферы становились менее инвазивными и более стабильными. Биохимические эксперименты дополнительно продемонстрировали, что SOX4 сотрудничает с SMAD3, ключевым переносчиком сигнала TGFβ, формируя в ядре кооперативный модуль, усиливающий активацию генов.
Подрыв передовой терапии при раке молочной железы
Пальбоциклиб — широко используемый препарат, блокирующий CDK4 и CDK6, белки, которые переводят клетки из состояния покоя в активное деление. У многих пациентов со временем развивается устойчивость к этому лечению. Авторы сопоставили крупные наборы данных об ответе на лекарства с лабораторными экспериментами в нескольких линиях клеток рака молочной железы и 3D-культурах. Они обнаружили, что усиленная активность TGFβ вместе с сигнатурами SOX4 и родственных генов ассоциируется с более высокими дозами пальбоциклиба, необходимыми для подавления роста. В лаборатории добавление TGFβ делало раковые клетки менее чувствительными к пальбоциклибу, тогда как блокирование сигнальной передачи TGFβ или подавление SOX4 восстанавливало чувствительность. Длительное воздействие пальбоциклиба приводило к получению устойчивых линий клеток, в которых наблюдались усиленная сигнализация TGFβ, больше SOX4 и более выраженные признаки активного хроматина у самого гена SOX4. В моделях на цыплячках-зебрафиш ингибирование TGFβ существенно уменьшало рост опухолей, полученных из клеток, устойчивых к пальбоциклибу. 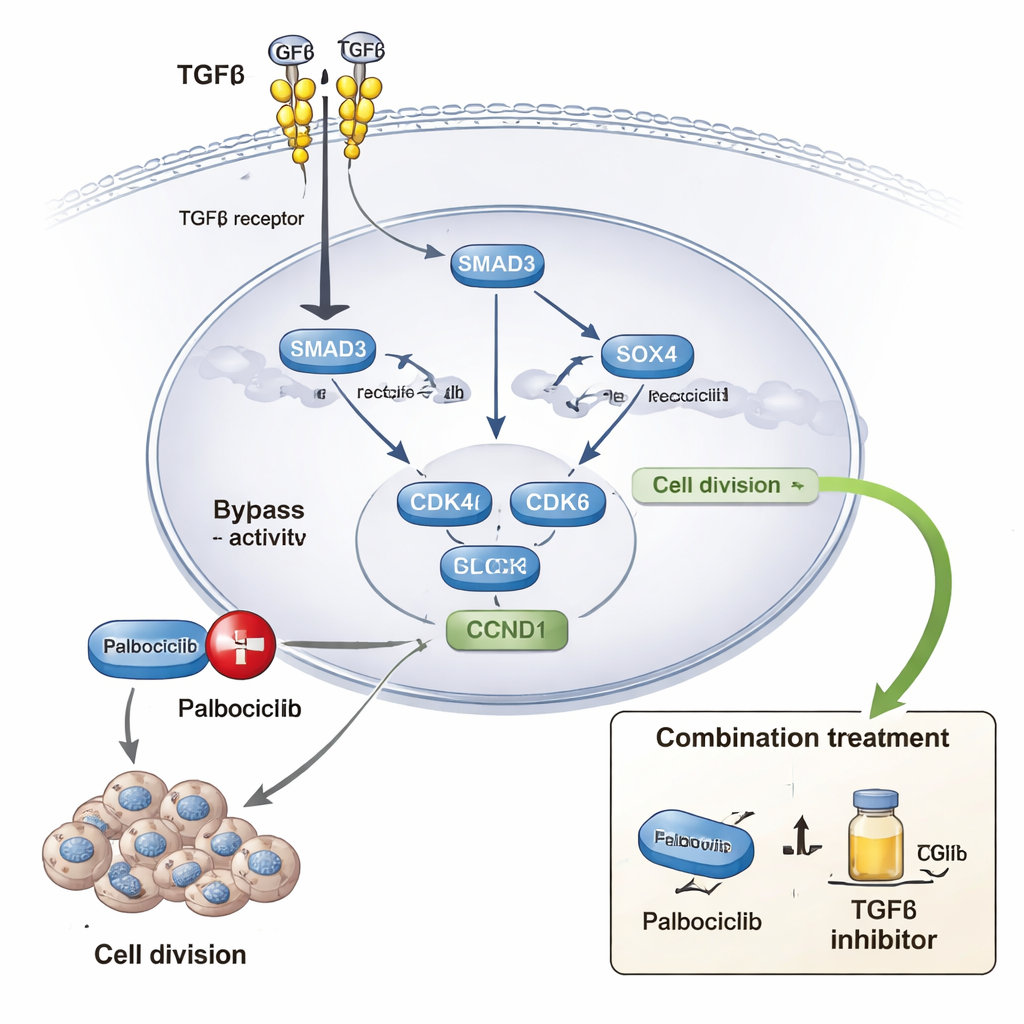
Что это значит для пациентов и будущих терапий
Для неспециалиста главное послание таково: сигнал, призванный защищать нас от рака, в неправильном контексте может быть захвачен и помочь опухолям выживать и обмануть лекарства. В этом исследовании TGFβ объединяется с SOX4, чтобы открывать важные участки генома, включать «двигатели» клеточного цикла, такие как CDK4 и CDK6, и ослаблять эффект пальбоциклиба. Результаты указывают, что для некоторых случаев рака молочной железы комбинирование ингибиторов CDK4/6 с препаратами, блокирующими сигнализацию TGFβ — или с подходами, нацеленными на программы, управляемые SOX4 — может отсрочить или преодолеть устойчивость. Хотя требуется больше клинических исследований, это исследование картирует подробный молекулярный путь ухода опухоли и указывает на новые способы его прервать.
Цитирование: Ali, M.M., Itoh, Y., Badji, A.M.P. et al. TGFβ signaling promotes cell cycle progression and resistance to the CDK4/6 inhibitor palbociclib through SOX4 transcriptional modulation in breast cancer cells. Cell Death Dis 17, 209 (2026). https://doi.org/10.1038/s41419-026-08435-4
Ключевые слова: рак молочной железы, сигнализация TGF-бета, SOX4, устойчивость к пальбоциклибу, клеточный цикл