Clear Sky Science · ru
BCL-xL как терапевтическая мишень при колоректальном раке, резистентном к цетуксимабу
Почему это важно для людей с раком толстой кишки
Колоректальный (толстокишечный и прямокишечный) рак — одно из самых распространённых онкологических заболеваний в мире; многие пациенты с распространённым течением получают таргетный антительный препарат цетуксимаб. Этот препарат сначала может уменьшать опухоли, но у большинства пациентов в течение нескольких месяцев опухоль находит пути уйти от действия препарата, и у врачей остаётся мало эффективных вариантов. В этом исследовании поставлен актуальный вопрос: когда опухоли толстой кишки перестают реагировать на цетуксимаб, есть ли другая уязвимость, которую могли бы использовать новые лекарства, чтобы заставить раковые клетки погибнуть?
Когда таргетный препарат перестаёт работать
Цетуксимаб блокирует на поверхности раковых клеток «антенну» — эпидермальный фактор роста (EGFR), который стимулирует их рост. Команда создала лабораторную модель резистентности, подвергая чувствительную линию колоректальных раковых клеток (LIM1215) постепенному повышению доз цетуксимаба в течение шести месяцев. Возникли две независимо выведенные резистентные популяции клеток, которые продолжали расти даже при высоких концентрациях препарата, при этом после отмены лекарства они выглядели так же здоровыми и быстрорастущими, как исходные клетки. Важно, что у резистентных клеток на поверхности по-прежнему присутствовала мишень препарата и к ней по-прежнему мог присоединяться цетуксимаб, что указывает на то, что рак не просто «скрыл» или существенно не изменил рецептор.
Резистентные клетки перенаправляют сигналы роста
Чтобы понять, как клетки обходили действие цетуксимаба, исследователи изучили ключевые внутриклеточные пути роста. У исходных клеток цетуксимаб обычно подавлял путь MAPK, главный двигатель деления клеток. У резистентных клеток активность MAPK оставалась высокой даже при блокировании EGFR, что свидетельствует о разъединении сигнала роста от первоначального рецептора. Секвенирование РНК выявило новые активирующие мутации в другом гене RAS — HRAS — в субпопуляциях резистентных клеток, но не в обычных «подозреваемых» KRAS, NRAS или BRAF. Попытки подавить это перенаправленное сигналирование с помощью ингибитора MEK (действующего ниже по ходу RAS) лишь умеренно снизили рост. Это показало, что вместо того, чтобы гоняться за каждой новой мутацией, может быть эффективнее атаковать общие механизмы жизни и смерти клетки, разделяемые разными резистентными клонами. 
Атака на систему жизнеобеспечения рака
Учёные переключили внимание на апоптоз — встроенную программу самоуничтожения клеток, которую раки часто подавляют. Анализ экспрессии генов показал изменения в путях, связанных с апоптозом, в резистентных клетках. В частности, антиапоптотический белок BCL-xL был повышен в одной резистентной популяции и умеренно увеличен в другой, при этом присутствовал и другой белок выживания, MCL-1. Команда испытала малые молекулы — BH3-микитики, разработанные для блокирования этих белков выживания и освобождения механизма смерти. В двумерных культурах все три линии клеток — исходная и резистентные — были чувствительны к препаратам, блокирующим BCL-xL или MCL-1, но что примечательно, более низкие дозы убивали цетуксимаб-резистентные клетки эффективнее. Добавление низкой дозы ингибитора протеасомы бортезомиба, который способствует накоплению про-смертных сигналов, дополнительно усиливало гибель, особенно в сочетании с блокатором MCL-1.
От плоских пластинок к 3D миниопухолям и тканям пациентов
Поскольку плоские слои клеток не полностью имитируют опухоли в организме, команда затем выращивала клетки в виде трёхмерных сфероидов, внедрённых в гель, что лучше отражает архитектуру и проблемы проникновения препарата в настоящие опухоли. И здесь блокирование BCL-xL или MCL-1 снижало жизнеспособность сфероидов, а комбинация этих препаратов с бортезомибом вызывала драматическое падение метаболической активности и явные признаки гибели клеток. Чтобы проверить, присутствует ли эта уязвимость в более реалистичном человеческом опухолевом материале, использовали тонкие срезы опухолей колоректального рака, резистентных к цетуксимабу, выращенные в мышах из опухолей пациентов (patient-derived xenografts). Эти модели были все KRAS дикого типа, как исходные клетки LIM1215, но несли разнообразные дополнительные мутации, включая BRAF и TP53, отражая генетическое разнообразие, наблюдаемое в клинике. 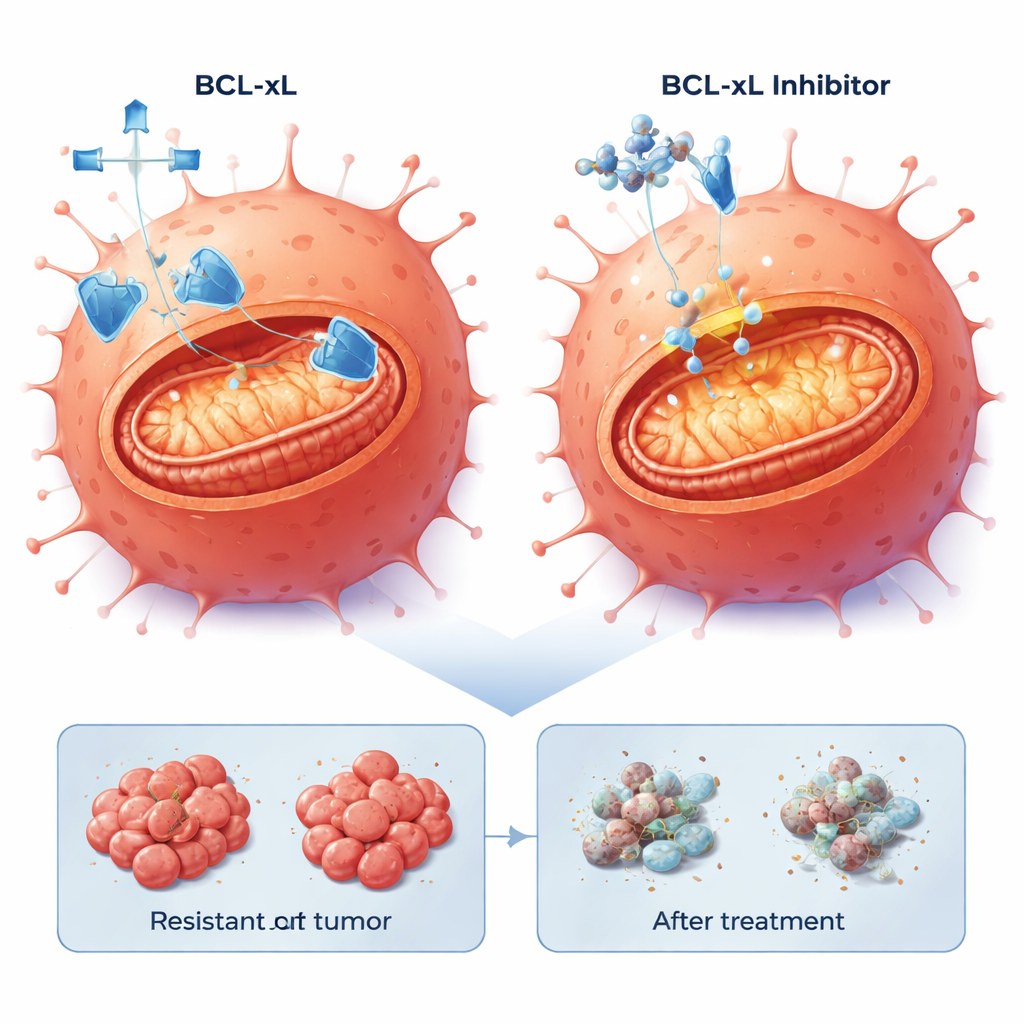
Таргетирование BCL-xL эффективно в различных резистентных опухолях
В срезах опухолей, полученных от пациентов, комбинация ингибитора BCL-xL с низкой дозой бортезомиба последовательно вызывала выраженную гибель клеток в 20–40% опухолевых клеток в четырёх разных моделях, включая опухоли с агрессивными мутациями BRAF. В свою очередь блокирование MCL-1 с бортезомибом давало сильный эффект лишь в части опухолей. Важно, что способность резистентных клеток проходить апоптоз сохранилась: когда удалялся «страховочный» BCL-xL, внутренняя программа смерти по-прежнему могла активироваться, независимо от того, каким конкретным генетическим путём опухоль ушла от действия цетуксимаба.
Что это значит для пациентов
Для людей, у которых колоректальный рак перестаёт реагировать на цетуксимаб, это исследование даёт осторожный оптимизм. Оно указывает на то, что даже после развития резистентности к терапии против EGFR многие раковые клетки остаются подготовленными к смерти, если заблокировать ключевой белок выживания BCL-xL. Хотя ингибиторы BCL-xL могут вызывать побочные эффекты, особенно в отношении тромбоцитов крови, работа указывает на стратегии комбинаций и оптимизации доз, которые могут ограничить токсичность и при этом использовать общую ахиллесову пяту трудноизлечимых опухолей. В будущем препараты, нейтрализующие BCL-xL, могут составить основу новых терапий второй линии для колоректального рака, резистентного к цетуксимабу, менее зависящих от постоянно меняющегося мутационного ландшафта опухоли.
Цитирование: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Ключевые слова: колоректальный рак, лекарственная резистентность, цетуксимаб, ингибиция BCL-xL, апоптоз