Clear Sky Science · ru
LAP2α стимулирует развитие рака молочной железы, снижая стресс репликации
Почему это важно для рака молочной железы
Опухоли молочной железы развиваются отчасти потому, что раковые клетки находят способы выживать при постоянном стрессе во время копирования ДНК. В этом исследовании показано, как относительно малоизвестный белок LAP2α помогает раковым клеткам защищать ДНК в процессе репликации, тем самым способствуя росту опухоли и усложняя лечение. Понимание этой скрытой «системы поддержки» открывает новые пути для ослабления опухолей и повышения эффективности существующих препаратов.
Скрытый помощник внутри ядер опухолевых клеток
Каждый раз при делении клетке необходимо точно скопировать свою ДНК. В раковых клетках этот процесс особенно напряжён: сигналы роста постоянно активированы, и репликационный аппарат работает на пределе. Это давление, известное как стресс репликации, оставляет участки одноцепочечной ДНК, которые необходимо быстро покрыть и стабилизировать белковым комплексом RPA. Ранее авторы показали, что LAP2α — белок, связанный с внутренним каркасом ядра — может связываться с RPA и помогать ему добираться до повреждённой ДНК. В текущей работе они проверили, действительно ли партнёрство LAP2α–RPA стимулирует развитие рака молочной железы и влияет на ответ опухолей на лечение.
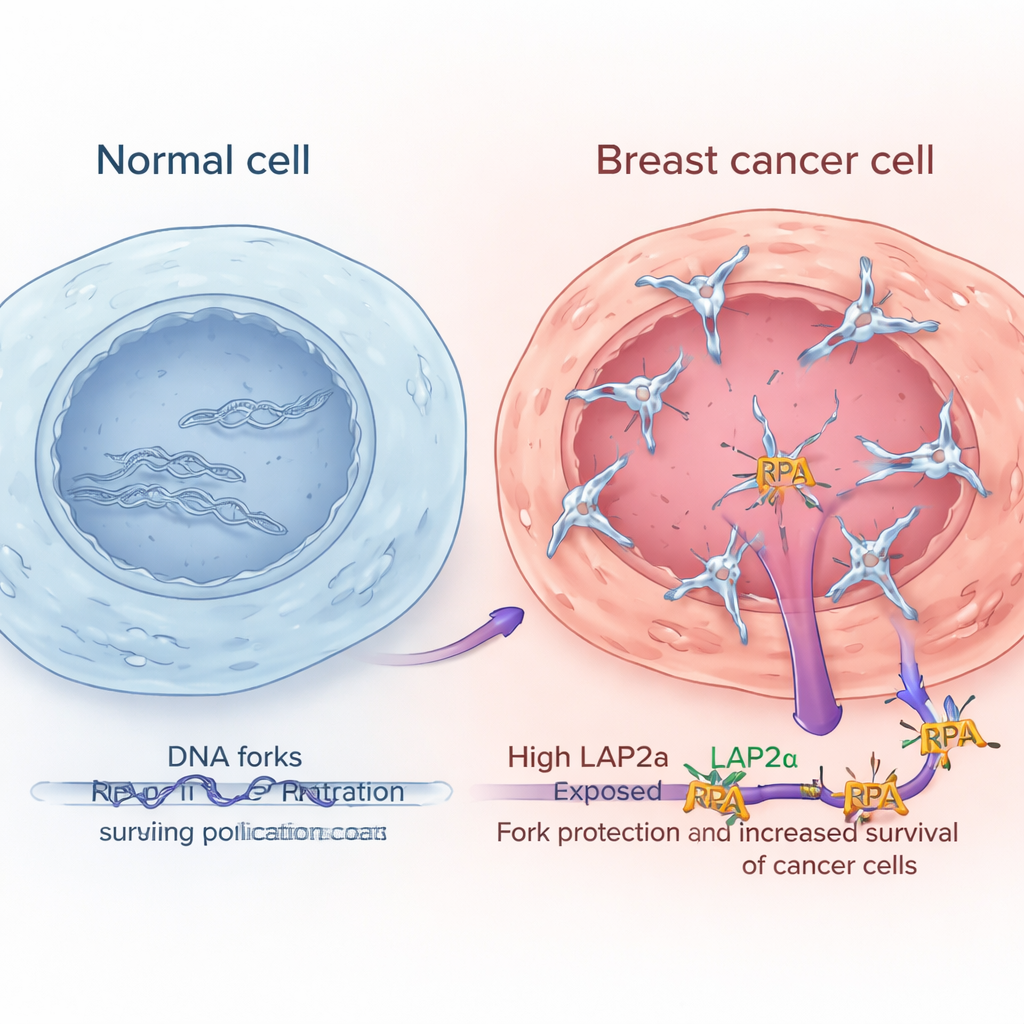
Высокий уровень LAP2α характерен для более агрессивных опухолей молочной железы
Анализ крупных общедоступных наборов экспрессии генов и микроскопическое исследование образцов опухолей показали, что LAP2α постоянно выше в тканях рака молочной железы по сравнению с прилегающей нормальной тканью. Его уровень повышается с увеличением градации опухоли: более атипичные и агрессивные опухоли обычно содержат больше LAP2α. Эта картина наблюдалась в нескольких основных подтипах рака молочной железы, включая гормонально-позитивные, обогащённые HER2 и тройной негативный. Существенно, что у пациентов с опухолями с высоким уровнем LAP2α прогноз был хуже. В то же время сами ключевые компоненты комплекса RPA не демонстрировали подобных изменений или явных связей с исходом, что указывает на то, что именно усиленная функция LAP2α, а не просто избыток RPA, помогает раковым клеткам справляться со стрессом репликации.
Отключение LAP2α замедляет опухоли и выявляет уязвимости
Чтобы выйти за рамки корреляций, исследователи использовали мышиные модели рака молочной железы, в которых LAP2α можно было выборочно удалить. После формирования опухолей генетическое удаление LAP2α приводило к более медленному росту опухолей и увеличению продолжительности жизни животных. Клетки опухолей без LAP2α реже делились и имели больше признаков повреждений ДНК, что проявлялось повышенной окраской маркеров разрывов ДНК и снижением покрытия ДНК белком RPA. Когда такие LAP2α-дефицитные опухолевые клетки пересаживали в новых мышей, они вновь формировали меньшие опухоли и были более чувствительны к ДНК-повреждающей химиотерапии, включая платиновый препарат цисплатин и ингибитор PARP. Аналогичные эксперименты на линиях человеческих клеток рака молочной железы подтвердили, что снижение LAP2α делает клетки более уязвимыми к нескольким генотоксическим препаратам, тогда как восстановление нормального LAP2α — но не мутантной формы, неспособной связываться с RPA — возвращало защиту ДНК и устойчивость к лекарствам.
Как LAP2α помогает защищать хрупкие участки ДНК
Для выяснения механизма исследователи воссоздали этапы связывания ДНК в пробирочных экспериментах. Они смешивали очищенный RPA, одноцепочечную ДНК и либо нормальный LAP2α, либо вариант, неспособный взаимодействовать с RPA. Оказалось, что LAP2α напрямую повышает эффективность покрытия одноцепочечной ДНК RPA и помогает RPA растягивать и стабилизировать эти уязвимые участки, действуя как «загрузчик» или шаперон. При наличии ДНК RPA, как правило, покидал LAP2α и полностью переходил к связыванию с одноцепочкой, что показывает: LAP2α не входит в окончательное защитное покрытие, а передаёт RPA ДНК. При отсутствии функционального взаимодействия LAP2α–RPA больше репликационных вилок рушилось, накапливались разрывы ДНК, и раковые клетки чаще погибали, особенно при дополнительном повреждении, вызванном химиотерапией.
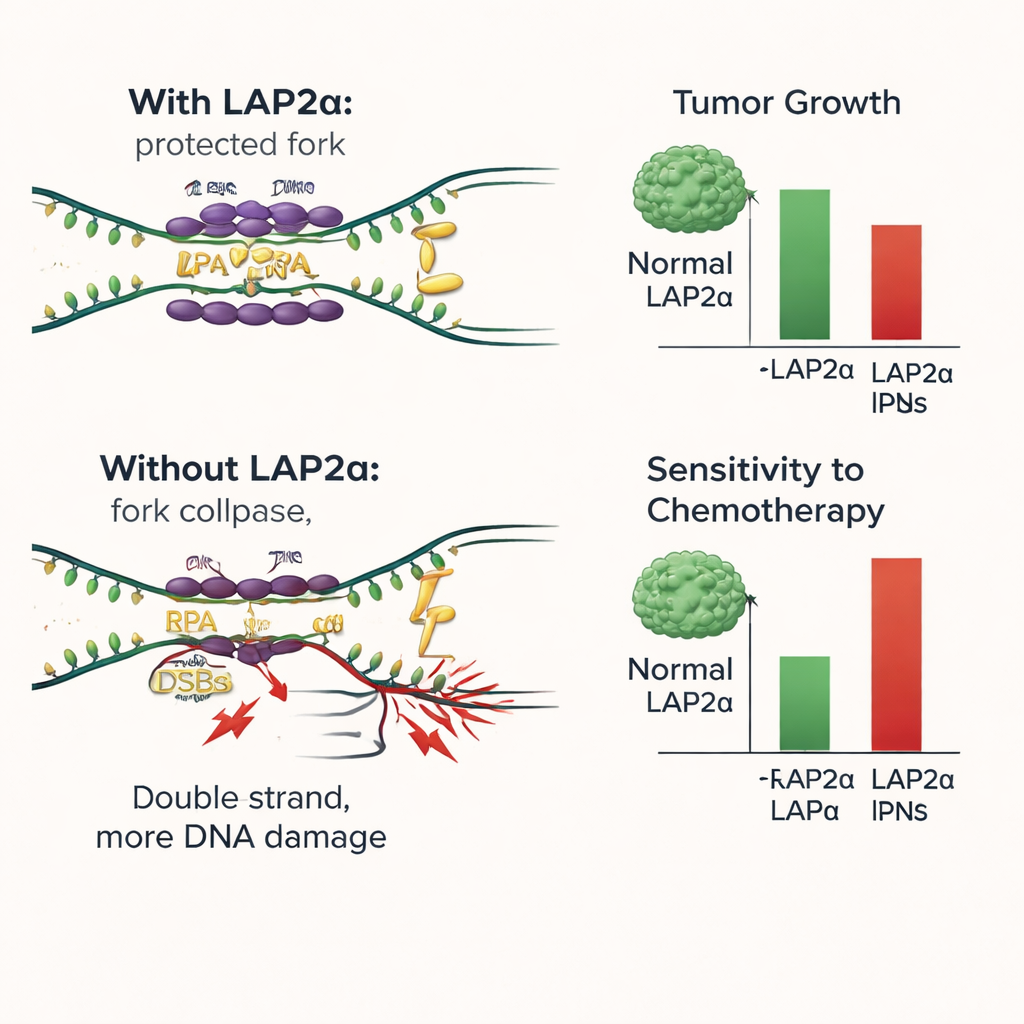
Что это значит для будущего лечения рака молочной железы
Проще говоря, это исследование показывает, что LAP2α выполняет роль «закулисного помощника», который помогает раковым клеткам молочной железы выдерживать напряжение, связанное с копированием ДНК. Эффективно загружая RPA на уязвимые участки ДНК, LAP2α уменьшает повреждения и поддерживает продолжающийся рост опухоли. Удаление или блокирование LAP2α меняет расстановку сил: повреждения ДНК накапливаются, клетки прекращают делиться, а стандартные препараты, атакующие ДНК, становятся более эффективными. Эти результаты указывают на то, что LAP2α может служить маркером неблагоприятного прогноза и новым терапевтическим мишенью. Препараты, блокирующие LAP2α или его связывание с RPA, могли бы улучшить работу существующих схем лечения, таких как платиновые средства и ингибиторы PARP, особенно в опухолях, которые сильно зависят от этой системы сглаживания стресса.
Цитирование: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Ключевые слова: рак молочной железы, стресс репликации ДНК, LAP2 alpha, репликационный белок A, чувствительность к химиотерапии