Clear Sky Science · ru
Таргетирование биосинтеза глицерофосфолипидов преодолевает химиорезистентность, вызванную потерей SLFN11 при саркоме Юинга
Почему это исследование важно для детского рака
Саркома Юинга — редкая, но агрессивная опухоль, которая преимущественно поражает детей и подростков. Многие пациенты изначально хорошо отвечают на химиотерапию, но у тех, у кого заболевание возвращается, текущие методы лечения часто оказываются неэффективными. В этой работе поставлен важный вопрос: какие внутриклеточные изменения позволяют клеткам саркомы Юинга переживать химиотерапию и можно ли эти изменения превратить в новые уязвимые места для лечения?
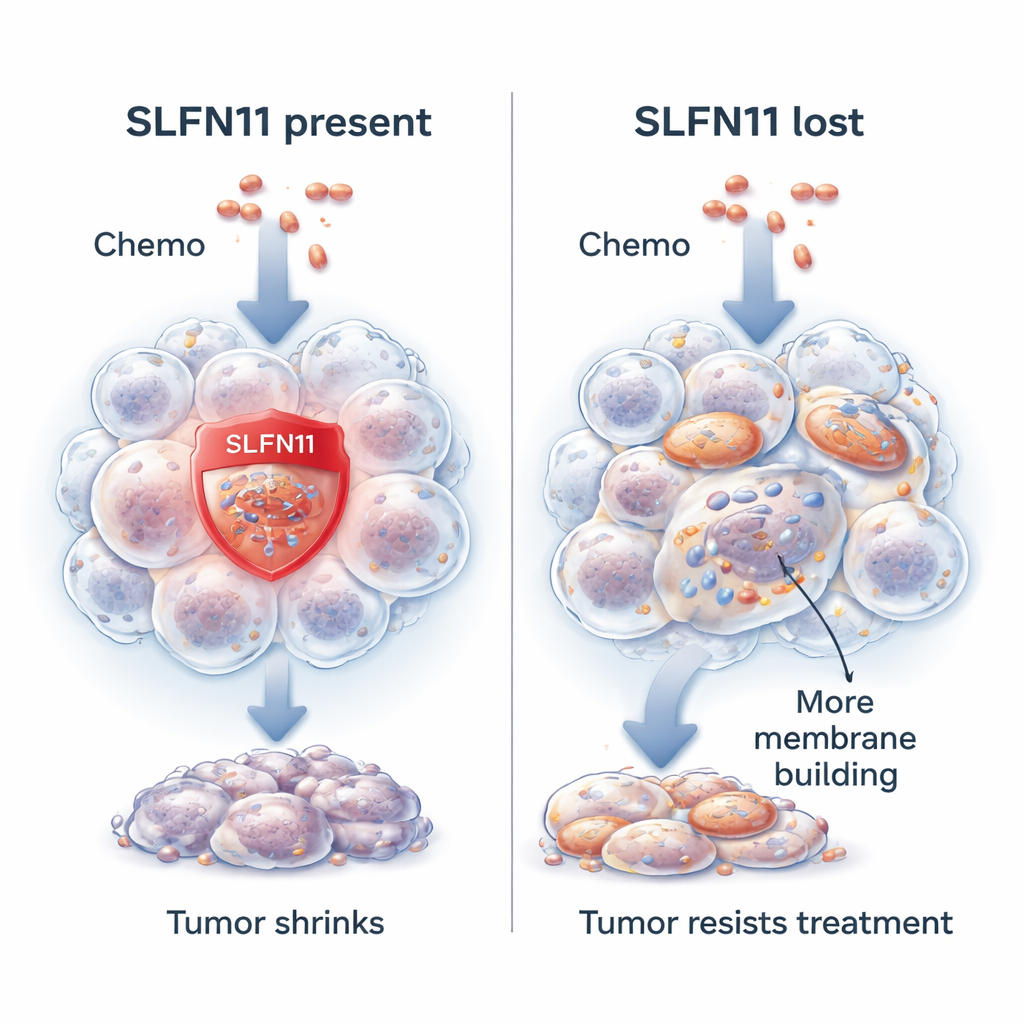
Ген, делающий раковые клетки легчеуничтожимыми
Исследователи сосредоточились на гене под названием SLFN11. Во многих опухолях саркомы Юинга SLFN11 высокоактивен и делает раковые клетки значительно более чувствительными к препаратам, повреждающим ДНК, генетический чертеж клетки. При действии таких препаратов SLFN11 способствует подавлению репарации ДНК и направляет клетку к программируемой гибели. Пациенты с опухолями, содержащими высокий уровень SLFN11, как правило, живут дольше и лучше отвечают на терапию. Однако примерно у одного из десяти опухолей SLFN11 либо изначально мало или отсутствует, либо теряется в ходе лечения. В таких случаях та же химиотерапия становится намного менее эффективной, хотя сами клетки по‑прежнему способны к активному росту.
Как клетки рака перенастраивают использование топлива и жиров
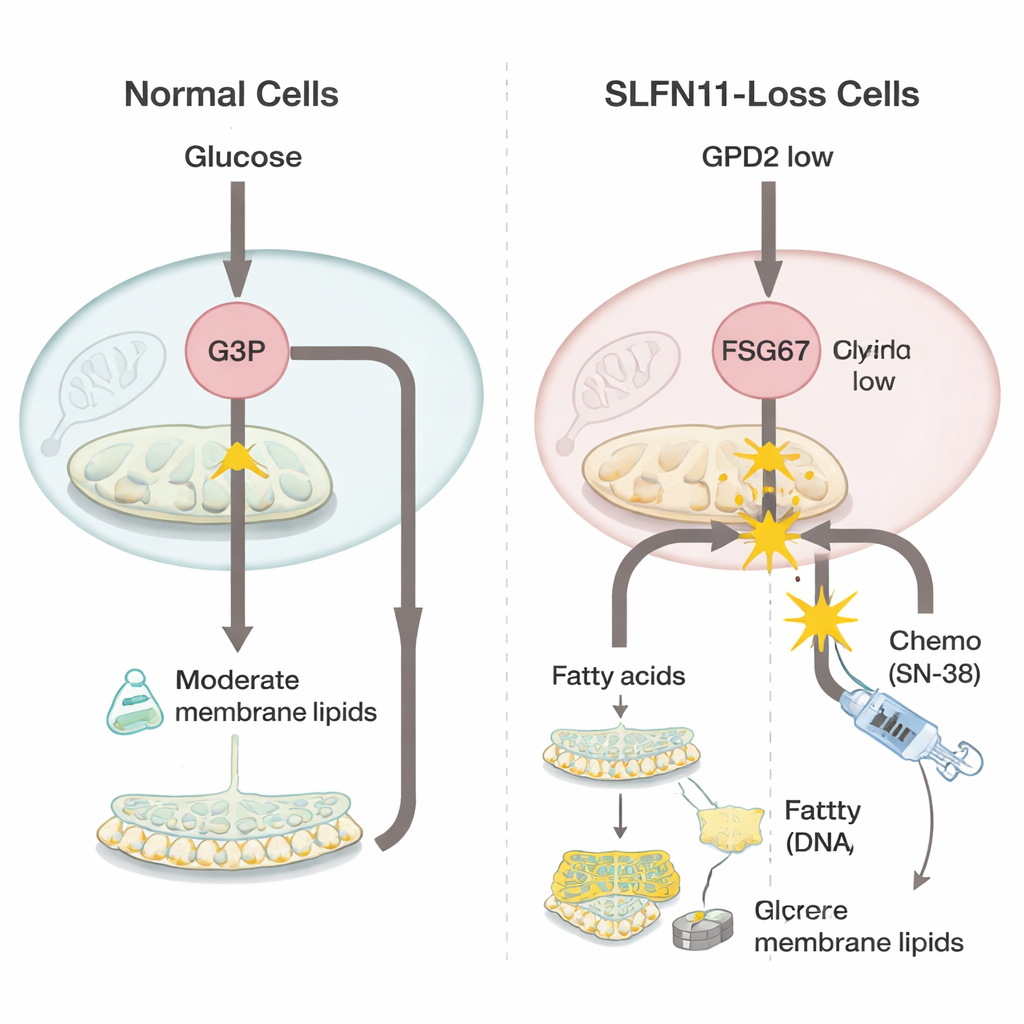
Чтобы понять, какие изменения происходят при потере SLFN11, команда сравнила клетки саркомы Юинга с этим геном и без него, используя мощные «омикс»‑методы, которые одновременно измеряют тысячи генов и малых молекул. Они обнаружили, что клетки, лишённые SLFN11, понижают уровень фермента в митохондриях под названием GPD2, который обычно участвует в окислении молекулы глицерол‑3‑фосфата в составе энергетического обмена. При снижении GPD2 глицерол‑3‑фосфат накапливается. Вместо того чтобы тратиться впустую, этот избыток используется для синтеза большего количества липидных компонентов клеточных мембран — группы, известных как глицерофосфолипиды. Клетки также демонстрировали признаки увеличенного образования более гибких, ненасыщенных жиров, что может помогать быстрорастущим опухолям адаптироваться к стрессу.
Преобразование трюка выживания в слабое место
Поскольку клетки, лишённые SLFN11, сильнее зависят от синтеза мембран, исследователи проверили, можно ли блокирование этого процесса восстановить чувствительность к химиотерапии. Они использовали соединение FSG67, которое ингибирует ключевой этап образования глицерофосфолипидов. Сам по себе стандартный препарат, повреждающий ДНК, SN‑38 стал значительно менее активен в клетках без SLFN11, что отражает клиническую проблему резистентности. Но при комбинации SN‑38 с FSG67 ранее резистентные клетки подвергались значительно более сильному поражению, и оба препарата показали синергетический эффект, превышающий суммарный результат по отдельности. Напротив, в клетках с сохранённым SLFN11, уже высокочувствительных к SN‑38, добавление FSG67 давало мало дополнительной пользы и даже могло быть слегка контрпродуктивным. Такая картина указывает на то, что новая зависимость от синтеза жиров и мембран специфична для резистентного состояния с низким уровнем SLFN11.
Потенциальный неинвазивный маркер трудноизлечимых опухолей
Далее учёные поинтересовались, можно ли эту метаболическую перенастройку обнаружить в реальных опухолях, а не только в клеточных культурах. Они вырастили опухоли саркомы Юинга у мышей с различным статусом SLFN11 и использовали ядерный магнитный резонанс (ЯМР) для анализа химического состава экстрактов опухолей. Опухоли без SLFN11 демонстрировали более высокое отношение двух холинсодержащих молекул, связанных с обменом мембран: фосфохолина и глицерофосфохолина. Высокое отношение фосфохолин/глицерофосфохолин в других типах рака уже связывали с агрессивным поведением и худшей реакцией на лечение. Поскольку холиновые сигналы можно измерять с помощью продвинутых методов визуализации, такое изменение со временем может служить неинвазивным маркером для выявления опухолей саркомы Юинга, которые перешли в это резистентное, усиленно синтезирующее мембраны состояние.
Что это может значить для будущих методов лечения
В целом исследование показывает, что при потере SLFN11 клетки саркомы Юинга становятся менее чувствительны к препаратам, повреждающим ДНК, и компенсируют это перенастройкой метаболизма в сторону увеличения синтеза мембранных липидов. Эта перестройка не только помогает клеткам выживать, но и создаёт новое Ахиллесово пятно. Блокирование образования глицерофосфолипидов с помощью препарата вроде FSG67 может частично восстановить эффективность химиотерапии в этих резистентных клетках. Хотя сам FSG67 пока не является клиническим препаратом, работа указывает на стратегию, при которой в будущем врачи смогут учитывать статус SLFN11 и метаболические особенности опухоли пациента и комбинировать препараты, повреждающие ДНК, с таргетными ингибиторами синтеза жиров и мембран, чтобы преодолеть резистентность.
Цитирование: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Ключевые слова: саркома Юинга, химиорезистентность, SLFN11, метаболизм рака, синтез липидов