Clear Sky Science · ru
Таргетирование гипоксических экзосомальных IGFBP2 преодолевает опосредованное CD47 уклонение от иммунитета при глиобластоме
Почему лишение опухоли кислорода может сыграть назад
Врачи давно знают, что глиобластома — смертельно опасная опухоль мозга — часто растёт в областях, лишённых кислорода. Эти гипоксические участки делают опухоль менее поддающейся лечению. В этом исследовании показано, как низкий уровень кислорода помогает раковым клеткам скрываться от иммунной системы, и предложена новая комбинированная терапия, которая могла бы сделать их более уязвимыми для атаки организма.
Смертельная опухоль мозга, уходящая от нашей защиты
Глиобластома — наиболее агрессивная распространённая опухоль мозга у взрослых, при которой ожидаемая выживаемость обычно измеряется месяцами. Хотя иммунные клетки проникают в эти опухоли, раковые клетки часто избегают уничтожения. Одним из ключевых механизмов ухода является белок на поверхности клеток CD47, иногда называемый «не ешь меня», который сигнализирует соседним иммунным клеткам, таким как макрофаги, не фагоцитировать и не уничтожать опухолевую клетку. Препараты, блокирующие CD47, уже испытывают в клинике, но результаты при солидных опухолях, таких как глиобластома, были смешанными, что указывает на то, что другие факторы в микроокружении опухоли могут подрывать эффективность этих терапий.
Гипоксические зоны и крошечные посылки от рака
С помощью одноклеточного РНК-секвенирования исследователи картировали тысячи клеток из различных областей образцов глиобластомы, сравнивая низко-кислородное ядро опухоли с её периферией. Они обнаружили особенно агрессивный подтип клеток в гипоксическом ядре, называемый мезенхимоподобными клетками ГБМ, которые сильно экспрессировали CD47 и белок IGFBP2. Одновременно они обнаружили, что эти ядро́вые клетки выделяют большое количество нанометровых везикул — экзосом — несущих IGFBP2 на своей поверхности. Поскольку экзосомы могут перемещаться по мозгу и даже попадать в кровоток, они способны распространять сигналы далеко за пределы места своего происхождения. 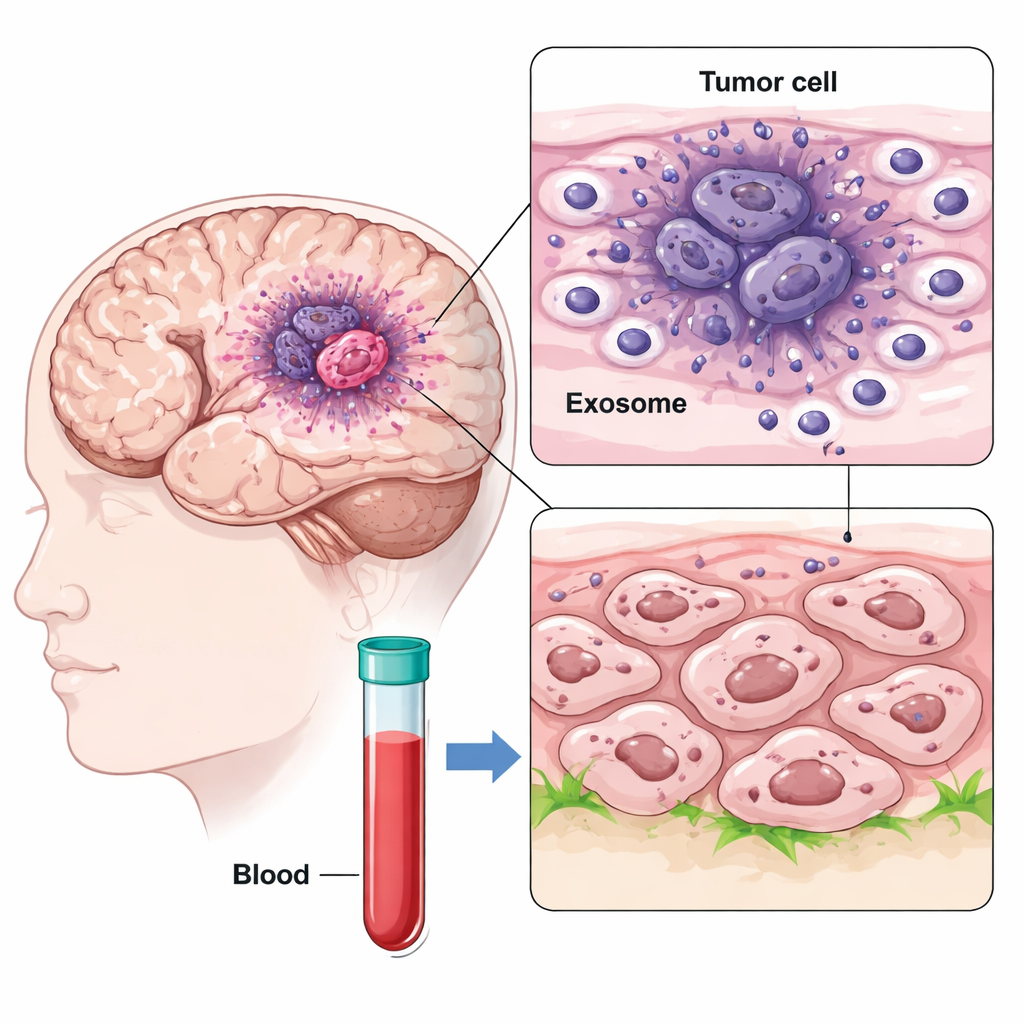
Как партнёрный белок усиливает сигнал «не ешь меня»
Далее команда изучала, что делает IGFBP2. Они показали, что при низком уровне кислорода сенсорный белок гипоксии HIF-2α включает ген IGFBP2 в опухолевых клетках. Затем IGFBP2 связывается со специфическими рецепторами — интегринами — на поверхности экзосом, «украшая» их наружную мембрану. Когда эти покрытые IGFBP2 экзосомы сливаются с другими опухолевыми клетками, они активируют каскад сигналов внутри клетки с участием белков FAK и STAT3. Этот каскад в конечном итоге увеличивает количество CD47 на поверхности опухолевой клетки, усиливая сообщение «не ешь меня» для макрофагов и дополнительно защищая раковые клетки от иммунной атаки. 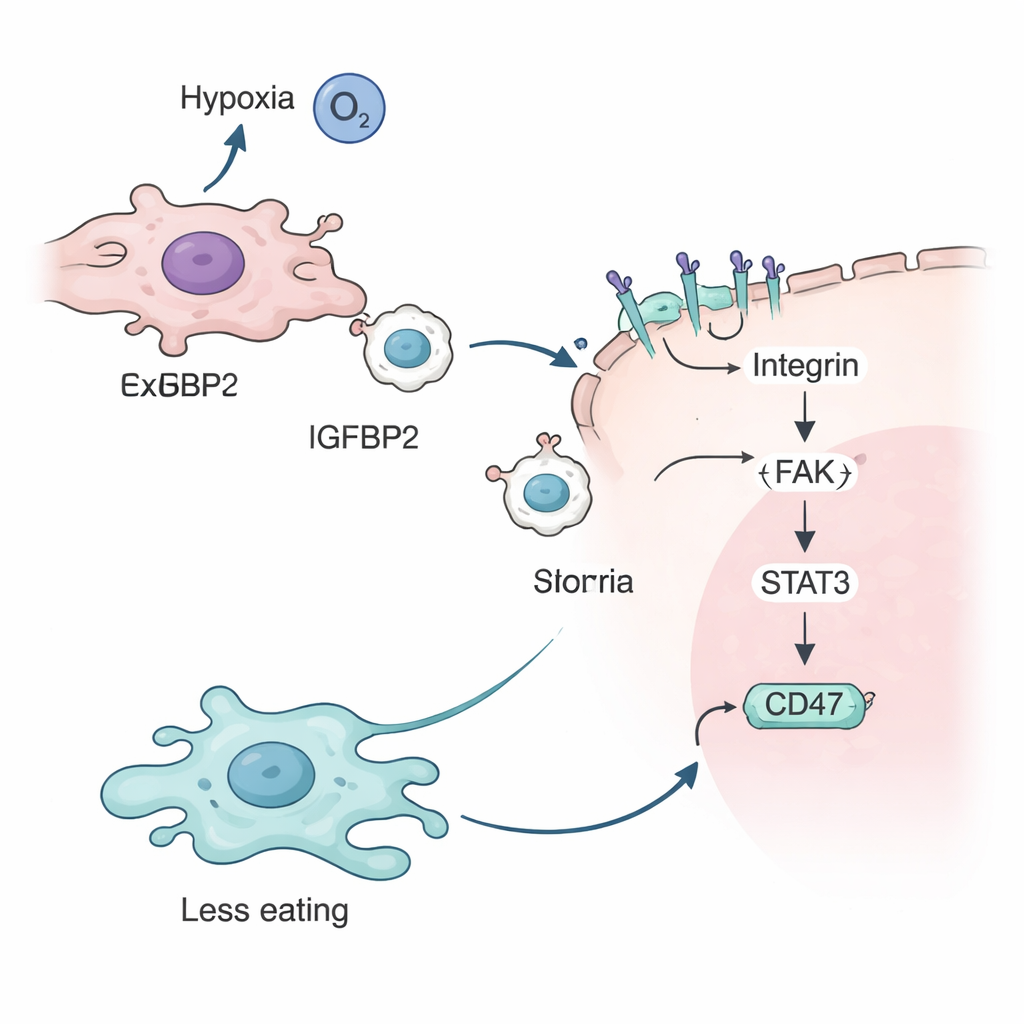
Данные из образцов пациентов и моделей на животных
Чтобы связать лабораторные открытия с реальной болезнью, исследователи проанализировали опухолевую ткань и кровь пациентов с глиомой. Они обнаружили, что уровни IGFBP2 были повышены как в опухолях, так и в экзосомах крови у пациентов с более прогрессирующим заболеванием, что позволяет предположить, что IGFBP2-положительные экзосомы могут служить маркером стадии опухоли в крови. В моделях на мышах снижение IGFBP2 в клетках глиобластомы делало их более уязвимыми для фагоцитоза макрофагами, замедляло рост опухоли и продлевало выживание. Наоборот, добавление дополнительных экзосом, богатых IGFBP2, повышало уровни CD47, снижало фагоцитоз иммунными клетками и ускоряло прогрессию опухоли.
Многообещающая комбинация для терапии
Наконец, команда проверила, может ли блокирование IGFBP2 повысить эффективность терапии, нацеленной на CD47. У мышей с опухолями мозга лечение антителами против IGFBP2 и CD47 в комбинации вызывало более активную работу макрофагов, уменьшение размеров опухолей и более длительное выживание по сравнению с любым из методов по отдельности. Прерывая гипоксию-опосредованный сигнал IGFBP2 и одновременно блокируя сигнал «не ешь меня» CD47, такая комбинированная терапия атаковала иммунную маскировку опухоли в двух направлениях. Для пациентов эти результаты указывают на то, что измерение IGFBP2 в экзосомах крови может помочь выявить тех, кто с наибольшей вероятностью получит пользу от иммунотерапии, нацеленной на CD47, а сочетание ингибиторов IGFBP2 и CD47 может оказаться более эффективной стратегией против глиобластомы, чем каждый препарат по отдельности.
Цитирование: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Ключевые слова: глиобластома, экзосомы, уклонение от иммунитета, CD47, гипоксия