Clear Sky Science · ru
HSPA5 способствует стабильности YAP/TAZ независимо от пути Hippo и индуцирует переход от пронейронального к мезенхимальному типу в глиобластоме
Почему это исследование рака мозга важно
Глиобластома — один из самых смертельных видов рака мозга, отчасти потому, что многие опухоли со временем переходят в более устойчивое к лечению состояние. В этом исследовании показано, как распространённый белок стресс‑ответа HSPA5 способствует этому сдвигу и обеспечивает более длительную жизнь молекулам, поддерживающим опухоль, чем им полагается. Понимание этого «трюка выживания» указывает на новые способы сделать глиобластому менее агрессивной и более чувствительной к существующим терапиям.
Опухоль, меняющая «характер»
Врачи и учёные теперь признают, что глиобластома — это не единое заболевание, а смесь молекулярных подтипов. Два основных варианта — «пронейрональный» тип, который обычно менее агрессивен, и «мезенхимальный» тип, более инвазивный, устойчивый к лечению и связанный с более ранним рецидивом. Опухоли могут эволюционировать от пронейронального к мезенхимальному состоянию — процесс, который авторы называют переходом от пронейронального к мезенхимальному (PMT). Команда поставила задачу выяснить, какие белки стресс‑ответа могут продвигать опухоль по этому опасному пути.
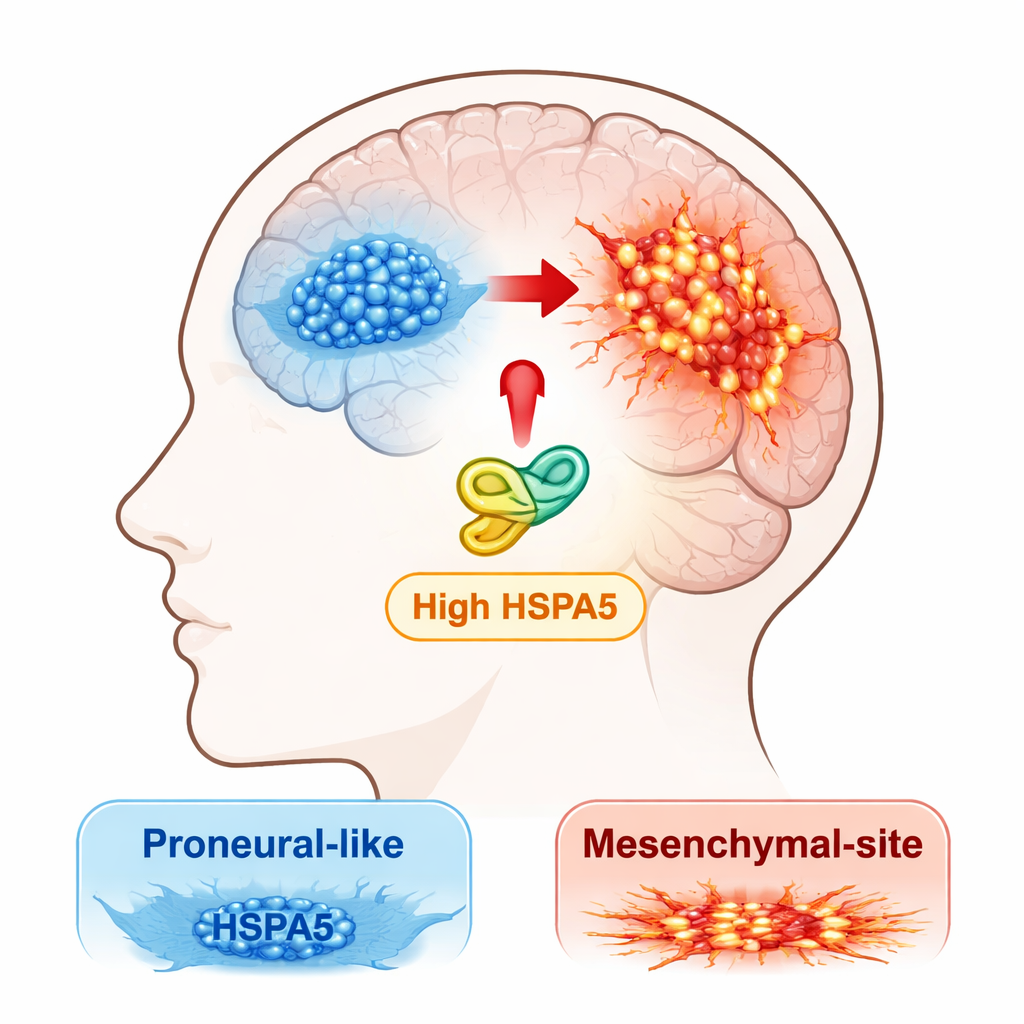
Белок‑помощник стресса в центре внимания
Исследователи начали с анализа больших открытых онкологических баз данных и собственных образцов пациентов в поисках членов семейства HSP70 — группы «шаперонных» белков, помогающих другим белкам правильно сворачиваться и выживать при стрессе. Один шаперон, HSPA5, выделился. Его активность была наибольшей в мезенхимальном подтипе глиобластомы и заметно выше в опухолях по сравнению с нормальной тканью мозга. У пациентов с опухолями, содержащими больше HSPA5, наблюдалась худшая общая выживаемость, что подчёркивает его роль потенциального драйвера агрессивного заболевания, а не пассивного наблюдателя.
Принуждение клеток к более агрессивному поведению
Чтобы выяснить, что HSPA5 делает внутри опухолевых клеток, команда вырастила первичные клетки глиобластомы, выделенные непосредственно у пациентов, и разделила их на похожие на пронейрональные и на мезенхимальные группы. Когда пронейрональным клеткам заставляли синтезировать дополнительный HSPA5, они начали вести себя как мезенхимальные: делиться быстрее, активнее мигрировать и инваировать, включать характерные мезенхимальные маркеры, такие как CD44 и c‑MET, и снижать экспрессию пронейрональных маркеров, таких как SOX2 и OLIG2. Обратное также верно — уменьшение уровня HSPA5 в мезенхимальных клетках снижало их рост и инвазию и частично возвращало их к менее агрессивному профилю.
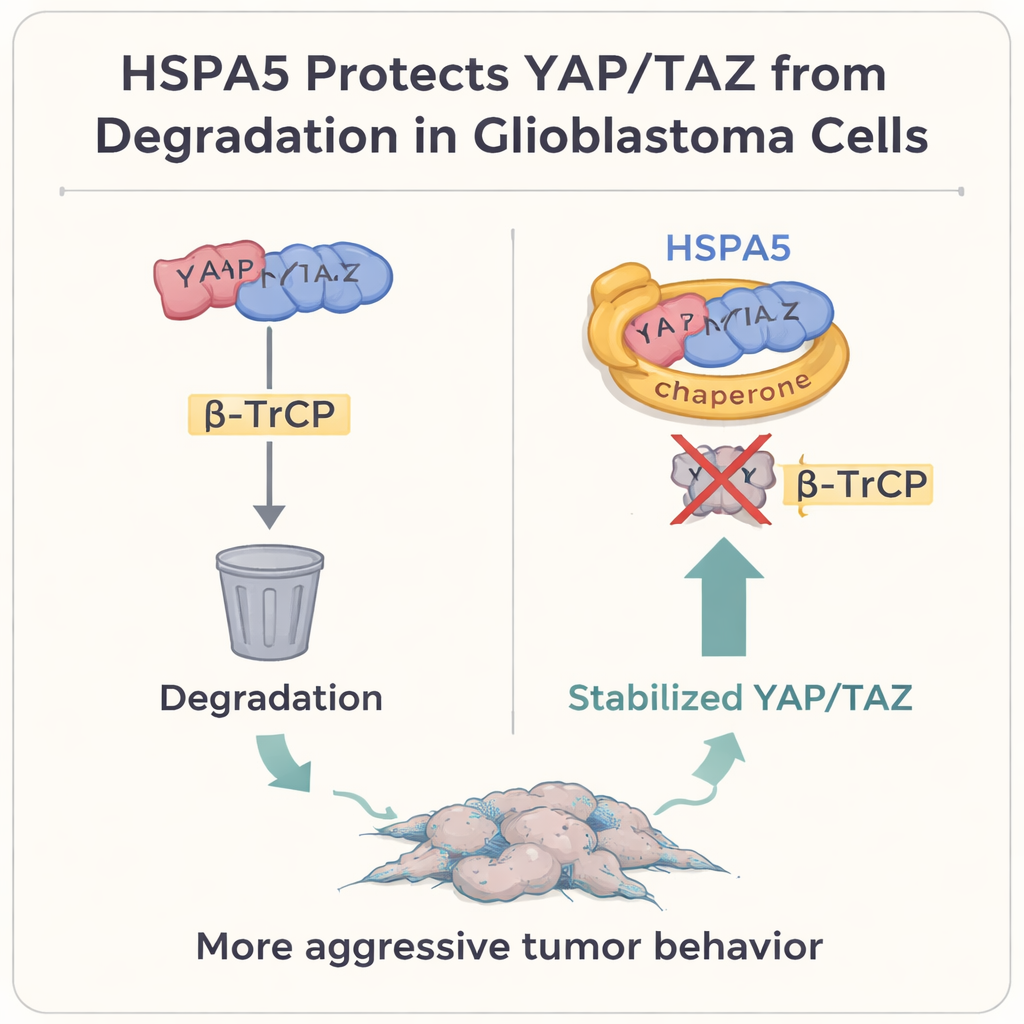
Защита ключевых переключателей роста от «мусорной корзины» клетки
Углубляясь, авторы сосредоточились на двух мощных регуляторах роста — YAP и TAZ, которые находятся в центре сигнального пути Hippo. Во многих солидных опухолях, включая глиобластому, эти белки действуют как главные переключатели, способствующие росту клеток, пластичности и мезенхимальному состоянию. Обычно, когда клетка пытается сдержать эту программу, она помечает YAP и TAZ для уничтожения посредством белка β‑TrCP, который направляет их к «мусорной корзине» клетки — протеасоме. В исследовании показано, что HSPA5 физически связывается с YAP и TAZ, используя свой домен связывания субъстрата подобно защитной перчатке. Это мешает прикреплению β‑TrCP, предотвращает убиквитинирование и разрушение YAP/TAZ и позволяет им накапливаться в ядре, где они включают мезенхимальные гены, в том числе CD44 и c‑MET.
От чашек Петри и мышей до опухолей у пациентов
Команда подтверждала этот механизм несколькими способами. Блокирование HSPA5 ускоряло исчезновение белков YAP и TAZ, если только протеасома не была химически ингибирована, и увеличивало сигналы «мусорной» метки на них. Повторная активация YAP и TAZ восстанавливала потерю роста и инвазии, наблюдавшуюся при снижении HSPA5, тогда как подавление YAP/TAZ устраняло про‑опухолевые эффекты сверхэкспрессии HSPA5. В мышиных моделях, где человеческие клетки глиобластомы имплантировали в мозг, опухоли с высоким уровнем HSPA5 росли больше и быстрее уничтожалиских животных; снижение HSPA5 или прерывание его поддержки YAP/TAZ замедляло рост и продлевало выживание. Наконец, в парных образцах у тех же пациентов, взятых до и после рецидива, рецидивирующие, более мезенхимальные опухоли показывали более высокие уровни HSPA5, YAP, TAZ и мезенхимальных маркеров по сравнению с исходными пронейрональными опухолями.
Что это значит для будущего лечения рака мозга
Проще говоря, эта работа показывает, что клетки глиобластомы используют помощник стресс‑ответа HSPA5, чтобы защищать ключевые переключатели роста (YAP и TAZ) от разрушения. Эта защита помогает опухолям перейти в и поддерживать более агрессивную, устойчивую к лечению идентичность. Поскольку малые молекулы‑ингибиторы HSPA5 уже существуют и опухолевые клетки могут сильнее зависеть от этого шаперона, чем нормальные клетки, ось HSPA5–YAP/TAZ представляет собой привлекательную новую мишень. Терапии, ослабляющие этот защитный щит, могут сделать клетки глиобластомы менее адаптивными, менее инвазивными и более уязвимыми к стандартным методам лечения, таким как химио‑ и радиотерапия.
Цитирование: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Ключевые слова: глиобластома, HSPA5, YAP/TAZ, пластичность опухоли, мезенхимальный переход