Clear Sky Science · ru
Митохондриальная ДНК активирует ось NLRP3–IL-1β в микроглии, связываясь с NLRP3 и приводя к нейродегенерации в моделях болезни Паркинсона
Почему это важно для болезни Паркинсона
Болезнь Паркинсона наиболее известна тремором и замедленностью движений, но за этими симптомами скрывается сложная внутричерепная борьба. В этом исследовании показано, как крошечные фрагменты генетического материала из повреждённых митохондрий в иммунных клетках мозга могут инициировать воспаление, которое постепенно убивает дофамин-продуцирующие нейроны, необходимые для плавных движений. Понимание этой цепочки реакций открывает новые, весьма конкретные мишени для лекарств, которые могли бы замедлить или предотвратить повреждение, подобное болезни Паркинсона.
Иммунные клетки мозга и «электростанции» под стрессом
В мозге есть не только нейроны, но и микроглия — его ресидентные иммунные клетки. При болезни Паркинсона микроглия часто становится гиперактивной, выделяя токсичные молекулы и провоспалительные сигналы, которые вредят соседним нейронам. Авторы сосредоточились на митохондриях — «электростанциях» клеток, которые имеют собственную ДНК. Когда митохондрии повреждаются — из‑за токсинов, старения или других стрессов — их ДНК может окисляться, то есть получать химические повреждения под действием реактивных форм кислорода. Поскольку митохондриальная ДНК по строению напоминает бактериальную, эти повреждённые фрагменты могут действовать как сигналы тревоги в мозге, активируя иммунную систему и потенциально поддерживая хроническое воспаление.
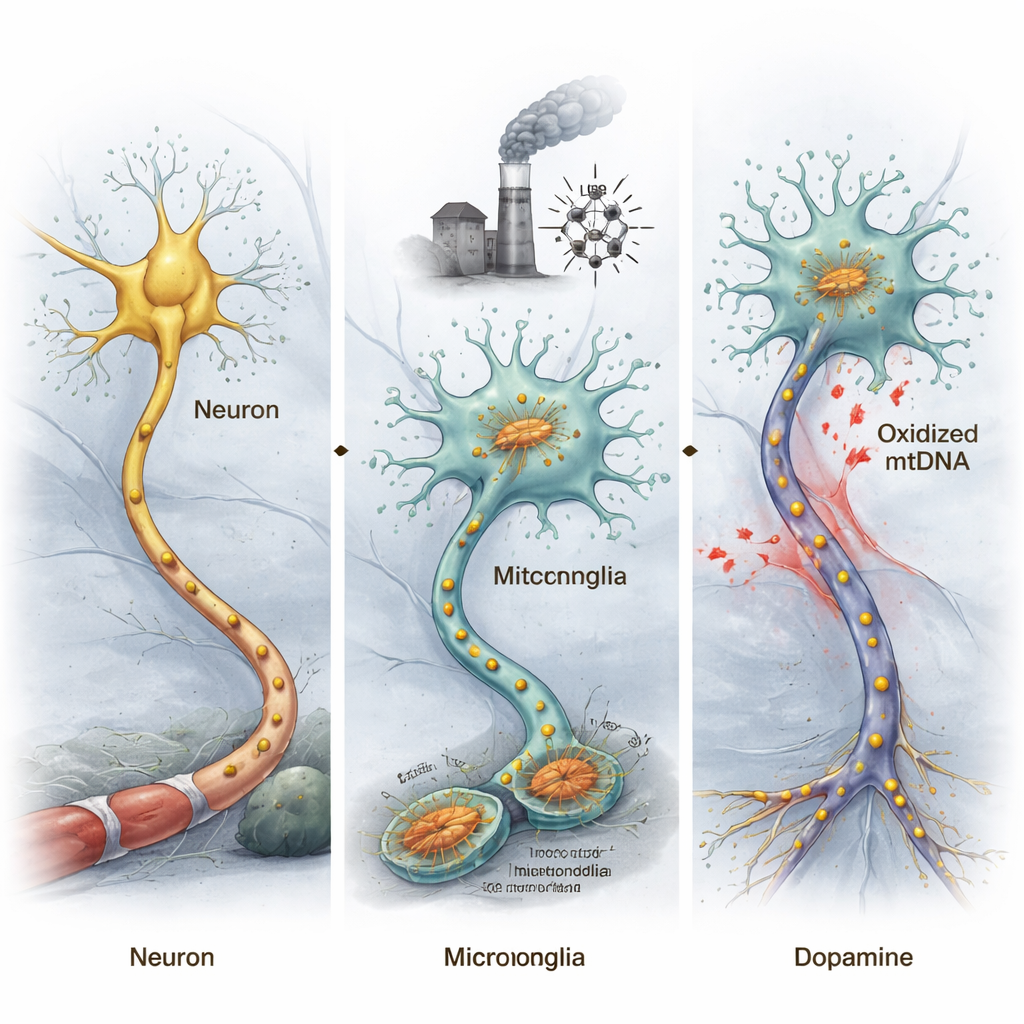
Повреждённая митохондриальная ДНК может толкать мышей к состоянию, похожему на Паркинсона
Чтобы проверить, может ли окисленная митохондриальная ДНК (ox-mtDNA) реально запускать изменения, похожие на паркинсонизм, исследователи экстрагировали ox-mtDNA из стрессированных микроглиальных клеток и вводили его непосредственно в область мозга, где обычно находятся дофамин-продуцирующие нейроны, важные для движений. Мыши, подвергшиеся воздействию этой ox-mtDNA, показали снижение подвижности в поведенческих тестах и потерю этих дофаминовых нейронов, что отражает ключевые признаки болезни Паркинсона. Разделив нейроны и микроглию из среднего мозга и проанализировав их активность генов, команда обнаружила усиление аномалий в генах, связанных с болезнью Паркинсона, в нейронах, тогда как у микроглии сильно активировались гены, связанные с воспалением.
Молекулярный выключатель тревоги внутри микроглии
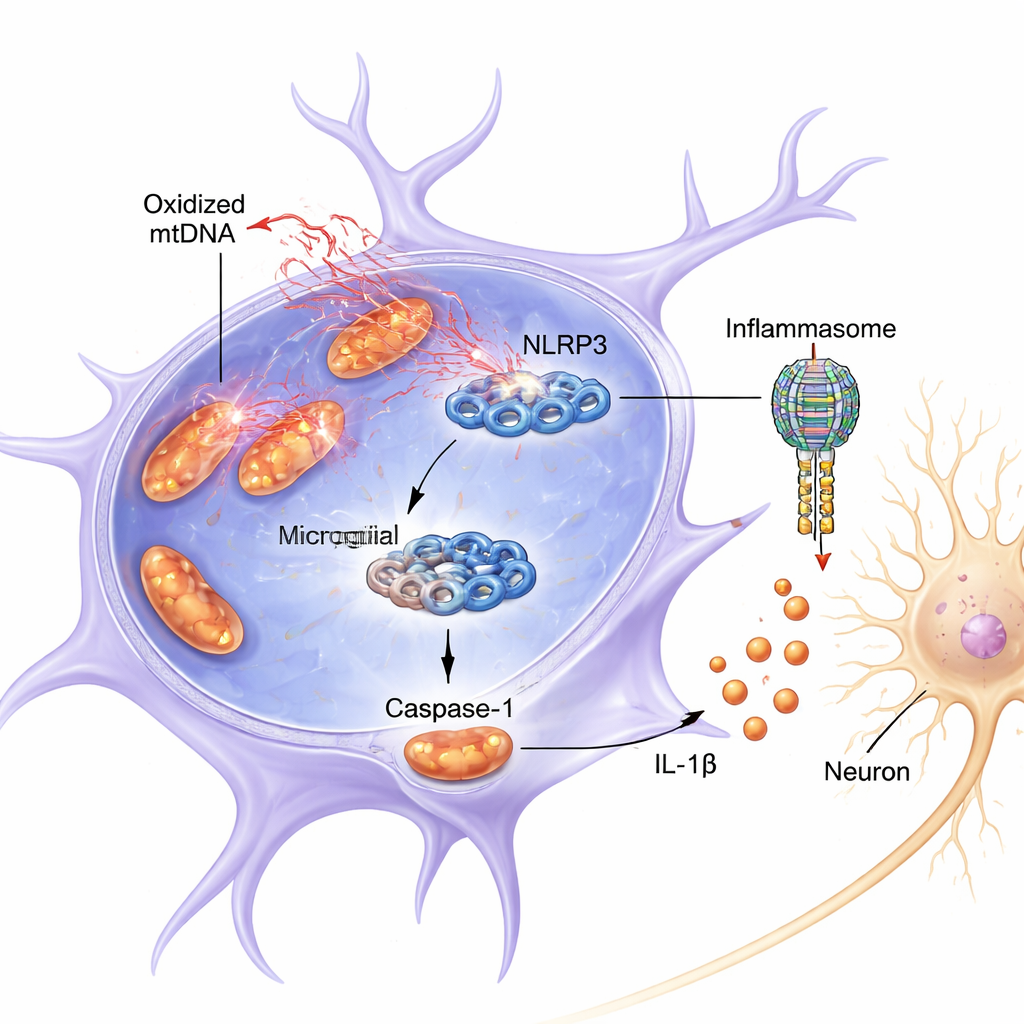
Исследование сфокусировалось на белковом комплексе в микроглии, называемом NLRP3, который входит в состав более крупного агрегата — инфламмасомы. При активации NLRP3 способствует включению каспазы‑1, фермента, который расщепляет провоспалительную молекулу IL‑1β до её активной, вредной формы. Как в опытах на мышах, так и в культурах клеток сочетание провоспалительного прайминга (LPS, компонент бактерий) и токсина, похожего на пестицид (ротенон) вызывало у микроглии выброс окисленной митохондриальной ДНК в цитозоль. Этот выброс совпадал с усиленной активацией NLRP3, повышением уровня расщеплённой (активной) каспазы‑1 и увеличением IL‑1β. Среда, забранная из этих чрезмерно активированных микроглиальных клеток, была напрямую токсична для выращенных в чашке нейроноподобных дофаминовых клеток, снижая их выживаемость и уровень ключевого маркера — тирозин гидроксилазы.
Прямое связывание: как окисленная ДНК включает переключатель NLRP3
Помимо простой корреляции, авторы показали, что ox-mtDNA не только присутствует при воспалении — оно, по-видимому, физически связывается с NLRP3 и включает его. Когда они блокировали выход митохондриальной ДНК с помощью препарата, активация каспазы‑1 и IL‑1β снижалась. Наоборот, прямая доставка окисленной mtDNA в микроглию значительно усиливала сигналы NLRP3 больше, чем неокислённая mtDNA. С помощью биохимических pull‑down экспериментов они обнаружили mtDNA, богатую маркерами окислительного повреждения, связанную с NLRP3. Компьютерное моделирование и протеиновая химия показали, что ox-mtDNA связывается с положительно заряженным, гибким сегментом NLRP3 (внутренне неструктурированная область) в пределах аминокислот 180–187. Когда этот критический участок удаляли из NLRP3, его способность связывать ox-mtDNA и активировать каспазу‑1 значительно уменьшалась.
Выключение инфламмасомы бережёт нейроны
Далее исследователи выяснили, может ли вмешательство в работу NLRP3 защитить нейроны. В культурах микроглии генетическое снижение уровня NLRP3 резко уменьшало активацию каспазы‑1 и IL‑1β после обработки LPS и ротеноном, а кондиционированная среда от этих клеток была гораздо менее токсичной для нейроноподобных дофаминовых клеток. У мышей селективный ингибитор NLRP3 (MCC950) снижал активацию микроглии, сохранял дофаминовые нейроны и уменьшал уровни белков, связанных с инфламмасомой, в моделях, вызванных либо LPS с ротеноном, либо введением mtDNA. В совокупности эти эксперименты показывают, что цепочка ox-mtDNA–NLRP3–IL‑1β не просто ассоциирована с повреждением — она необходима для значительной части наблюдаемой потери нейронов.
Что это значит для будущих терапий болезни Паркинсона
Для неспециалистов главный вывод в том, что повреждённая митохондриальная ДНК, утекающая из иммунных клеток мозга, может напрямую «зацепиться» за внутренний «выключатель тревоги» (NLRP3), вызывая волну воспаления, которая повреждает дофаминовые нейроны и в моделях приводит к состоянию, близкому к болезни Паркинсона. Поскольку это взаимодействие опирается на короткий, четко определённый участок белка NLRP3 и на окислённую природу митохондриальной ДНК, оно предлагает точные новые лекарственные мишени. Терапии, которые предотвращают повреждение или выход митохондриальной ДНК, блокируют её связывание с NLRP3 или ингибируют сам NLRP3, теоретически могут охладить этот воспалительный каскад и замедлить прогрессирование болезни Паркинсона.
Цитирование: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Ключевые слова: болезнь Паркинсона, микроглия, митохондриальная ДНК, инфламмасома NLRP3, нейровоспаление