Clear Sky Science · ru
Дефицит, опосредованный SLC46A1, и ограничение фолата подавляют прогрессию колоректального рака через эпигенетико-транскрипционную перепрограммировку
Почему витамин B9 и рак кишечника — неожиданная пара
Многие знают фолат, или витамин B9, как питательное вещество, важное при беременности и для здоровья сердца. В этом исследовании показано, что фолат также играет неожиданную роль при раке толстой и прямой кишки. Суть в том, что польза фолата зависит от одного «привратного» белка на поверхности раковых клеток — SLC46A1, который решает, сколько фолата действительно попадёт внутрь опухолевых клеток. Понимание этой скрытой «двери» может помочь объяснить, почему прежние исследования фолата и рака оказались противоречивыми, и может дать направление для более безопасного использования фолата в питании и лечении.
Питательный привратник в кишечнике
Клетки нашего кишечника не синтезируют фолат сами; они должны захватывать его из окружающей среды с помощью специальных транспортных белков. Авторы показывают, что SLC46A1 является основным фолатным транспортером в человеческом толстом кишечнике, значительно более активным, чем другие известные переносчики фолата. При анализе крупных общедоступных онкологических наборов данных и образцов тканей пациентов они обнаружили, что уровень SLC46A1 резко снижен в колоректальных опухолях по сравнению с прилегающей здоровой тканью. Опухоли с более низким уровнем SLC46A1, как правило, были более продвинутыми, с большей вероятностью давали метастазы и были связаны с худшим выживанием пациентов, что указывает на то, что этот транспортер ведёт себя скорее как тормоз, а не как ускоритель при этом виде рака.
Как утрата «двери» меняет поведение рака
Чтобы проверить функцию SLC46A1, исследователи изменяли его уровень в линиях клеток колоректального рака. При снижении SLC46A1 клетки росли быстрее, легче мигрировали и проникали через искусственные барьеры в лабораторных условиях. При повышении уровня SLC46A1 в клетках с низкой экспрессией они становились менее инвазивными. Аналогичные закономерности наблюдались у мышей: опухоли, выросшие из клеток с дефицитом SLC46A1, были крупнее и давали больше метастазов в лёгких. В то же время опухоли и культивируемые клетки с уменьшенным SLC46A1 содержали меньше фолата внутри, что подтверждало, что этот белок действительно служит ключевым входом для витамина.
От нехватки витамина к нарушенному контролю генов
Фолат делает больше, чем просто участвует в синтезе строительных блоков ДНК; он также подпитывает химическую систему, наносящую маленькие метильные «ярлыки» на ДНК, которые помогают включать или выключать гены. Команда показала, что при утрате SLC46A1 и снижении уровня фолата внутри клетки общая способность устанавливать эти метки падает. Это избирательно удаляет метильные метки из контрольной области гена FOS, хорошо известного драйвера клеточного роста. Без этих меток FOS включается и активирует несколько генов, отвечающих за «рост и распространение», включая CCND1, BCL2 и PLAU, которые помогают раковым клеткам делиться, избегать смерти и прорваться через окружающие ткани. Блокирование FOS или PLAU в значительной степени устраняло дополнительный рост и инвазивность, вызванные потерей SLC46A1, связывая эту цепочку событий воедино.
Когда фолат помогает только если дверь открыта
Исследование также проясняет, когда сам фолат благоприятен или вреден для опухолей. В культурах клеток, выращенных в условиях дефицита фолата, возвращение фолата на уровнях, сходных с таковыми в крови человека, замедляло рост и движение раковых клеток — но только если SLC46A1 присутствовал и мог доставить фолат внутрь. В опухолях мышей прямые инъекции фолата в опухолевую массу уменьшали рост и снижали признаки деления клеток, снова только когда раковые клетки продолжали синтезировать SLC46A1. Опухоли, лишённые этого транспортёра, почти не реагировали. В образцах пациентов исследователи наблюдали обратный паттерн: опухоли с высоким уровнем SLC46A1 имели более низкий фолат в окружающей жидкости, словно эффективно его поглощая, и демонстрировали более низкие уровни FOS и PLAU. Опухоли с низким SLC46A1 оставляли больше фолата неиспользованным и имели повышенные уровни этих маркеров агрессивности.
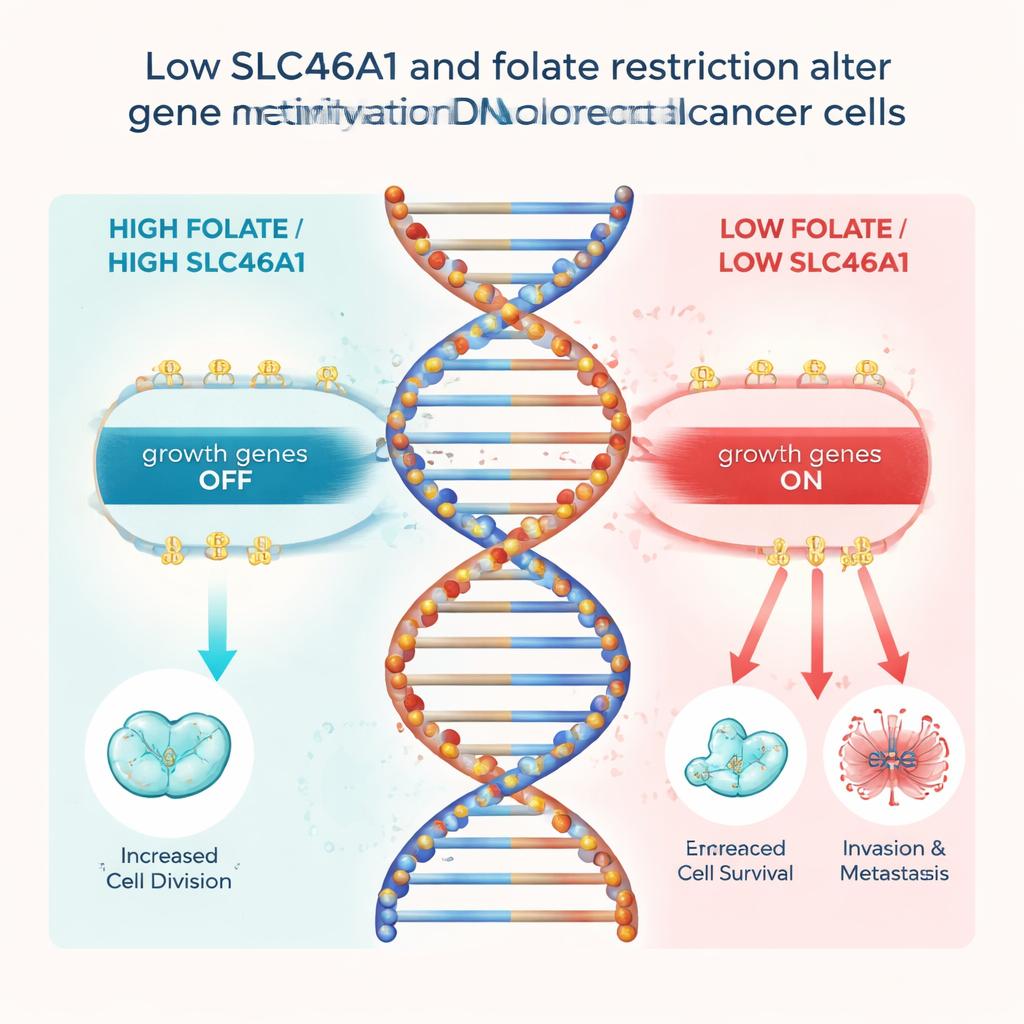
Что это значит для пациентов и профилактики
Для непрофессионала главный вывод таков: влияние фолата на колоректальный рак зависит от того, экспрессируют ли опухолевые клетки «дверь» SLC46A1, позволяющую фолату войти. Когда эта дверь присутствует, реалистичные количества фолата могут поддерживать здоровую систему ДНК-меток и помогать держать в узде гены, стимулирующие рост. Когда дверь отсутствует, опухоль не может использовать фолат в этой защитной роли и вместо этого смещается в более агрессивное состояние, управляемое высвобождёнными генами, такими как FOS. Работа предполагает, что в будущем скрининг колоректальных опухолей на уровень SLC46A1 может помочь врачам предсказывать прогноз и решать, будут ли диеты или лечения, связанные с фолатом, полезны, что является шагом к более персонализированной, учитывающей питание онкологической помощи.
Цитирование: Zhou, Y., Liu, Y., Liu, Y. et al. SLC46A1 deficiency-mediated folate restriction suppresses colorectal cancer progression through epigenetic-transcriptional reprogramming. Cell Death Dis 17, 189 (2026). https://doi.org/10.1038/s41419-026-08423-8
Ключевые слова: фолат, колоректальный рак, эпигенетика, SLC46A1, метилирование ДНК