Clear Sky Science · ru
Таргетирование GNG4 тормозит прогрессирование опухоли и возвращает чувствительность к энзалутамиду при раке предстательной железы за счёт подавления аутофагии
Почему это исследование важно
У многих мужчин с прогрессирующим раком предстательной железы мощные гормоноподавляющие препараты, такие как энзалутамид, изначально хорошо работают, но со временем их эффект слабеет. В этом исследовании обнаружен скрытый «приём» выживания, который используют опухолевые клетки, и выделен конкретный белок — GNG4, — помогающий опухолям продолжать расти и сопротивляться лечению. Понимание этого механизма может привести к комбинированным терапиям, которые сделают существующие препараты более эффективными и долговечными.
Переключатель белка на виду у всех
Клетки рака предстательной железы сильно зависят от мужских гормонов, поэтому стандартная терапия при распространённом заболевании направлена на блокировку этих сигналов. Тем не менее большинство опухолей со временем становятся «кастрационно-устойчивыми» и вновь начинают расти. Авторы искали гены, которые значительно более активны в опухолевой ткани по сравнению с прилежащей нормальной предстательной железой у тех же пациентов. Среди нескольких кандидатов выделился GNG4: при снижении его уровня в клетках рака предстательной железы рост опухолевых клеток резко уменьшался. Анализы сотен образцов пациентов подтвердили, что GNG4 выше в первичных раках предстательной железы по сравнению с нормальной тканью и особенно повышен в более агрессивных, высокогрейдовых опухолях.
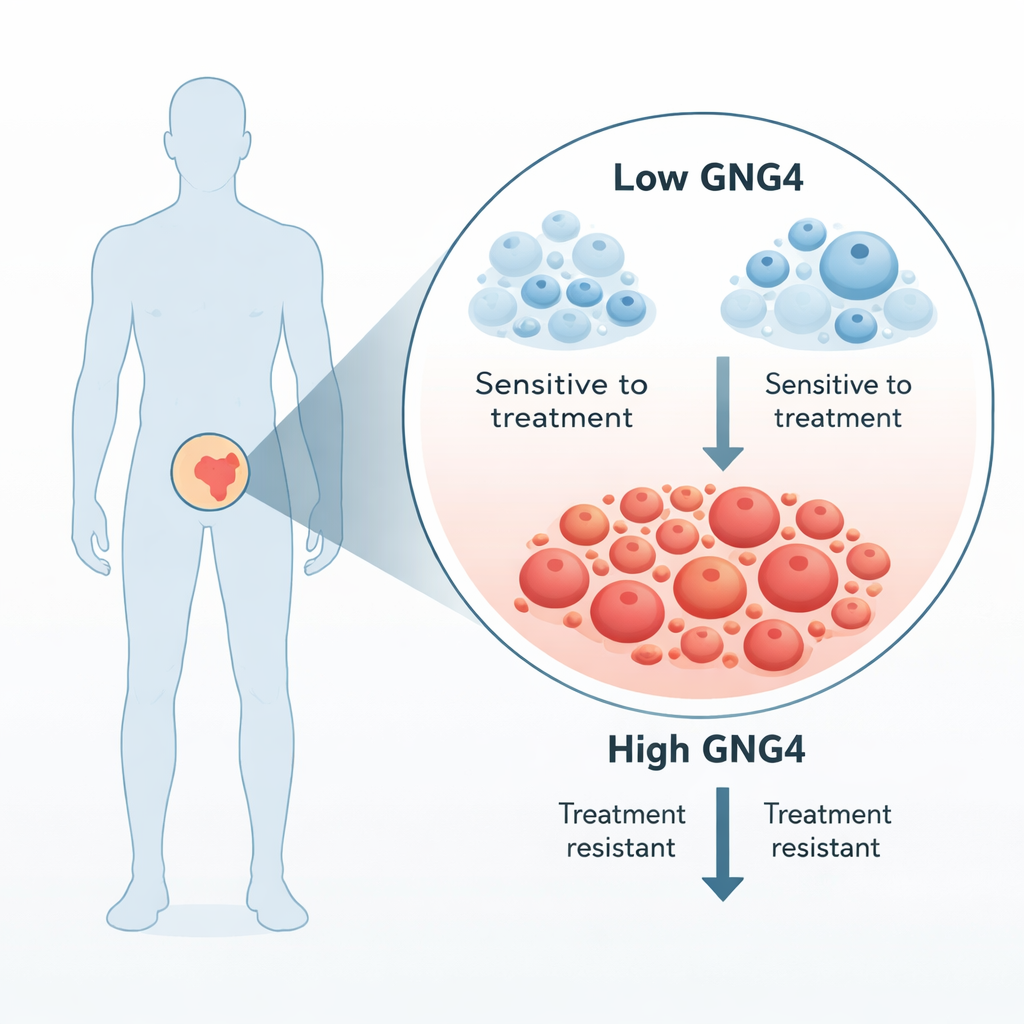
Как GNG4 помогает опухолям выживать
GNG4 входит в более крупное семейство сигнальных белков, известных как G‑белки, которые располагаются в мембране клетки и передают внешние сигналы во внутреннее пространство клетки. Команда показала, что подавление GNG4 в линиях клеток рака предстательной железы замедляло деление клеток, вызывало остановку на контрольной точке клеточного цикла и увеличивало программируемую клеточную гибель. Эти изменения также снижали способность раковых клеток мигрировать и закрывать раны в лабораторных тестах, а опухоли, образованные клетками с дефицитом GNG4, росли медленнее у мышей. В совокупности эти данные указывают, что GNG4 действует как педаль газа для роста и распространения рака предстательной железы.
Аутофагия: запасный продовольственный шкаф раковой клетки
Далее исследователи сосредоточились на процессе, называемом аутофагией, при котором клетки расщепляют и повторно используют свои собственные компоненты, чтобы пережить стресс — например голодание или лечение лекарствами. Во многих продвинутых формах рака аутофагия служит аварийным «кладовым», помогающим опухолевым клеткам справляться с неблагоприятными условиями. В этом исследовании клетки рака предстательной железы с высокой активностью GNG4 демонстрировали больше признаков активной аутофагии, тогда как клетки с пониженным GNG4 имели меньше структур для переработки и более низкие уровни ключевых маркеров аутофагии. При сверхэкспрессии GNG4 клетки лучше переносили энзалутамид и испытывали меньше гибели. Блокирование аутофагии химическим ингибитором устраняло большую часть этой защиты, что указывает на то, что GNG4 помогает опухолям выживать при лечении главным образом за счёт усиления системы переработки.
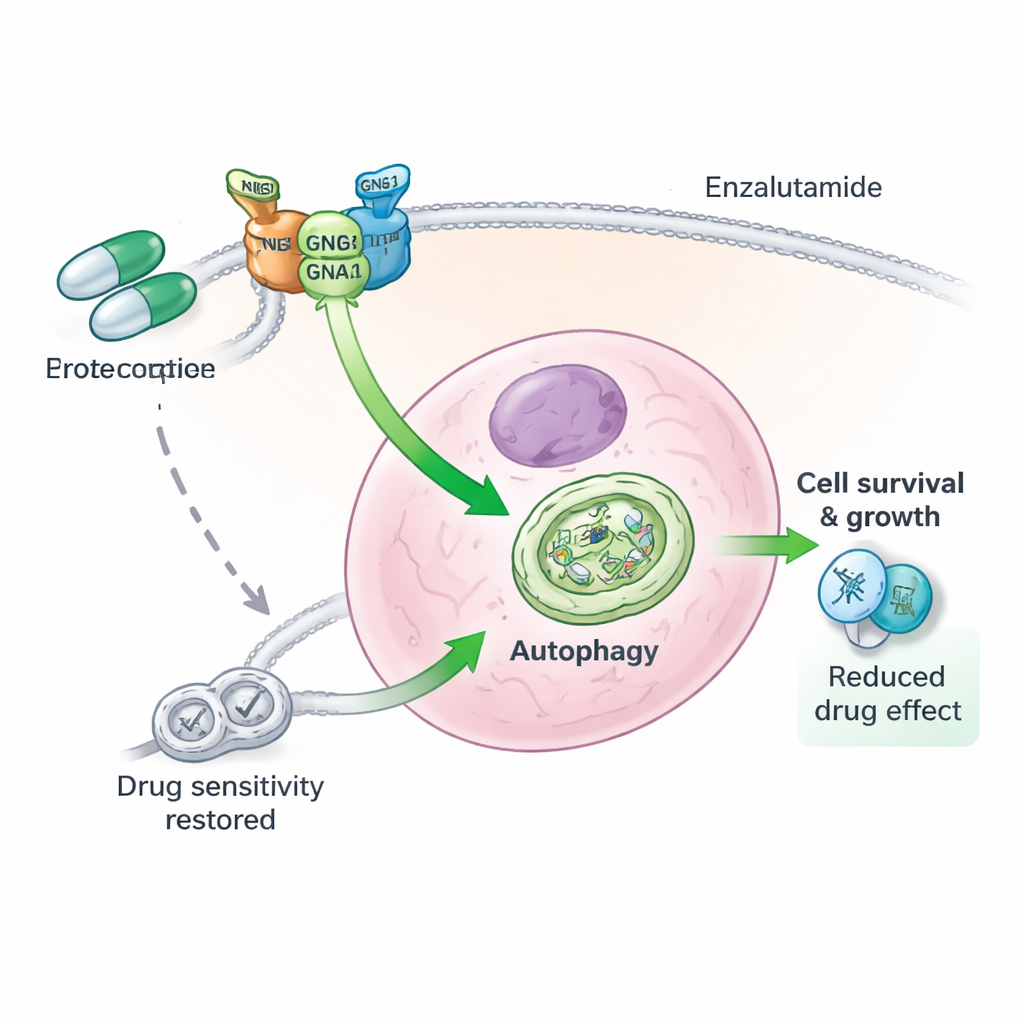
Трёхкомпонентная белковая команда, стоящая за лекарственной устойчивостью
Углубившись, авторы обнаружили, что GNG4 не действует в одиночку. Он физически взаимодействует с другим компонентом G‑белка, GNB1, чтобы стабилизировать третий белок — GNAI3. Вместе эти три субъединицы образуют функциональный комплекс, усиливающий аутофагию в клетках рака предстательной железы. При снижении уровня GNG4 белок GNAI3 быстрее помечался для разрушения и утилизировался клеточными системами утилизации, что выключало аутофагический сигнал. Удаление самого GNAI3 отменяло преимущества в росте и выживании, которые давала лишняя экспрессия GNG4, как в культурах клеток, так и в опухолях у мышей. Иными словами, GNG4 стимулирует злокачественность и устойчивость к стрессу главным образом через ось GNG4–GNB1–GNAI3.
Как повысить эффективность существующих препаратов
Наконец, команда изучила, что происходит при сочетании таргетирования GNG4 с энзалутамидом, ведущим препаратом при запущенном раке предстательной железы. В лаборатории подавление GNG4 значительно повышало чувствительность клеток к энзалутамиду и снижало их способность образовывать колонии после лечения. У мышей опухоли с пониженным GNG4 сильнее уменьшались при назначении энзалутамида, чем опухоли с нормальным уровнем GNG4, без очевидного усиления токсичности. Прямое блокирование аутофагии давало похожие улучшения. Эти результаты предполагают, что вмешательство в индуцированную GNG4 аутофагию может лишить опухолевые клетки важного механизма выживания, позволив существующим гормоноподавляющим терапиям нанести более сильный и продолжительный удар.
Что это значит для пациентов
Для неспециалиста главный вывод таков: некоторые раки предстательной железы переживают лечение, включая механизм внутренней переработки, работающий как резервный генератор. В этом исследовании GNG4 идентифицирован как главный переключатель, включающий этот механизм; он действует вместе с партнёрскими белками, защищая клетки от энзалутамида. Отключив этот переключатель — либо напрямую нацелившись на GNG4, либо безопасно подавив аутофагию — будущие терапии могут замедлить рост опухоли и вернуть чувствительность к лекарствам у мужчин, чьи опухоли стали трудно поддающимися лечению.
Цитирование: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Ключевые слова: рак предстательной железы, лекарственная резистентность, аутофагия, G‑белки, энзалутамид