Clear Sky Science · ru
DNA-PKcs координирует вызванный истощением CTLA-4 процесс старения в раковых клетках
Преобразование переключателя роста рака в сигнал «стоп»
Иммунотерапевтические препараты против рака часто нацеливаются на молекулу CTLA-4, обнаруживаемую на иммунных клетках, чтобы помочь организму атаковать опухоли. Это исследование раскрывает неожиданную деталь: CTLA-4 также встречается внутри самих раковых клеток и может действовать как скрытый помощник роста. Когда учёные целенаправленно удаляли этот внутриклеточный CTLA-4 в меланомных клетках, раковые клетки переставали делиться и входили в длительное «выходное» состояние, известное как клеточное старение. Понимание этой неожиданный роли открывает новые пути для замедления или даже сокращения опухолей за счёт нацеливания CTLA-4 внутри раковых клеток, а не только на иммунных клетках.
Когда клетки выбирают «пенсию» вместо неуправляемого роста
Клетки обычно делятся, восстанавливаются и — при повреждении, превосходящем возможности ремонта — либо погибают, либо входят в состояние сенесценции, постоянной остановки роста. Сенесцентные клетки как правило увеличиваются в размерах, меняют форму и начинают продуцировать специфические маркёры, которые можно обнаружить в лаборатории. Исследователи установили, что при снижении уровня CTLA-4 внутри мышиных и человеческих меланомных клеток они становились крупнее, их пролиферация сильно уменьшалась, а классические признаки старения усиливались, включая ферменты, выявляемые специальными крашениями, и белки p16 и p21, блокирующие клеточный цикл. Эти изменения наблюдались как при временном приглушении CTLA-4, так и при его полном удалении с помощью инструментов редактирования генома.
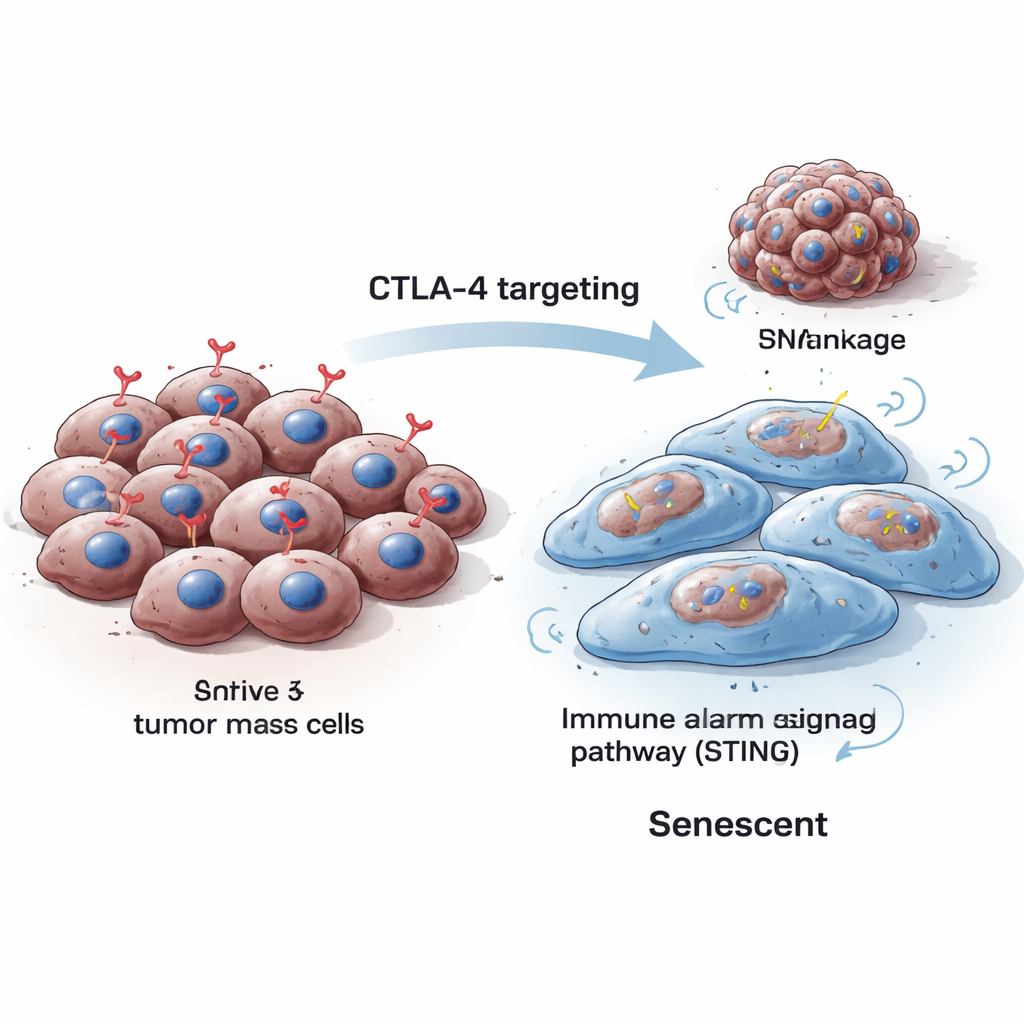
Трещины в генетическом чертеже приводят к остановке
Чтобы понять, почему потеря CTLA-4 переводит раковые клетки в сенесценцию, команды изучили, как эти клетки справляются с ДНК во время деления. Они обнаружили, что истощение CTLA-4 снижает уровни Aurora B — белка, помогающего хромосомам правильно расходиться при делении клеток. При падении Aurora B клетки развивали геномную нестабильность: появлялись крошечные дополнительные ДНК-содержащие структуры, называемые микронуклеусами, и возрастание маркёров повреждения ДНК. Такой тип ДНК-стресса известен тем, что тянет клетки в сторону сенесценции, а не неограниченного роста. Важно, что восстановление Aurora B помогало уменьшить число микронуклеусов, что напрямую связывает потерю CTLA-4 с нарушением обращения с хромосомами и повреждением ДНК.
Повреждение ДНК включает внутреннюю систему сигнализации тревоги
Сломанная и неправильно локализованная ДНК в клетках с пониженным CTLA-4 не оставалась незамеченной. Это активировало DNA-PKcs — сенсор повреждений ДНК, который в свою очередь запустил путь STING, встроенную систему оповещения на присутствие посторонней ДНК внутри клетки. После включения STING передача сигнала шла по вниз по течению, затрагивая молекулы, включая TBK1 и IRF3, а также усиливая ещё один ключевой путь, контролирующий рост — AKT. Вместо стимулирования роста такое сочетание сигналов в итоге повышало уровень p21, мощного тормоза клеточного цикла, укрепляя состояние сенесценции. Когда учёные блокировали DNA-PKcs, активация STING и признаки старения значительно уменьшались, показывая, что DNA-PKcs находится в центре этой цепи оповещения.
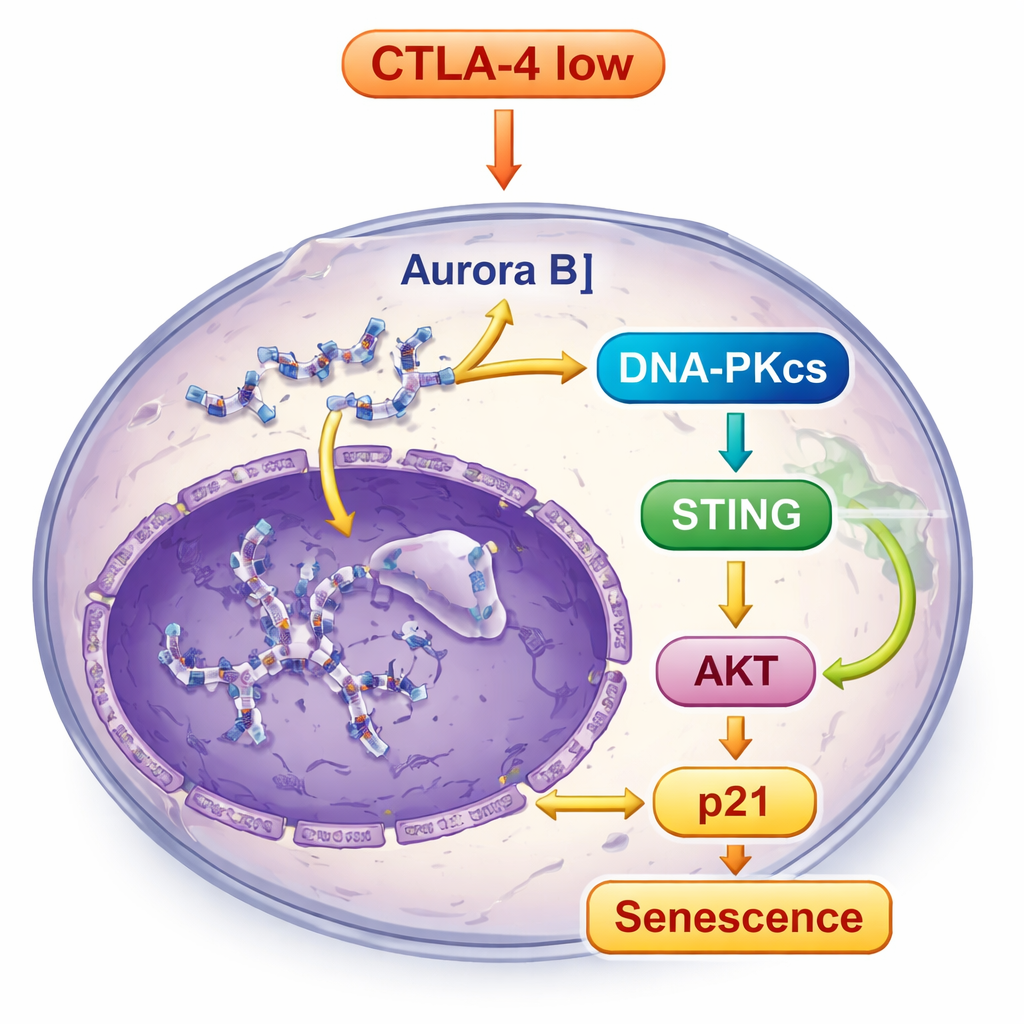
От клеточной культуры до опухолей в живых животных
Сведения из чашек Петри дают лишь часть картины, поэтому исследователи проверили, повлияет ли потеря CTLA-4 на реальные опухоли у мышей. Они имплантировали меланомные клетки с CTLA-4 и без него по разные стороны у одних и тех же животных. Опухоли, лишённые CTLA-4, росли медленнее, имели меньший вес и объём по сравнению с опухолями, содержащими CTLA-4. Эти опухоли с дефицитом CTLA-4 также демонстрировали более выраженные признаки сенесценции и более высокий уровень повреждений ДНК и активации пути STING. Анализ данных пациентов из крупных публичных баз подтвердил связь: в ряде типов рака экспрессия CTLA-4 была склонна коррелировать обратно с DNA-PKcs и другими компонентами системы ремонта ДНК, что перекликалось с лабораторными находками на человеческих образцах.
Что это означает для будущих методов лечения рака
В целом исследование показывает, что CTLA-4 внутри раковых клеток помогает им поддерживать генетическую стабильность и продолжать деление. При удалении CTLA-4 хромосомы становятся нестабильными, накапливаются разрывы ДНК, и внутренняя система тревоги — центрированная вокруг DNA-PKcs и STING — переводит клетки в состояние постоянной остановки роста. Для неспециалиста это означает, что отключение CTLA-4 в опухолевых клетках подталкивает рак от опасного быстрого роста к более безопасному «пенсионному» состоянию. Эти выводы предполагают, что будущие терапии против рака могут разрабатываться не только для разблокирования иммунной системы путём ингибирования CTLA-4 на иммунных клетках, но и для прямого обезвреживания опухолей путём нацеливания CTLA-4 внутри раковых клеток и использования сенесценции как встроенного тормоза роста рака.
Цитирование: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Ключевые слова: клеточное старение, меланома, CTLA-4, повреждение ДНК, путь STING