Clear Sky Science · ru
Шаттлинг TET2 между цитоплазмой и ядром: врожденный тормоз в прогрессировании колоректального рака
Как раковые клетки носят в себе собственный тормоз
Колоректальный рак — одно из самых распространённых злокачественных заболеваний в мире; он часто становится смертельным, когда опухолевые клетки учатся прорастать в соседние ткани и метастазировать в другие органы. В этом исследовании показано, что многие такие клетки на самом деле несут внутри «тормозную систему» — белок TET2, который может замедлять их продвижение, когда локализуется в ядре. Понимание того, как включается и выключается этот встроенный тормоз, может открыть новые способы сдерживать рост опухоли, не сводясь лишь к попыткам напрямую уничтожить раковые клетки.
Наблюдение за перемещением ключевого белка в опухолевых клетках
Учёные сосредоточились на TET2 — белке, который контролирует, какие гены включены или выключены, удаляя определённые химические метки с ДНК. В образцах тканей от сотен пациентов с колоректальным раком они проследили, где именно находится TET2 в опухолевых клетках. Выделили четыре основных паттерна: преимущественно в ядре, преимущественно в цитоплазме или явно смещённый в ту или иную сторону. Пациенты, чьи опухоли содержали больше TET2 в ядре, в целом жили дольше, тогда как у тех, где TET2 оставался в цитоплазме, прогноз был хуже. По мере прогрессирования заболевания ядерный TET2 встречался реже, что указывает на то, что потеря этой ядерной защиты является частью механизма становления опухолей более агрессивными.
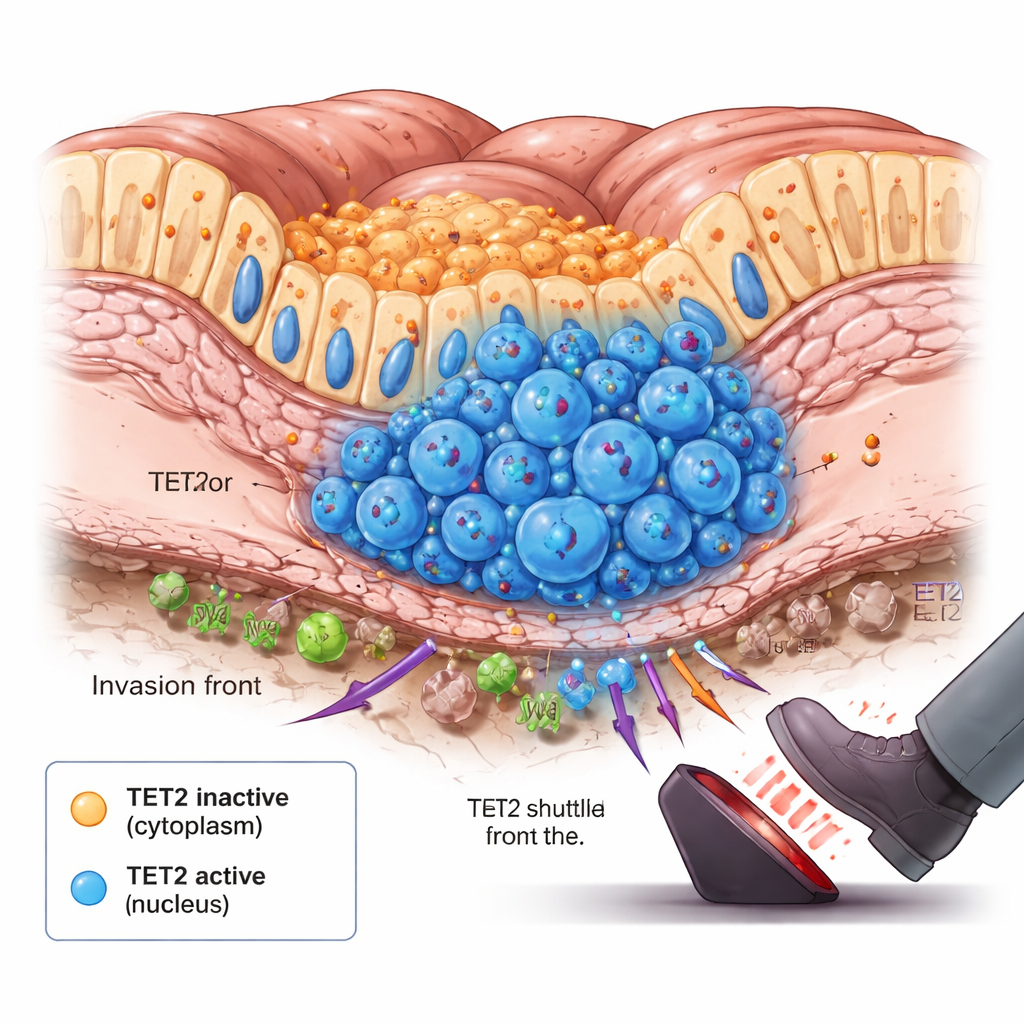
Передовая линия опухоли и момент перемены
Глубже в изучении команда обнаружила неожиданную деталь: в опухолях, которые только начинали распространяться, наблюдалось небольшое увеличение числа клеток с TET2, переместившимся в ядро. Эти клетки скапливались у основания слизистой кишечника, на фронте инвазии, где клетки впервые проникают в более глубокие слои. Эксперименты на животных и длительные культуры клеток, моделирующие рост опухоли, показали аналогичную картину во времени. На ранних этапах TET2 оставался в цитоплазме и был в основном неактивен. По мере роста опухоли и истощения кислорода и питательных веществ в её внутренних зонах внутриклеточные сигналы запускали перемещение TET2 в ядро у определённых субпопуляций. Там TET2 начинал удалять метилирование ДНК и замедлять рост опухоли, действуя как аварийный тормоз при переходе рака критический порог.
Когда «вперёд» сигналы одновременно запускают тормоз
Колоректальные опухоли часто опираются на два мощных «стартовых» механизма: переход эпителиальной клетки в мезенхимальную (EMT), который делает клетки более подвижными и инвазивными, и сигнальный путь WNT, усиливающий рост и выживание. Эти пути обычно рассматривают как исключительно вредные в контексте рака. Однако исследование показывает, что при сильной активации EMT и WNT они также способствуют перемещению TET2 в ядро. С помощью препаратов и генетических инструментов в культурах клеток учёные продемонстрировали, что активация EMT или WNT увеличивает долю клеток с ядерным TET2, а блокирование этих путей даёт обратный эффект. Попав в ядро, активный TET2 затем подавлял связанные с EMT и WNT гены, снижая миграцию клеток и замедляя пролиферацию. Иначе говоря, те же сигналы, которые помогают опухоли расти, одновременно пробуждают внутреннюю противодействующую силу.
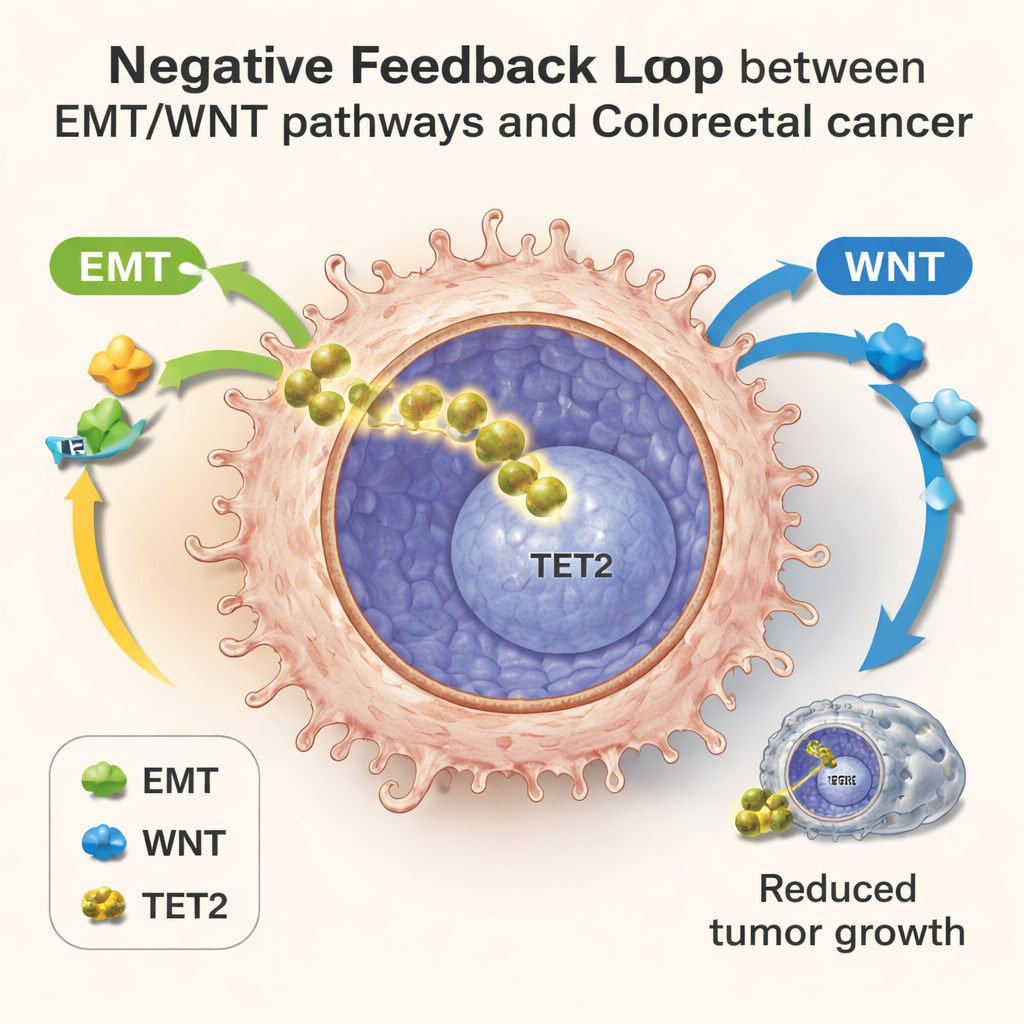
Одиночные клетки выявляют скрытую петлю обратной связи
Чтобы подробно картировать эту борьбу, команда использовала секвенирование РНК на уровне отдельных клеток, позволяющее прочитать набор активных генов в тысячах индивидуальных клеток одновременно. В лабораторно выращенных колониях, в опухолях мышей и в образцах от пациентов с колоректальным раком они наблюдали клетки, распределённые вдоль шкалы прогрессирования. Ранние клетки демонстрировали нормальный метаболизм и слабую активность EMT/WNT; более поздние клетки показывали перестройку метаболизма, сильные EMT/WNT-сигналы и затем повышение экспрессии генов-мишеней TET2. На этих этапах клетки с более высокой активностью TET2 имели более низкие уровни генов, связанных с инвазией, и ассоциировались с лучшими исходами для пациентов, даже среди опухолей, которые уже начали распространяться. Эта картина подтверждает идею отрицательной петли обратной связи: метаболический стресс и активация EMT/WNT продвигают TET2 в ядро, а ядерный TET2, в свою очередь, сдерживает те же агрессивные программы.
Что это значит для будущего лечения рака
Для неспециалистов главный вывод таков: прогрессирование колоректального рака не представляет собой простого переключателя «включено/выключено» между «хорошим» и «плохим» поведением. Вместо этого существует встроенный, отсроченный механизм безопасности: по мере того как опухолевые клетки становятся более инвазивными, они также активируют TET2 в ядрах, что частично их сдерживает. Со временем многие опухоли уходят от этого контроля, теряя ядерный TET2 или преодолевая его эффекты. Найдя способы удерживать TET2 в ядре или усиливать его активность — возможно, в комбинации с препаратами, модулирующими EMT или WNT — клиницисты могли бы укрепить этот природный тормоз и замедлить распространение рака. Вместо того чтобы действовать только извне, будущие терапии могли бы восстанавливать и усиливать эту внутреннюю систему контроля.
Цитирование: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Ключевые слова: колоректальный рак, TET2, эпигенетика, EMT WNT сигнальный путь, прогрессирование рака