Clear Sky Science · ru
Отклонённое поддержание фактора транскрипции развития PAX6 способствует гибели нейронов через сигнальный путь JNK3
Почему это исследование важно для зрения
Глаукома — одна из ведущих причин необратимой слепоты, главным образом потому, что нервные клетки, передающие зрительную информацию от глаза к мозгу, медленно умирают. Многие методы лечения снижают внутриглазное давление, но люди всё равно могут терять зрение, даже если давление хорошо контролируется. В этом исследовании ставится более глубокий вопрос: что заставляет эти клетки сетчатки принять решение о смерти при стрессе и можно ли выключить это решение на уровне генетического управления внутри ядра клетки?
Сетчатка под атакой стресса
В основе глаукомы и родственных заболеваний глаза лежит медленная утрата ганглиозных клеток сетчатки (RGC) — выходных нейронов глаза. Эти клетки уязвимы к разным видам стресса, включая токсические уровни нейромедиатора глутамата, который гиперактивирует NMDA-рецепторы и вызывает повреждающий перегруз кальцием. Исследователи использовали хорошо зарекомендовавшую себя модель на мышах, в которой в глаз вводится небольшое количество NMDA, избирательно повреждающее RGC и при этом в значительной степени не затрагивающее другие слои сетчатки. Они подтвердили, что такое лечение не меняет внутриглазное давление, но вызывает типичные признаки программируемой гибели клеток в RGC, такие как высвобождение цитохрома c из митохондрий и появление TUNEL‑положительных ядер.
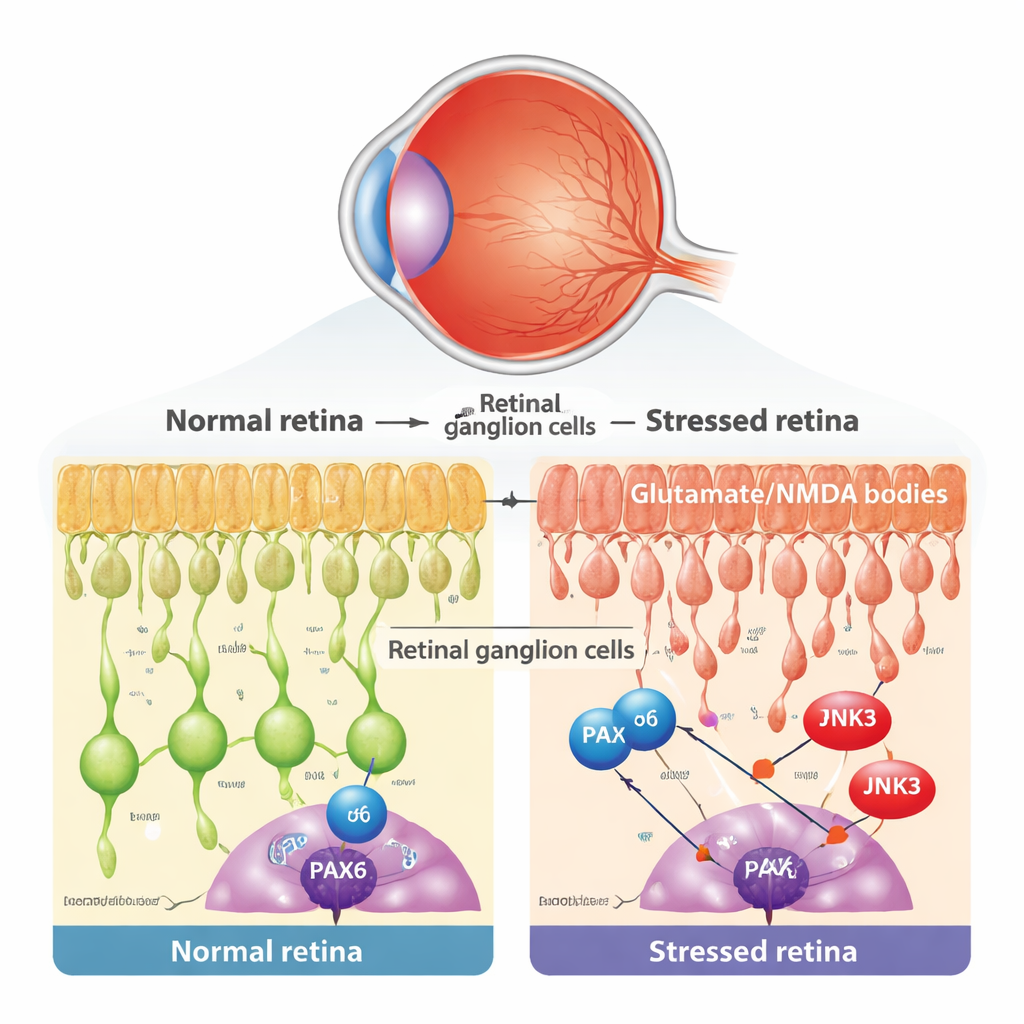
Ген развития, который отказывается на покой
Во время раннего развития регулятор генов PAX6 выступает в роли главного архитектора глаза, направляя формирование и проводку разных клеток сетчатки. Обычно считается, что такие программы развития в основном выключаются во взрослом состоянии. Повторный анализ данных одноядерного/одно-клеточного РНК‑секвенирования сетчатки мыши и человека показал, что PAX6 на самом деле сильно и избирательно сохраняется в зрелых RGC и в некоторых интернейронах. С помощью микроскопической иммуноокраски они показали, что в слое, где располагаются RGC, PAX6 в основном присутствует в ганглиозных клетках, а не в соседних амакриновых клетках. Это породило интригующую гипотезу: во взрослом организме старая программа развития может быть присвоена и превращена в драйвер дегенерации.
От защитника к палачу: PAX6 меняет роль
Чтобы проверить, помогает ли PAX6 выживанию RGC или, наоборот, их гибели при стрессе, учёные применили подход, похожий на генную терапию. Они доставили в сетчатку вирусный вектор, несущий малую РНК, специфически подавляющую PAX6, а затем подвергли глаза воздействию NMDA. По сравнению с контрольными глазами, сетчатки с дефицитом PAX6 показали значительно меньше апоптотических RGC и гораздо меньше митохондриального повреждения, что указывает на то, что PAX6 необходим для полной реализации гибели клеток в этой модели. Геномное РНК‑секвенирование выявило, что многие про‑смертные гены, особенно те, что участвуют в митохондриальном повреждении и активации каспаз, резко индуцировались NMDA у нормальных мышей, но их индукция была ослаблена при молчании PAX6. Иными словами, PAX6 способствует включению сети генов, толкающих RGC за край.
Киназа стресса, переключающая PAX6
Как стресс активирует PAX6, не увеличивая его количество? Команда сосредоточилась на JNK3, стресс‑резponsive ферменте, обнаруженном преимущественно в нейронах. При повреждении NMDA JNK3 переместился в ядро RGC и физически взаимодействовал с PAX6. Биохимические «тестовые трубки» с очищенными белками показали, что JNK3 способен непосредственно добавлять фосфатные метки на PAX6, и эта реакция блокировалась ингибитором JNK. У мышей с нокаутом гена Jnk3 NMDA больше не вызывало тот же паттерн фосфорилирования PAX6. Карта взаимодействия с хроматином (ChIP‑seq) и целевые тесты связывания ДНК показали, что при стрессе фосфорилированный PAX6 вместе с JNK3 сильнее связывается с регуляторными областями ключевых проапоптотических генов, таких как Bax и Gadd45a, усиливая их активность. При подавлении либо PAX6, либо JNK3 это связывание и соответствующая активация про‑смертных генов были резко снижены.
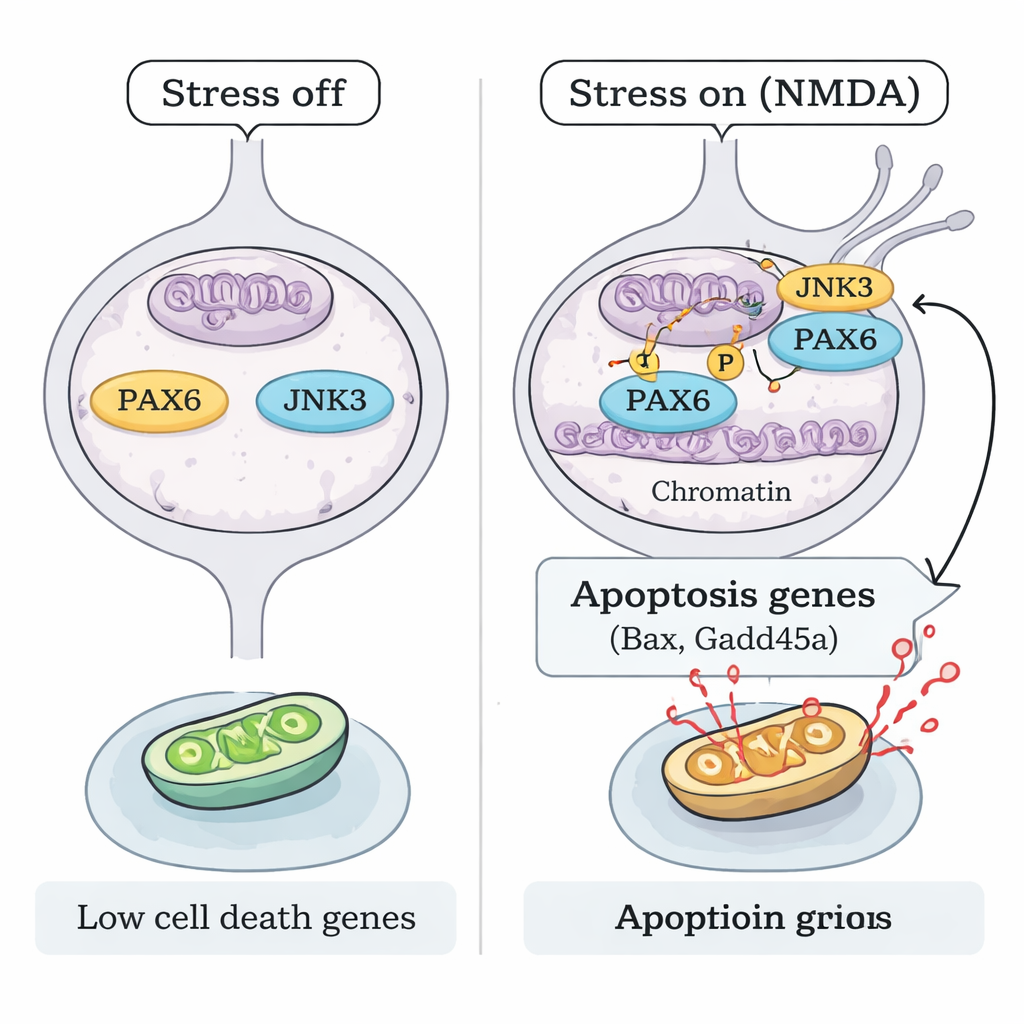
Выключение программы смерти ради сохранения зрения
Наконец, исследователи выяснили, достаточно ли блокирования оси JNK3–PAX6 для защиты клеток, критичных для зрения. Как в мышей с подавлением PAX6, так и у JNK3‑дефицитных животных RGC сохранялись значительно лучше после воздействия NMDA: меньше клеток погибало и структура сетчатки была в более здоровом состоянии. Это указывает на ясную механистическую модель: при экситотоксическом стрессе JNK3 фосфорилирует постоянно экспрессируемый PAX6, превращая его из белка‑строителя развития в мощного активатора программы гибели клеток у взрослых RGC. Прерывание этой связи — путем заглушения PAX6 или отключения JNK3 — сохраняет многие из этих нейронов живыми. Для пациентов эта работа подразумевает, что будущие терапии глаукомы могут выходить за рамки снижения внутриглазного давления и напрямую нацеливаться на генетические переключатели, определяющие, будут ли нейроны сетчатки жить или умирать.
Цитирование: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Ключевые слова: глаукома, ганглиозные клетки сетчатки, PAX6, JNK3, нейродегенерация