Clear Sky Science · ru
Таргетирование ENO1 перепрограммирует поляризацию макрофагов, чтобы вызвать антитуморный иммунитет и улучшает терапевтический эффект радиотерапии
Преобразование опухолевых щитов в мишени
Рак часто выживает не только за счёт быстрого роста, но и за счёт тихого обезвреживания защитных сил организма. В этом исследовании рассматривается скрытый молекула на раковых клетках — ENO1, — которая помогает опухолям ускользать от иммунной системы и сопротивляться радиотерапии. Разработав новое антитело, направленное против ENO1, авторы показывают, что можно осушить опухоль от её защитных химических факторов, «разбудить» иммунные клетки и повысить эффективность облучения в моделях колоректального и тройного-негативного рака молочной железы. 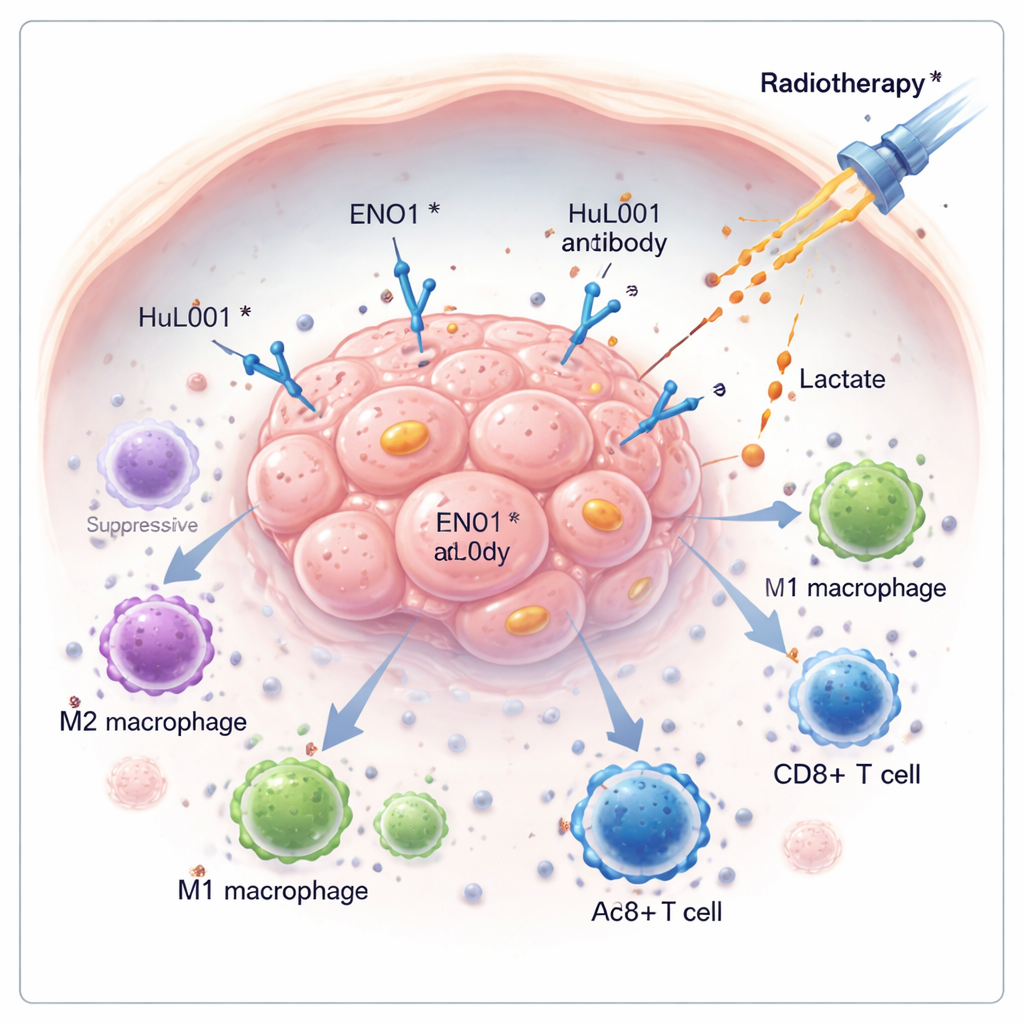
Метаболический трюк, которая заглушает иммунитет
Многие опухоли перепрограммируют использование энергии, расщепляя сахар таким образом, что образуется большое количество молочной кислоты даже при наличии кислорода. Эта молочная кислота выводится из раковых клеток и накапливается вокруг опухоли, превращая окружающую среду в агрессивную, кислую нишу, которая ослабляет иммунную атаку. В работе авторы сосредоточились на ENO1 — ферменте, участвующем в расщеплении сахара, который также может находиться на поверхности раковых клеток. На поверхности клетки ENO1 взаимодействует с другим белком — транспортером MCT4, — чтобы способствовать экспорту лактата, подпитывая среду, благоприятную для роста опухоли и подавляющую иммунные клетки.
Как радиация может сработать во вред
Радиотерапия рассчитана на повреждение ДНК опухоли и запуск иммунных ответов, но она также имеет побочные эффекты в микроокружении опухоли. Команда обнаружила, что сигналы, опосредованные молекулой TGFβ1 и усиливаемые радиацией, активируют фермент PRMT5, который химически модифицирует ENO1 и перемещает его на поверхность раковой клетки. Попав туда, ENO1 физически взаимодействует с MCT4, стабилизирует его и способствует вывозу лактата. Более высокие уровни ENO1 на поверхности обнаруживались у пациентов с прогрессирующим колоректальным и тройным-негативным раком молочной железы и ассоциировались с большим количеством метастазов и худшей выживаемостью, что указывает на то, что радиация может непреднамеренно укреплять лактат-опосредованный иммуноподавляющий «щит» вокруг опухолей.
Перепрограммирование дружественных и враждебных иммунных клеток
В кислой «ореоле» вокруг опухолей иммунные клетки — макрофаги — переводятся в «целительское» состояние (часто называемое M2), которое фактически помогает опухолям, подавляя воспаление и способствуя восстановлению, а не уничтожению раковых клеток. Исследователи создали гуманизированное антитело HuL001, которое распознаёт ENO1 как на мышиных, так и на человеческих раковых клетках. В культурах клеток и мышиных моделях HuL001 нарушало поддержку MCT4 со стороны ENO1, уменьшало выброс лактата и смещало макрофаги из опухоль-поддерживающего состояния M2 в состояние M1, которое более агрессивно по отношению к раку и лучше фагоцитирует опухолевые клетки. Важно, что HuL001 не уничтожало макрофаги; вместо этого оно их перепрограммировало, одновременно напрямую увеличивая гибель раковых клеток.
Усиление действия радиотерапии
Когда HuL001 сочетали с радиотерапией в мышиных моделях колоректального и тройного-негативного рака молочной железы, опухоли сокращались сильнее, повторный рост происходил медленнее, и у многих животных опухоли полностью исчезали. 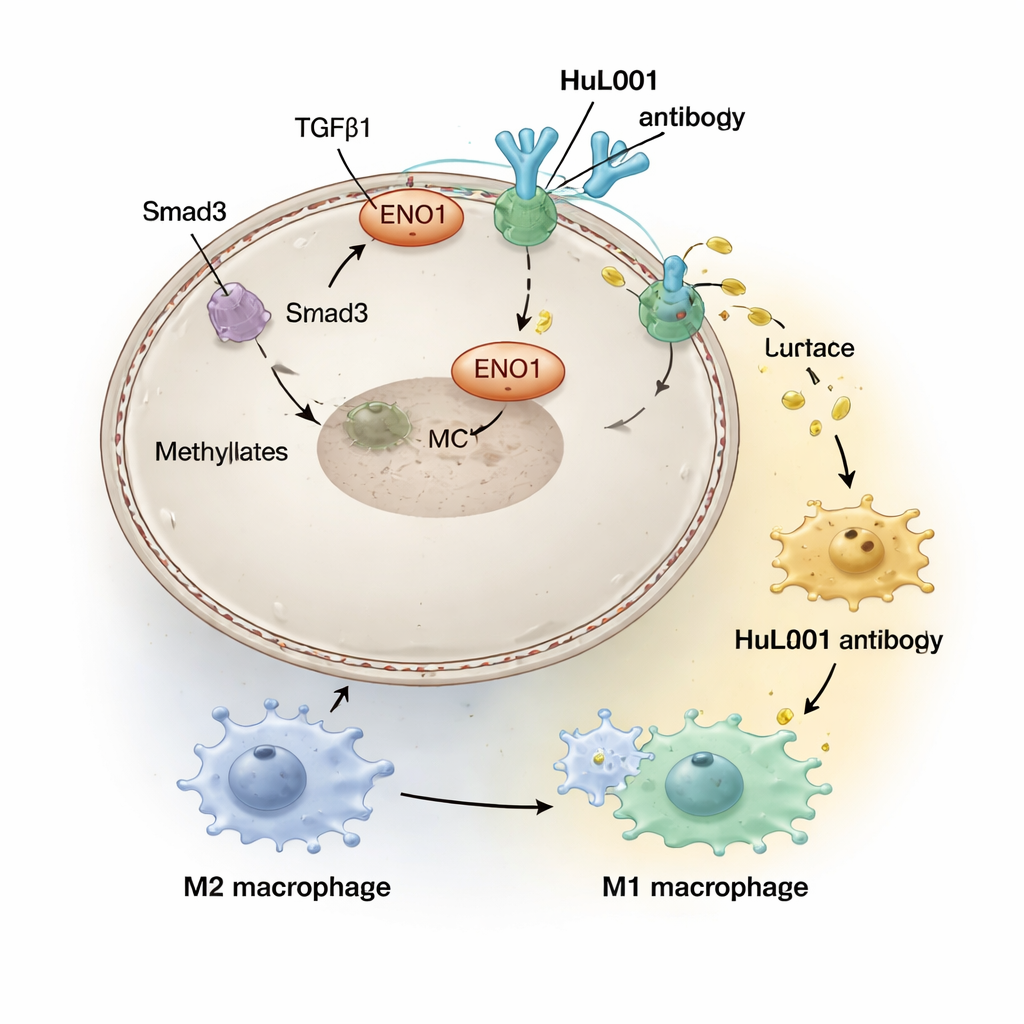
От сложных путей к практическим перспективам
Для неспециалистов главный вывод этого исследования в том, что химия опухоли и её окружение из иммунных клеток тесно взаимосвязаны. ENO1 находится на перекрёстке путей: он помогает опухолям расщеплять сахар, вывозить молочную кислоту и привлекать неподходящую иммунную «помощь». Блокируя поверхностный ENO1 таргетным антителом, исследователи смогли уменьшить вредное накопление лактата, перевести макрофагов из помощников опухоли в её противников и повысить эффективность радиотерапии в трудноизлечимых моделях рака. Хотя HuL001 ещё не является клиническим лекарством, работа указывает на то, что прицельное воздействие на метаболические «шлюзы», такие как ENO1, может стать мощным способом обратить защиту опухоли против неё самой и усилить существующие терапии, включая радиотерапию.
Цитирование: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Ключевые слова: метаболизм опухоли, поляризация макрофагов, радиотерапия, иммунотерапия, лактат