Clear Sky Science · ru
Sec8: новый положительный регулятор RIG-I в защите от РНК-вирусов
Как наши клетки обнаруживают хитрые вирусы
Многие опасные вирусы, включая грипп и вновь возникающие зоонозные вирусы, хранят свой генетический материал в виде РНК. Наши клетки опираются на внутренние системы оповещения, чтобы быстро заметить этих захватчиков и запустить противовирусный ответ. В этой работе исследуют малоизвестный клеточный белок Sec8 и показывают, что он молча играет ключевую роль, поддерживая один из наших основных вирусных датчиков, RIG‑I, живым и активным достаточно долго, чтобы защитить нас.
Клеточная «сигнализация» под угрозой
RIG‑I — молекулярная «сигнализация», патрулирующая внутри клетки в поисках фрагментов вирусной РНК. Когда он обнаруживает подозрительную РНК, он меняет конформацию, активируется и посылает сигналы, которые в итоге запускают выработку интерферонов типа I — мощных молекул‑предупреждений, помогающих соседним клеткам сопротивляться инфекции и активировать иммунные защиты. Поскольку чрезмерно активная сигнализация может вызывать вредное воспаление или аутоиммунные болезни, клетки строго контролируют уровни RIG‑I. Несколько других белков могут помечать RIG‑I для уничтожения, присоединяя к нему короткие цепочки убиквитина, направляя его в клеточный «измельчитель» — протеасому. До сих пор было неясно, какие дополнительные клеточные факторы защищают RIG‑I от преждевременной деградации, особенно во время активной РНК‑вирусной инфекции.
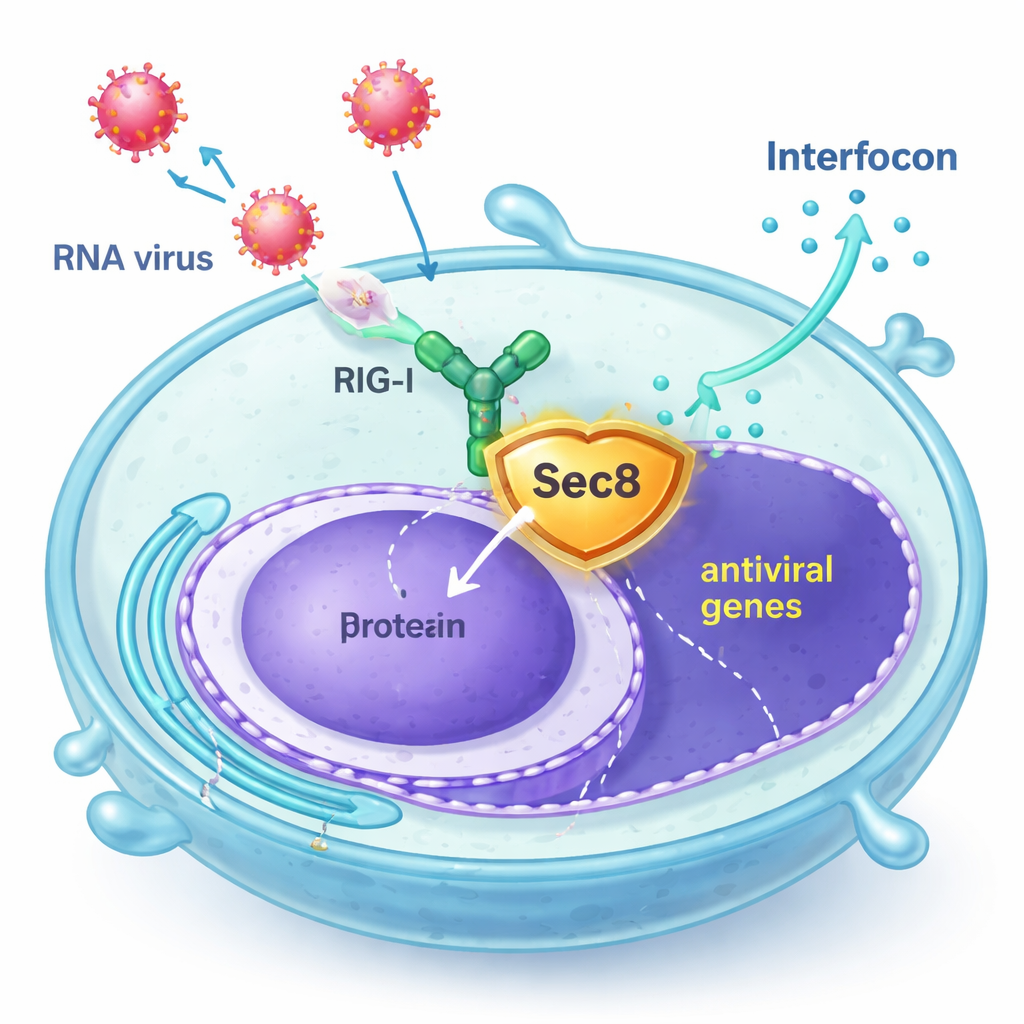
Sec8 вступает в роль телохранителя
Авторы обнаружили, что Sec8, известный прежде всего как часть восьмибелкового комплекса, помогающего секреторным везикулам сливаться с клеточной мембраной, на самом деле усиливает противовирусную сигнализацию. В человеческих клеточных линиях и в первичных иммунных клетках мышей увеличение уровня Sec8 приводило к более сильной активации генов, связанных с интерфероном, после инфицирования РНК‑вирусами, такими как везикулярный стоматитный вирус (VSV) и вирус Сендая, либо после обработки синтетической вирусной РНК. И наоборот, снижение Sec8 уменьшало выработку интерферона и индуцируемых интерфероном генов, делая клетки менее способными сопротивляться репликации вируса. Эти результаты указывают, что Sec8 действует не только в секреции, но и как положительный регулятор в пути противовирусной сигнализации.
Блокирование клеточной «шредерной» машины
Углубив исследование, учёные выяснили, что Sec8 не увеличивает экспрессию гена RIG‑I; вместо этого он предотвращает деградацию белка RIG‑I. При удалении Sec8 уровни RIG‑I падали быстрее, и эту потерю можно было предотвратить препаратами, блокирующими протеасому, что указывает на участие клеточного аппарата утилизации белков. Команда идентифицировала другой белок, STUB1, как ключевого «маркировщика», который присоединяет к RIG‑I специфический тип убиквитиновой цепочки (связи через K48) на остатке лизина 190. Эта метка направляет RIG‑I на разрушение. Sec8 вмешивается в этот процесс двумя способами: он физически конкурирует со STUB1 за связывание с той же активационной областью RIG‑I и снижает количество STUB1, производимого клеткой в целом.
Sec8, p53 и контроль маркировщика
Чтобы объяснить, как Sec8 снижает продукцию STUB1, авторы обратились к регуляции генов. Они выделили короткий участок ДНК, действующий как основной переключатель (промотор) для гена STUB1, и показали, что известный супрессор опухолей p53 связывается с этим регионом и повышает уровни STUB1. Sec8 ослабляет как количество p53, так и его активирующую фосфорилирование, поэтому p53 уже не может столь эффективно стимулировать продукцию STUB1. При блокировании p53 или тишинe STUB1 вредные эффекты потери Sec8 на производство интерферона и рост вируса были в значительной степени обращены. Это помещает Sec8 в вершину регуляторной цепочки, идущей от p53 к STUB1 и, в конце концов, к стабильности RIG‑I.
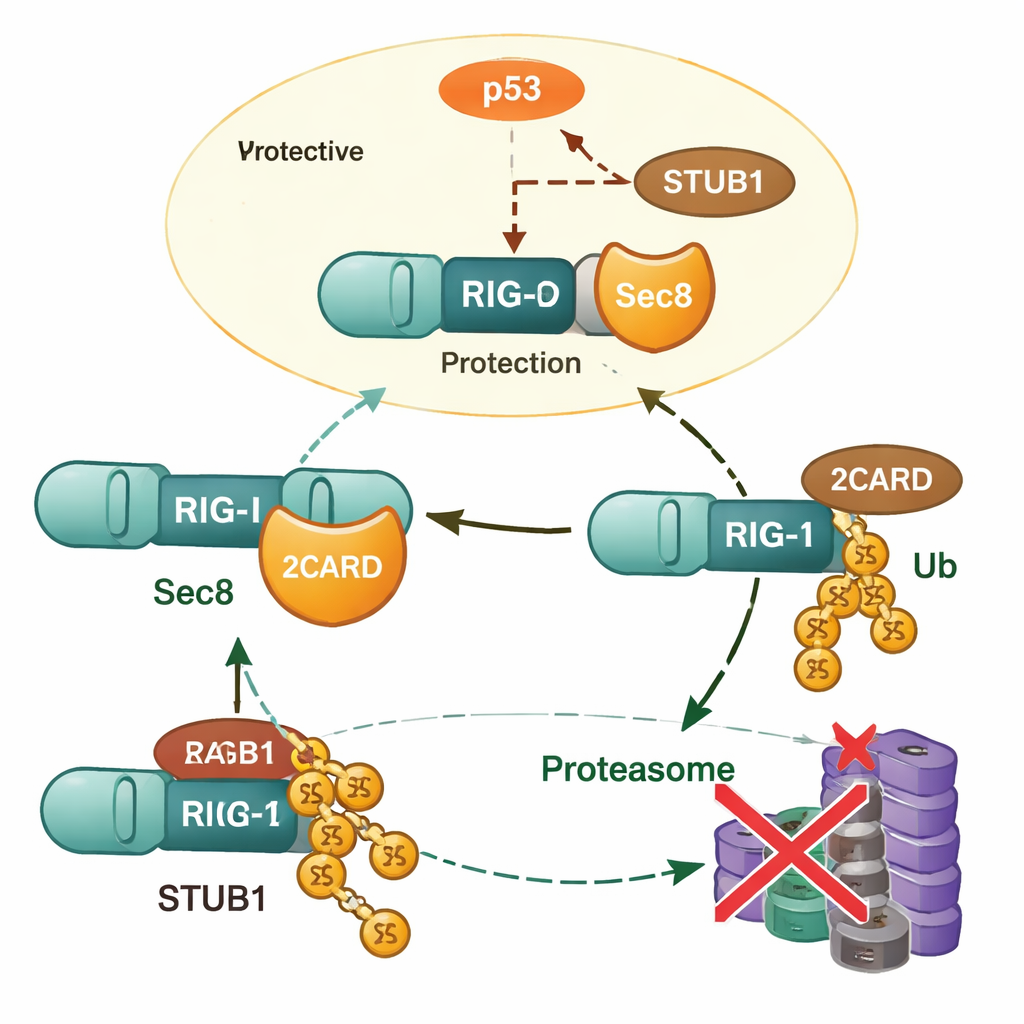
От чашки Петри до живых животных
Затем команда проверила значимость Sec8 на мышах, у которых ген Sec8 был удалён специально в определённых иммунных клетках. После инфицирования VSV эти животные вырабатывали меньше интерферона, несли больше вируса в органах, таких как селезёнка, печень и лёгкие, и демонстрировали более серьёзное повреждение лёгких, большую потерю веса и ниже выживаемость по сравнению с контрольными мышами. Эти результаты in vivo подтвердили, что Sec8 не является второстепенным участником, а представляет собой значимого защитника от РНК‑вирусной инфекции в целом организме.
Почему это важно для будущих терапий
Проще говоря, это исследование показывает, что Sec8 выступает в роли телохранителя для антивирусного сенсора RIG‑I. Поддерживая под контролем «маркировщика» STUB1 и прямо защищая RIG‑I от отправки в клеточный «шредер», Sec8 позволяет клеткам своевременно вызывать интерфероновый ответ и лучше контролировать РНК‑вирусы. Понимание этой недавно описанной оси p53–STUB1–RIG‑I открывает путь к будущим противовирусным стратегиям, направленным на стабилизацию RIG‑I или имитацию защитных действий Sec8, что потенциально усилит нашу защиту против широкого круга РНК‑содержащих вирусных инфекций.
Цитирование: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Ключевые слова: врождённый иммунитет, РНК-вирусы, RIG-I, убиквитинирование, сигнализация интерферона