Clear Sky Science · ru
Передача лактата от гипоксических опухолевых клеток вызывает сенесценцию макрофагов и M2‑поляризацию через ось DNMT1‑NHE7, ускоряя прогрессирование эндометриального рака
Почему важно лишать опухоли кислорода
Эндометриальный рак, возникающий из слизистой оболочки матки, становится всё более распространённым во всём мире. Многие поздние стадии болезни тяжело поддаются лечению: опухоль может рецидивировать, метастазировать или сопротивляться стандартной терапии. В этом исследовании изучают процессы внутри опухолей при дефиците кислорода — частом явлении в быстрорастущих раках — и показывают, как простой метаболит‑отход, лактат, может перепрограммировать соседние иммунные клетки так, что они начинают поддерживать рост опухоли вместо борьбы с ней.
Нехватка кислорода превращает опухоли в фабрики лактата
По мере размножения клеток эндометриального рака кровоснабжение не успевает за ростом, образуя участки с низким содержанием кислорода, или гипоксией. Клетки реагируют включением ключевого регулятора HIF1A, который перестраивает их энергетический обмен. Вместо опоры на более эффективные пути производства энергии клетки усиливают гликолиз — быстрый, но неэффективный процесс, порождающий большие объёмы лактата. Исследователи проанализировали данные опухолей сотен пациентов и обнаружили, что высокий уровень HIF1A коррелировал с повышенной активностью множества генов, связанных с гликолизом, и транспортеров, выкачивающих лактат из раковых клеток. Пациенты с опухолями, где HIF1A был повышен, как правило, имели худший прогноз, что указывает на связь этого метаболического сдвига с агрессивным течением болезни.
Как отходы опухоли перестраивают «полезные» иммунные клетки
Макрофаги — клетки иммунной системы, которые могут либо атаковать опухоль, либо поддерживать её, в зависимости от своего состояния. В работе показано, что при гипоксии клетки эндометриального рака выделяют в окружающую среду значительно больше лактата. Лактат экспортируется из опухолевых клеток через транспортер MCT3 и затем импортируется в макрофаги через другой транспортер, MCT1. Попав внутрь, лактат смещает макрофаги с оборонительного состояния в так называемый M2‑фенотип, связанный с восстановлением тканей, подавлением воспаления и, к сожалению, поддержкой роста опухоли. В лабораторных экспериментах макрофаги, подвергнутые воздействию лактат‑содержащей опухолевой жидкости, проявляли больше маркеров типа M2, а секретируемые ими факторы в свою очередь усиливали рост, подвижность и инвазивность раковых клеток. 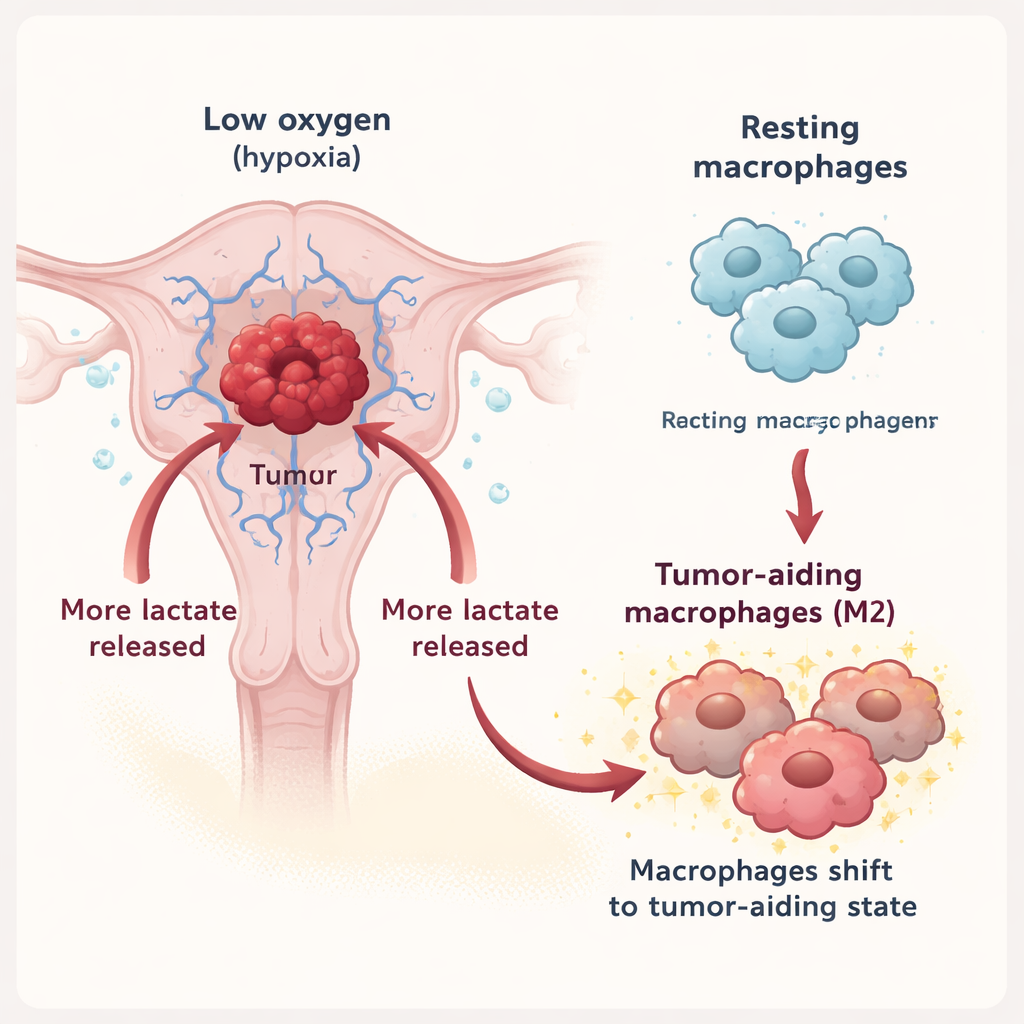
Эпигенетический переключатель, который отключает клеточный «клапан pH»
Исследование шагнуло дальше и выявило молекулярный переключатель в макрофагах, который связывает лактат, происходящий из опухоли, с этим вредоносным поведением. Лактат не просто плавает в цитоплазме; он может модифицировать гистоны в ядре — химическая метка, известная как лактиляция, — и тем самым влиять на включение или выключение генов. Учёные обнаружили, что лактат усиливает конкретную гистонную метку в регуляторной области гена DNMT1, повышая его активность. DNMT1 — фермент, добавляющий метильные группы к ДНК и способный выключать гены. Одной из его мишеней в данном случае оказался NHE7, белок, участвующий в контроле кислотности внутри отдельных клеточных компартментов. При усилении DNMT1 увеличивается метилирование гена NHE7 и его подавление. Снижение NHE7 нарушает внутриклеточный pH и активирует сигнальный путь MAPK. Этот путь, в свою очередь, сдвигает макрофаги в опухоль‑поддерживающее состояние M2 и вызывает их сенесценцию — форму старения, которая фиксирует их в хронически провоспалительном, проопухолевом режиме.
От молекулярной каскадной реакции к более быстрому росту опухолей
Чтобы проверить значимость этой цепочки событий в живых организмах, учёные создали мышиные модели, в которых клетки человеческого эндометриального рака выращивались вместе с макрофагами, имитирующими человеческие. При дополнительной подаче лактата опухоли становились крупнее, содержали больше делящихся клеток и больше макрофагов типа M2 и сенесцентных макрофагов с высоким уровнем DNMT1 и низким уровнем NHE7. Что примечательно, при искусственном переэкспрессировании NHE7 в макрофагах эффект лактата по стимулированию опухолевого роста ослаблялся: опухоли были меньше, в них наблюдалось больше умирающих клеток и меньше M2‑ и сенесцентных макрофагов. Блокирование фермента DNMT1 или пути MAPK также уменьшало способность лактата перепрограммировать макрофаги, подтверждая идею о связанной оси действия этих молекул.
Преобразование уловок опухоли в терапевтические мишени
Для неспециалистов главное послание состоит в том, что эндометриальные опухоли могут использовать гипоксию и лактат — ранее рассматриваемые главным образом как клеточные отходы — чтобы «зомбировать» соседние иммунные клетки и превратить их в помощников рака. Они делают это через эпигенетическую передачу сигнала: лактат усиливает DNMT1, который подавляет NHE7, что запускает сигналы, фиксирующие макрофаги в опухоль‑дружественном, стареющем состоянии. Нарушив любой шаг в этой цепочке лактат–DNMT1–NHE7–MAPK, возможно восстановить противоопухолевую активность иммунитета и замедлить рост рака. Эта работа указывает путь к будущим методам лечения, которые нацелены не только на раковые клетки напрямую, но и на «переобучение» окружающих их иммунных клеток, к которым опухоль приспособилась.»}
Цитирование: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Ключевые слова: эндометриальный рак, опухолевый микроокружение, метаболизм лактата, поляризация макрофагов, эпигенетическая регуляция