Clear Sky Science · ru
За рамками метаболизма: исследование регуляторных и терапевтических последствий лактата и лактиляции при регулируемой гибели клеток в раке
Почему «отход» от расщепления сахара важен при раке
Долгое время лактат — вещество, из‑за которого горят переутомленные мышцы — считали клеточным мусором. В этом обзоре показано, что в контексте рака лактат вовсе не отход. Он служит топливом, химическим сигналом и даже переключателем, который может решать, выживают ли опухолевые клетки или гибнут. Понимание этой скрытой роли может открыть новые пути заставить раковые клетки самоуничтожаться, щадя при этом здоровые ткани.
Сахарная короткая дорога, перестраивающая раковые клетки
Раковые клетки известны своей «сладкоежкой». Даже при достатке кислорода они предпочитают быстро расщеплять глюкозу до лактата вместо полного окисления в митохондриях — явление, известное как эффект Варбурга. Такая стратегия позволяет опухолям быстро получать энергию и компоненты для синтеза. Образующийся поток лактата выкачивается через специальные переносчики, создавая кислую, богатую питательными веществами опухолевую микроокружение, которое поддерживает рост и помогает опухоли адаптироваться к стрессам, таким как гипоксия или химиотерапия.
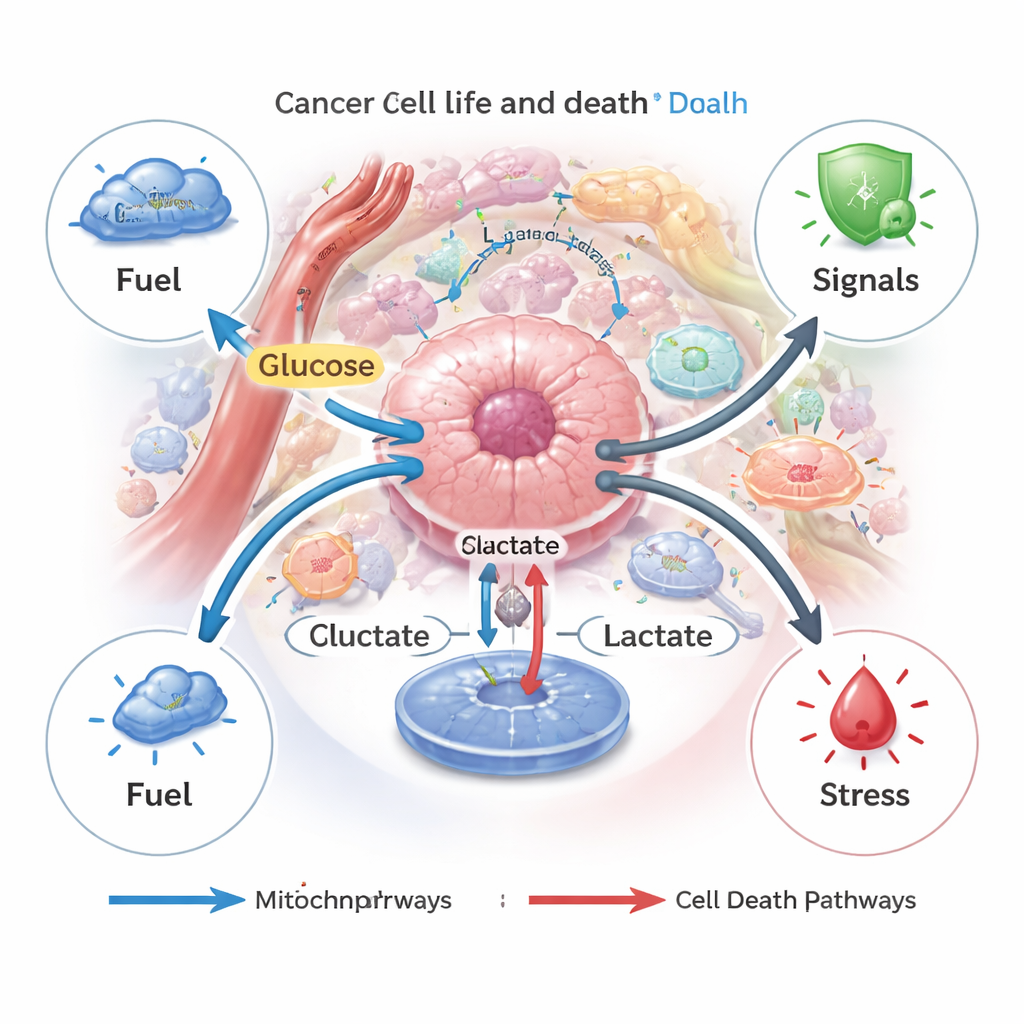
Лактат как регулятор разных видов гибели клеток
Гибель клеток в организме обычно строго контролируется, помогая удалять повреждённые или опасные клетки. Раковые клетки часто уклоняются от этих программ. Авторы описывают, как лактат может как блокировать, так и вызывать несколько регулируемых путей гибели — апоптоз (клеточное «самоубийство»), аутофагию (самопереваривание), ферроптоз (железозависимое повреждение мембран), пиоптоз (воспалительное взрывообразное разрушение) и купроптоз (медно‑зависимый коллапс). Когда раковые клетки генерируют или импортируют умеренные количества лактата, они используют его как топливо и сигнал выживания, включая пути, защищающие от химиотерапии, дефицита питательных веществ или нацеленных препаратов. Но если лактат накапливается внутри клетки, например при блокировке его экспорта, возникший кислотный стресс и повреждение митохондрий могут переключить ситуацию и подтолкнуть клетку к апоптозу или ферроптозу.
Лактиляция: когда лактат «пишет» по белкам
Впечатляющее недавнее открытие заключается в том, что лактат может превращаться в небольшой химический маркер и прикрепляться к остаткам лизина на белках — модификацию, известную как лактиляция. Ферменты выступают в роли «писателей» и «стиралок» этих меток, украшая ими как гистоны, связанные с ДНК, так и многие другие белки. Эти метки меняют, какие гены включаются, как ведут себя ферменты и насколько устойчивы ключевые регуляторы. При раке лактиляция тонко настраивает баланс между выживанием и самоуничтожением. Она может, например, повышать уровень белков, блокирующих апоптоз, усиливать аутофагию, защищать от ферроптоза через более строгий контроль железа и усиление антиоксидантной защиты или модифицировать новые формы гибели, такие как купроптоз, изменяя обращение клеток с медь-чувствительными белками.
Двусторонний разговор между метаболизмом и программами гибели
Взаимосвязь двунаправленная: пути гибели клеток также перестраивают то, как опухоли используют сахар и образуют лактат. Когда митохондрии повреждаются в раннем апоптозе или при митофагии (селективном удалении митохондрий), клетки часто переходят на быстрый гликолиз, повышая выход лактата. Окружающие поддерживающие клетки, например фибробласты, ассоциированные с опухолью, могут претерпевать похожую перестройку и становиться фабриками по производству лактата, подпитывая соседние опухолевые клетки. Другие типы гибели, такие как ферроптоз, как правило, подавляют гликолиз и, следовательно, снижают уровни лактата. В результате возникает динамическая петля обратной связи, в которой метаболизм и механизмы гибели постоянно подстраиваются друг под друга по мере эволюции опухоли и её ответа на лечение.
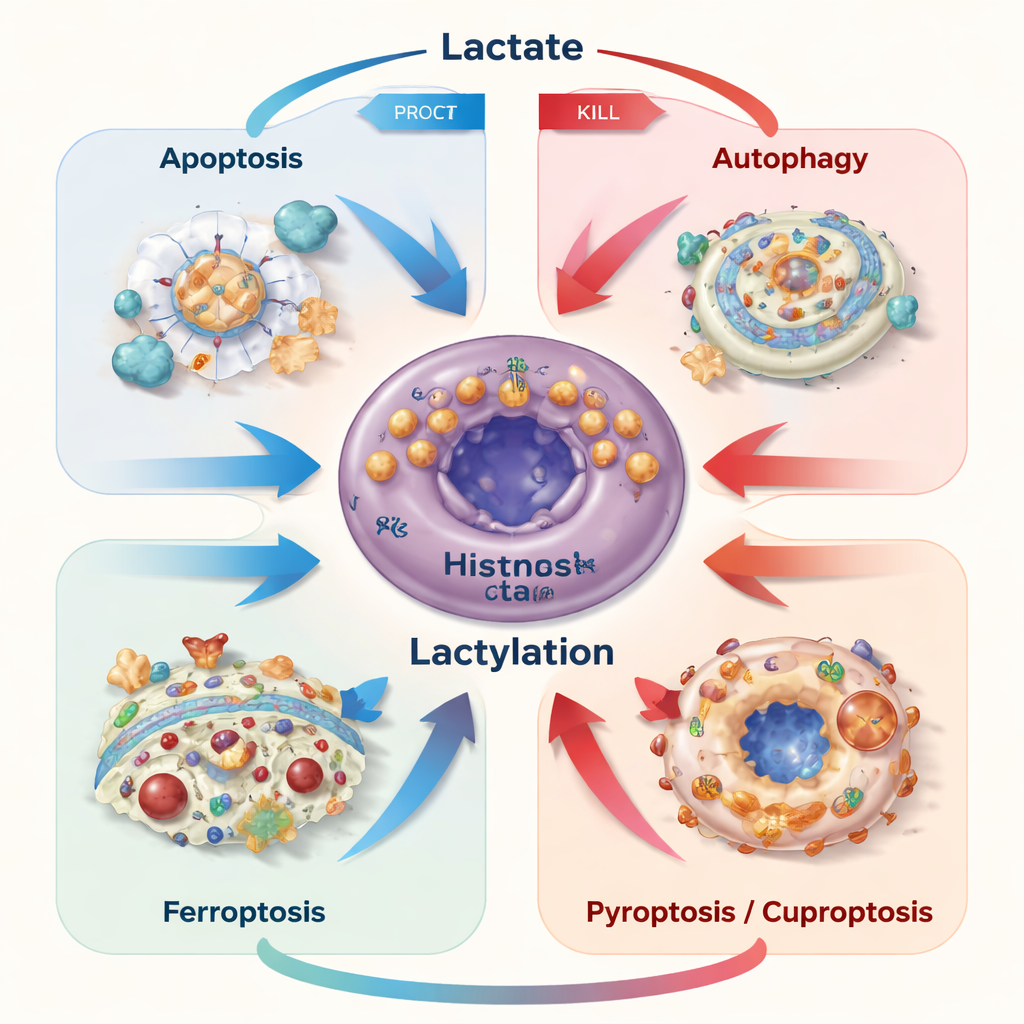
Превращение уязвимости в стратегию лечения
Поскольку лактат и лактиляция в зависимости от контекста могут либо защищать, либо убивать раковые клетки, авторы утверждают, что терапии должны делать больше, чем просто блокировать синтез лактата. Будущие подходы могут избирательно перенаправлять потоки лактата, модифицировать его переносчики или нацеливаться на конкретные метки лактиляции, чтобы подталкивать раковые клетки к гибели, одновременно восстанавливая активность антитуморных иммунных клеток, которые сейчас парализованы кислой средой. Умные системы доставки лекарств и наномедицины, реагирующие на локальные уровни лактата или pH, появляются как способы применить такую точность. Проще говоря, посыл статьи в том, что то, что ранее выглядело как метаболический мусор, на самом деле является мощной ручкой управления судьбой раковых клеток — и умение правильно крутить эту ручку может сделать существующие терапии гораздо эффективнее.
Цитирование: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Ключевые слова: лактат, лактиляция, гибель раковых клеток, метаболизм опухоли, ферроптоз