Clear Sky Science · ru
Иммунный контекст опухоли и уклонение от иммунного ответа при спорадических и ассоциированных с синдромом Линча колоректальных раках с микросателлитной нестабильностью
Почему это важно для пациентов с раком
Иммунотерапия изменила прогноз для многих пациентов с колоректальным раком, но приносит пользу не всем. В этом исследовании поставлен ключевой вопрос: почему одни опухоли, которые теоретически должны быть хорошо заметны для иммунной системы, всё же умудряются её обходить? Сравнивая два типа генетически нестабильных колоректальных опухолей — связанные с наследственным синдромом Линча и возникающие спорадически — авторы выявляют важные различия в том, как иммунные клетки окружают, атакуют или порой защищают эти опухоли.
Два пути к одному типу опухоли
Колоректальные рак с микросателлитной нестабильностью (MSI) содержат большое число ошибок в ДНК, которые создают аномальные белки, действующие как «флаги» для иммунной системы. Такие опухоли могут возникать либо из-за наследственных дефектов в системе репарации ДНК (синдром Линча), либо вследствие изменений, появляющихся только в самой опухоли (спорадические MSI). Хотя оба типа опухолей схожи при микроскопическом исследовании, их иммунное окружение — и, возможно, ответ на лечение — различаются. Авторы собрали 43 MSI-опухоли толстой кишки у финских пациентов, включая случаи, связанные с синдромом Линча, и спорадические, и проанализировали их с помощью тканевого окрашивания, секвенирования целого генома и РНК-секвенирования, чтобы подробно описать, какие иммунные клетки присутствуют и как опухоли избегают уничтожения.
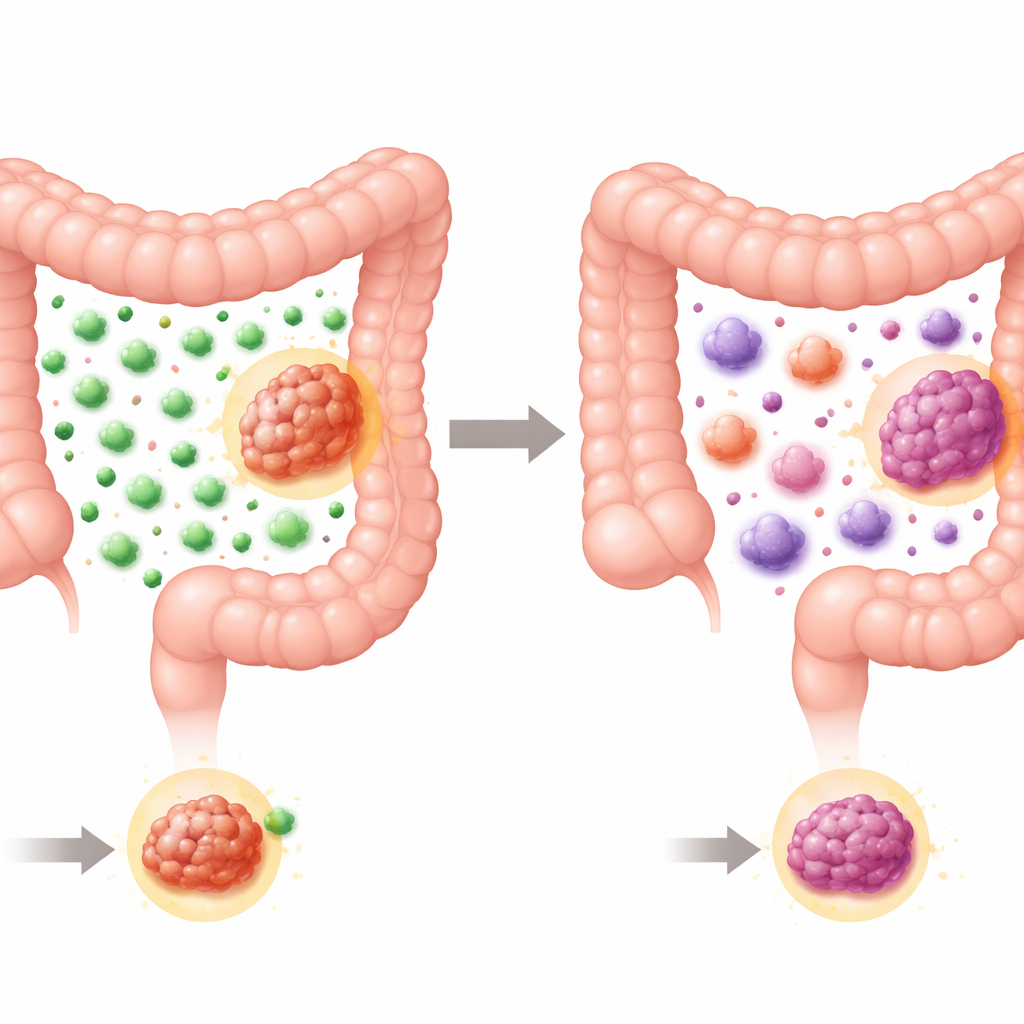
Сколько приходят иммунных клеток
Сначала исследователи сосредоточились на Т-клетках — целенаправленных «убийцах» иммунной системы. Они измерили установленный иммунный балл, который объединяет плотность общей популяции Т-клеток и цитотоксических Т-клеток в центре опухоли и на её инвазивном крае. Как и ожидалось, в целом MSI-опухоли имели более высокие баллы, чем типичные колоректальные раки, что отражает их повышенную способность привлекать Т-клетки. Но при анализе внутри группы MSI выявилась чёткая картина: все опухоли, связанные с синдромом Линча, имели высокий иммунный балл, тогда как спорадические MSI-опухоли разделились примерно пополам между высокими и низкими показателями. Иными словами, наследственные MSI-опухоли почти всегда привлекали мощные армии Т-клеток, тогда как спорадические MSI-опухоли были более разнородны — некоторые выглядели относительно «холодными» для иммунной системы.
Дружественные и враждебные вспомогательные клетки
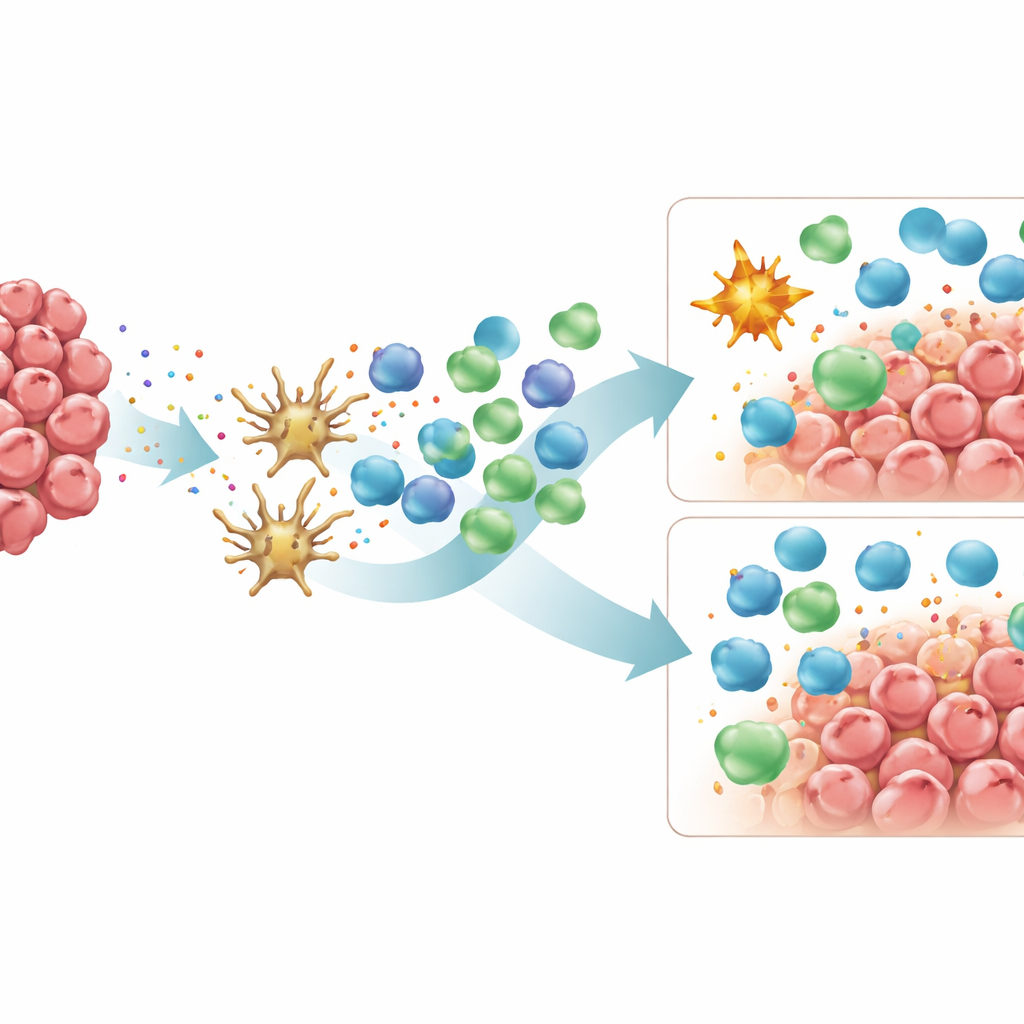
Далее исследование переключилось на миелоидные клетки — клетки врождённого иммунитета, такие как макрофаги и нейтрофилы, которые могут либо помогать Т-клеткам бороться с раком, либо, парадоксально, защищать опухоль. С помощью мультиплексного окрашивания, отмечающего несколько белков одновременно, авторы классифицировали макрофаги на два общих типа: M1-подобные клетки, поддерживающие воспаление и уничтожение опухоли, и M2-подобные клетки, склонные к «успокаивающей», заживляющей функции и часто способствующие росту опухоли. И в опухолях синдрома Линча, и в спорадических MSI встречалось много миелоидных клеток, но спорадические опухоли выделялись большим числом M2-подобных макрофагов, особенно в строме на инвазивном крае опухоли. В этой области M2-подобных клеток в спорадических опухолях даже было больше, чем M1-подобных. Внутри группы спорадических опухолей те, у которых были высокие показатели Т-клеток, также имели больше M1-подобных макрофагов, в то время как уровень M2-подобных оставался высоким независимо от этого — что намекает на то, что баланс между этими двумя типами макрофагов может определять, смогут ли Т-клетки эффективно атаковать опухоль.
Генетические ухищрения и гетерогенность опухоли
Чтобы понять, почему некоторые MSI-опухоли ускользают от иммунной системы, исследователи изучили генетические изменения, влияющие на презентацию антигенов опухолью и на применение «тормозов» иммунного ответа. И в опухолях синдрома Линча, и в спорадических MSI часто встречались мутации в ключевых компонентах механизма презентации антигенов, но различия между группами были лишь незначительными. Более заметными оказались различия в сигналах иммунных «контролей». Спорадические опухоли экспрессировали более высокие уровни PD-L2 и CD40L — молекул, которые могут формировать поведение иммунных клеток и которые всё активнее рассматриваются как мишени для препаратов в комбинации с уже существующими ингибиторами контрольных точек. Авторы также оценивали количество потенциальных неоантигенов в каждой опухоли и степень её генетической однородности или смешанности (клональность против гетерогенности). Удивительно, но более высокий прогнозируемый груз неоантигенов не приводил к увеличению числа Т-клеток. Вместо этого опухоли с большей генетической разнообразностью — особенно спорадические MSI — чаще несли больше неоантигенов, но также демонстрировали признаки, такие как сниженная присутствие нейтрофилов, что указывает на то, что иммунная система не полностью использует эти цели.
Что это значит для будущих методов лечения
В целом исследование описывает MSI-колоректальные опухоли, связанные с синдромом Линча, как последовательно «горячие» опухоли, богатые Т-клетками, тогда как спорадические MSI-опухоли представляют собой более смешанную группу: некоторые сильно инфильтрованы, а другие окружены иммуносупрессивными макрофагами и характеризуются повышенной экспрессией определённых контрольных молекул. Одновременно спорадические опухоли чаще демонстрируют высокую генетическую гетерогенность и большой багаж неоантигенов, распределённых по разным субклональным популяциям опухолевых клеток — паттерн, который, как показывают предыдущие работы, может ослаблять эффективность Т-клеточных ответов. Для пациентов эти выводы помогают объяснить, почему не все MSI-колоректальные раки одинаково хорошо отвечают на иммунотерапию, несмотря на общий высокий уровень мутаций. Они также указывают на новые стратегии, такие как препараты, перенастраивающие или истощающие M2-подобные макрофаги, или терапии, нацеленные на дополнительные контрольные точки, например PD-L2 и CD40L, которые могут быть особенно актуальны для спорадических MSI-опухолей. Лучше подбирая подходы к лечению в соответствии с уникальным иммунным ландшафтом каждой опухоли, клиницисты могут улучшить и персонализировать результаты иммунотерапии при колоректальном раке.
Цитирование: Martin, S., Elomaa, H., Väyrynen, J.P. et al. Tumour immune contexture and immune evasion in sporadic and Lynch syndrome-associated microsatellite unstable colorectal cancers. Br J Cancer 134, 1019–1030 (2026). https://doi.org/10.1038/s41416-025-03302-z
Ключевые слова: колоректальный рак с микросателлитной нестабильностью, синдром Линча, микроокружение опухоли и иммунитет, опухоле-ассоциированные макрофаги, иммунотерапия рака