Clear Sky Science · ru
Функциональные отпечатки дефицита гомологичной рекомбинации в раке простаты, выявленные по фрагментации ctDNA и доступности факторов транскрипции
Почему это важно для пациентов с раком
Многим мужчинам с распространённым раком простаты могли бы помочь препараты, эксплуатирующие уязвимости в механизмах ремонта их опухолевой ДНК. Однако сегодня врачи часто не определяют, кто ответит на лечение, потому что тестирование обычно требует сложных тканевых биопсий и ограничивается лишь несколькими генами. В этом исследовании показано, как простой забор крови можно превратить в богатый многослойный отчёт о таких дефектах репарации ДНК, что потенциально позволит выбирать более точные и щадящие варианты лечения.
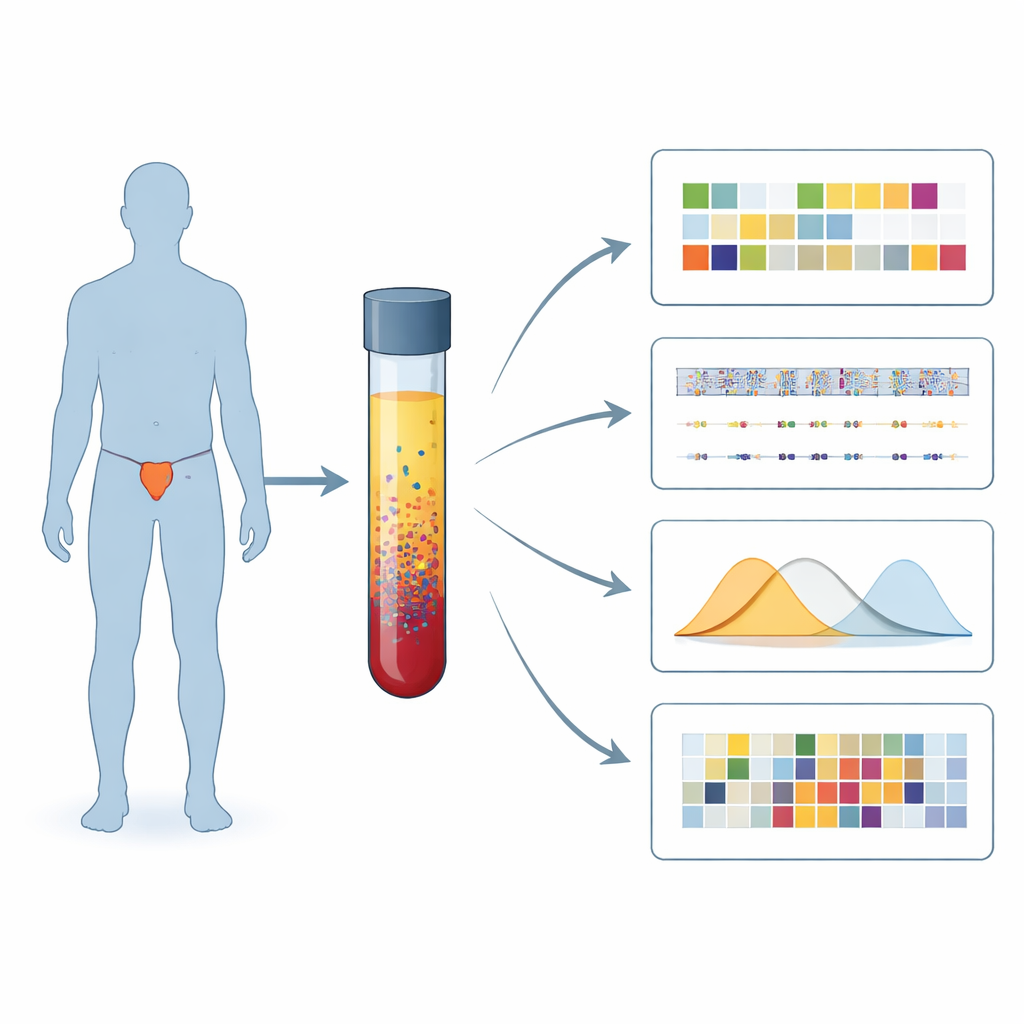
Новый способ считывать сигналы рака из крови
Исследователи сосредоточились на специфической проблеме репарации — дефиците гомологичной рекомбинации (HRD), который делает опухоли особенно уязвимыми к ингибиторам PARP и некоторым химиотерапевтическим препаратам. Вместо того чтобы полагаться на образцы опухоли из кости или предстательной железы, они проанализировали фрагменты опухолевой ДНК, циркулирующей в крови (circulating tumor DNA, ctDNA). Из 375 мужчин с метастатическим раком простаты отобрали 106, в крови которых было достаточно опухолевой ДНК для глубокого изучения, и применили несколько взаимодополняющих тестов к одним и тем же образцам плазмы.
Взгляд за пределы одиночных мутаций
Сначала они секвенировали панель ключевых генов репарации ДНК, включая хорошо известные BRCA2, BRCA1 и PALB2, а также другие гены, влияющие на агрессивность опухолей простаты. BRCA2 оказался наиболее часто изменяющимся геном репарации и часто наблюдался вместе с потерями других важных контролей, таких как PTEN и RB1. Но команда также изучила крупномасштабные изменения структуры хромосом по всему геному, используя низкозатратное секвенирование всего генома для расчёта индекса геномной нестабильности. Опухоли с повреждёнными генами BRCA или с высокими значениями этого индекса имели сильно реаранжированные геномы и ассоциировались с худшей общей выживаемостью, что подчёркивает: крупные структурные изменения могут не уступать в информативности отдельным мутациям.
Отпечатки сбоев репарации в паттернах мутаций
У части пациентов учёные провели более детальное секвенирование всех белок-кодирующих областей, чтобы прочитать тонкую структуру накопившихся со временем мутаций. Определённые комбинации замены оснований и небольших вставок/делеций ведут себя как отпечатки процессов, их породивших. Они обнаружили классические сигнатуры, связанные с HRD — например, SBS3 и индель-паттерн ID6 — которые были обогащены в опухолях с дефектами генов репарации и высокой геномной нестабильностью. Другие сигнатуры указывали на отдельные проблемы, такие как дефекты системы несовпадения (mismatch repair) или особый подтип, обусловленный CDK12, что подчёркивает: разные срывы в репарации ДНК оставляют в геноме отличимые шрамы.
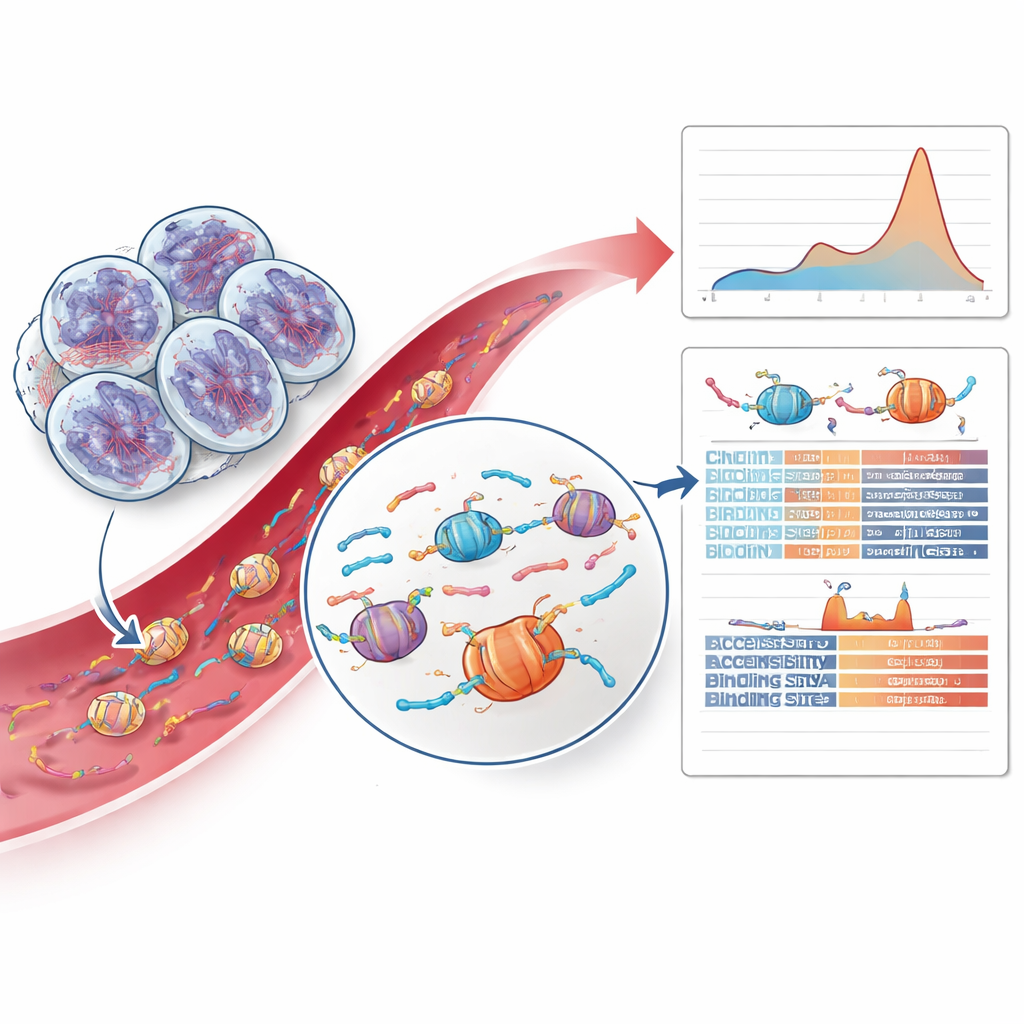
Расшифровка паттернов фрагментов ДНК и хроматиновых подсказок
Самая инновационная часть работы вышла за рамки анализа мутаций и изучила, как именно нарезана опухолевая ДНК на фрагменты. Когда клетки умирают, их ДНК разрезается вокруг белковых упаковок — нуклеосом, образуя фрагменты характерных длин и концевых паттернов. Команда обнаружила, что опухоли с HRD демонстрируют относительный избыток слегка более длинных фрагментов, соответствующих двум нуклеосомам — смещение, не наблюдавшееся у других раков простаты или у здоровых контролей. Обучив осторожную модель машинного обучения на длинах фрагментов и признаках концов фрагментов, они смогли выделять HRD-положительные случаи по одной только крови с обнадеживающей точностью. Также они исследовали доступность различных регионов генома вокруг сайтов связывания факторов транскрипции — белков, контролирующих активность генов — и обнаружили, что некоторые сайты связывания цинковых пальцев менее доступны в HRD-опухолях, что указывает на более глубокие, связанные с репарацией, изменения в организации хроматина.
Что это может означать для пациентов
Вместе эти слои информации — от отдельных генетических мутаций и масштабного перераспределения хромосом до тонких сдвигов в размере фрагментов ДНК и доступности хроматина — формируют более полную картину слабости механизмов ремонта ДНК при раке простаты. Для неспециалиста главный вывод таков: тщательно проанализированная проба крови может показать не только наличие мутации в знакомом гене, например BRCA2, но и то, ведёт ли опухоль себя так, будто у неё серьёзный дефект репарации, даже если обычные тесты кажутся нормальными. Если этот многомодальный подход на основе крови подтвердится в крупных и более разнообразных группах пациентов, он может помочь врачам надёжнее отбирать пациентов, которые с большой вероятностью получат пользу от ингибиторов PARP или платиновых препаратов, отслеживать изменения со временем и в конечном итоге персонализировать терапию при помощи простого и повторяемого теста.
Цитирование: Vlachos, G., Moser, T., Lazzeri, I. et al. Functional footprints of homologous recombination deficiency in prostate cancer revealed by ctDNA fragmentation and transcription factor accessibility. Br J Cancer 134, 949–960 (2026). https://doi.org/10.1038/s41416-025-03301-0
Ключевые слова: рак простаты, жидкостная биопсия, репарация ДНК, циркулирующая опухолевая ДНК, ингибиторы PARP