Clear Sky Science · ru
Спектр и функции ионных каналов и переносчиков в остеокластах
Почему нашим костям нужны крошечные привратники
Наш скелет кажется прочным и неизменным, но он постоянно разрушается и восстанавливается. Специализированные клетки — остеокласты — выполняют роль бригады сноса, растворяя старую кость, чтобы на её месте могла образоваться новая. В этом обзорном материале рассматривается скрытый ансамбль микроскопических «привратников» — ионных каналов и переносчиков — которые пропускают заряженные атомы и питательные вещества внутрь и наружу остеокластов. Поняв, как эти крошечные ворота контролируют распад кости, учёные надеются разработать лучшие методы лечения остеопороза и других заболеваний костной ткани.
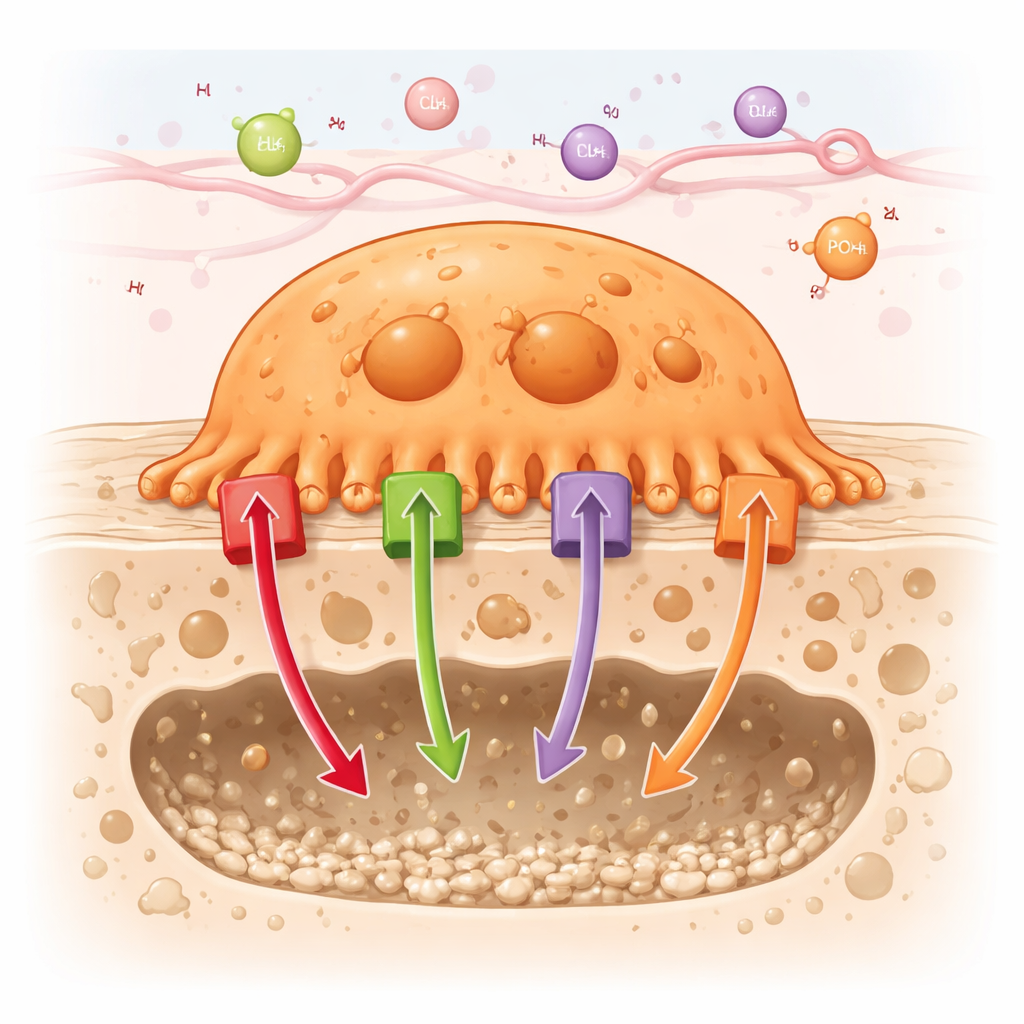
Как «поедатели кости» выполняют свою работу
Остеокласты действуют, плотно прилегая к поверхности кости и создавая изолированный отсек, где они могут безопасно растворять минерал и переваривать белки. Чтобы сделать эту миниатюрную «камера переваривания» крайне кислой, остеокласты перекачивают большое число протонов (ионов водорода) в отсек. Одновременно они транспортируют другие ионы — такие как хлорид, кальций и фосфат — через плазменную мембрану и внутриклеточные компартменты. В статье рассматривается около 90 различных каналов и переносчиков, обнаруженных в остеокластах, и группируется их по шести семьям, включая энергодвижимые насосы (АТФазы), катионные и анионные каналы, сопряжённые переносчики, носители питательных веществ и переносчики семейства ABC.
Кислота, соль и энергия: основная техника
Две белковые системы выделяются как центральные для резорбции кости. Во‑первых, везикулярные протонные насосы, известные как V‑ATPase, активно закачивают протоны в ресорбционный отсек, делая его достаточно кислым для растворения минерального матрикса кости и активации протеолитических ферментов. Определённые субъединицы V‑ATPase, такие как a3, d2 и некоторые компоненты V1, обогащены на ворсистом крае остеокласта и в лизосомах; генетические дефекты в этих субъединицах могут ослаблять кость или вызывать аномальное утолщение кости. Во‑вторых, обменник хлорид–протон ClC‑7, который взаимодействует с белком OSTM1, вносит ионы хлора в ту же область. Это уравновешивает электрический заряд и позволяет непрерывной перекачке протонов продолжаться. Мутации ClC‑7 у людей и мышей приводят к остеопетрозу — заболеванию, характеризующемуся избыточной плотностью, но хрупкостью кости, — что демонстрирует, насколько важен правильный ионный поток для нормального состояния скелета.
Кальций, фосфат и другие поддерживающие игроки
Помимо производства кислоты, остеокласты зависят от тонко настроенного обращения кальция и фосфата. Сеть кальциевых каналов и насосов в плазматической мембране, эндоплазматическом ретикулуме, лизосомах и митохондриях создаёт ритмические колебания кальция, которые включают ключевые гены, отвечающие за образование и слияние остеокластов. Транспортёры на ворсистом крае и на противоположной стороне клетки перемещают кальций и фосфат из растворённой кости, либо перерабатывая их внутри клетки, либо возвращая в кровоток. Другие металлы и минералы — такие как марганец, магний, цинк, медь и железо — также регулируются специализированными переносчиками и влияют на интенсивность резорбции. Например, железо и определённые формы гибели клеток, связанные с железом, могут усиливать или ослаблять активность остеокластов, тогда как цинковые переносчики, как правило, сдерживают чрезмерную потерю кости.
Регулирование движения внутри клетки
Ионные каналы не ограничены только наружной мембраной. Многие располагаются на внутренних компартментах, таких как лизосомы, эндосомы, аппарат Гольджи и митохондрии, создавая многоуровневую транспортную сеть. Эти внутренние ворота помогают устанавливать pH в пищеварительных везикулах, обеспечивать производство энергии в митохондриях и управлять перемещением ферментов и остатков. В обзоре подчёркивается, как несколько систем каналов работают согласованно: натрий‑водородные обменники регулируют внутреннюю кислотность, калий‑хлоридные котранспортеры помогают поддерживать мембранный потенциал и баланс хлора, а пуринергические и механочувствительные каналы превращают химические или механические сигналы в изменения резорбции кости. Транспортёры питательных веществ для глюкозы, аминокислот, нуклеозидов и витамина C дополнительно поддерживают высокий энергетический и биосинтетический спрос активно резорбирующих остеокластов.
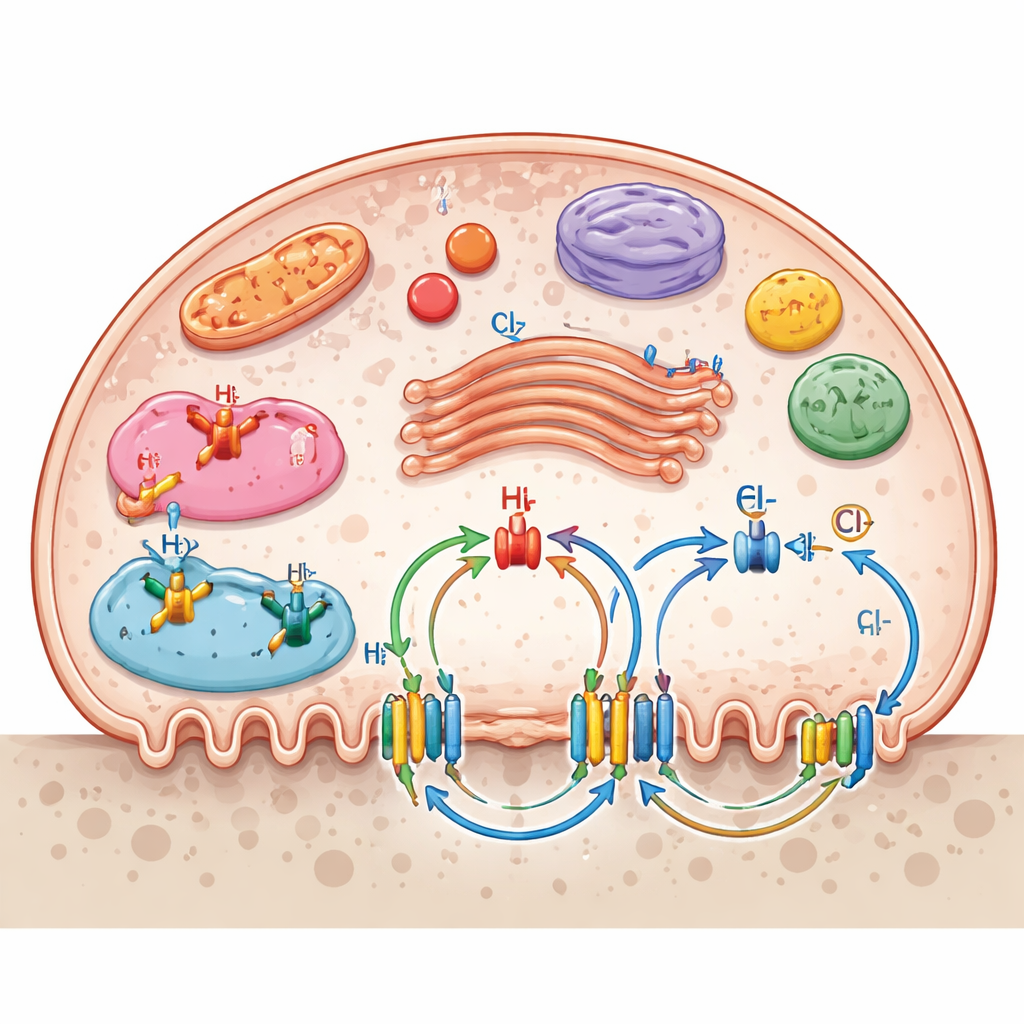
От базовой биологии к новым методам лечения
Поскольку многие заболевания кости возникают, когда остеокласты становятся либо сверхактивными, либо недостаточно активными, каналы и переносчики, задающие их поведение, представляют собой привлекательные лекарственные мишени. Авторы обзорной статьи рассматривают существующие и экспериментальные соединения, блокирующие V‑ATPase, кальциевые каналы TRP, хлоридные обменники, пуринергические рецепторы и другие переносчики, а также новые подходы, такие как разрушение специфических взаимодействий субъединиц или использование таргетных наночастиц для доставки препаратов прямо к кости. Они подчёркивают, что многие из этих белков также встречаются в других тканях, поэтому достижение истинной специфичности для остеокластов остаётся задачей. Тем не менее по мере того как геномные и визуализационные инструменты выявляют больше данных о локализации этих каналов и их взаимодействиях, расширяющаяся «ионная карта» остеокластов, вероятно, приведёт к более точным терапиям при остеопорозе, воспалительной потере кости и редких генетических заболеваниях скелета.
Цитирование: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Ключевые слова: остеокласты, ионные каналы, резорбция кости, V-ATPase, остеопороз