Clear Sky Science · ru
PRMT6 необходим для инициации и усиления макрофаг-индуцированного воспаления при гетеротопическом окостенении за счёт повышения экспрессии CCL2
Когда заживление заходит слишком далеко
Иногда после тяжелой травмы или операции организм старается восстановиться настолько активно, что начинает формировать кость там, где ей не место. Это болезненное состояние — нежелательный рост кости в мягких тканях — может ограничивать подвижность суставов, осложнять ампутации и затруднять повседневные движения. Существующие методы лечения ограничены и часто не предотвращают рецидив. В этом исследовании выявлен ключевой ранний переключатель в иммунной системе, который связывает травму с этим аномальным образованием кости, и показан короткий, но решающий временной интервал, когда целевое вмешательство может остановить процесс до его разгона. 
Проблема кости не в том месте
После тяжёлой травмы, например ожогов, переломов или ортопедических операций, у некоторых пациентов внутри мышц, сухожилий и других мягких тканей образуются островки кости. Новая кость формируется через процесс, схожий с нормальным остеогенезом: он начинается с воспаления и заканчивается зрелой минерализованной тканью. Врачи знают, что центральную роль в этом процессе играют иммунные клетки — макрофаги, однако поэтапный механизм их запуска и поддержания воспаления оставался неясным. Без этого знания такие терапии, как противовоспалительные препараты, облучение или позднее хирургическое удаление, в основном устраняют последствия, а не причину, поэтому рецидивы часты.
Ключевой посредник воспаления
Используя модель на мышах, сочетающую повреждение сухожилия с ожогом — что близко имитирует тяжёлую травму у людей — исследователи проследили развитие событий в месте травмы с течением времени. Они наблюдали быстрый приток макрофагов в первые дни после повреждения, которые затем сохранялись по мере формирования аномальной кости. При истощении этих клеток лишняя кость почти исчезала, а окружающие ткани демонстрировали гораздо меньше нарушения кровоснабжения и поддерживающих клеток. Глубокий анализ экспрессии генов в повреждённой ткани выделил одну молекулу в макрофагах: PRMT6 — фермент, который модифицирует белки и помогает управлять включением генов.
Молекулярная ручка громкости для воспаления
Команда обнаружила, что уровни PRMT6 в макрофагах быстро повышаются после травмы и в ответ на сигналы опасности и бактериальные компоненты в лабораторных условиях. У мышей без PRMT6 или у животных, у которых PRMT6 был избирательно уменьшен только в макрофагах, в месте повреждения оказалось значительно меньше макрофагов, и аномальная кость развивалась гораздо слабее. Важно, что повреждённые сухожилия у этих животных заживали даже лучше — с более упорядоченной тканью и меньшим образованием рубца. Это указывает на то, что PRMT6 не обязателен для здорового заживления, а действует как ручка громкости, усиливающая вредное воспаление. Блокада PRMT6 с помощью препарата была эффективна только при раннем введении — в течение первых недель после травмы. Поздний старт лечения имел мало эффекта, что подчёркивает узкое, но мощное терапевтическое окно. 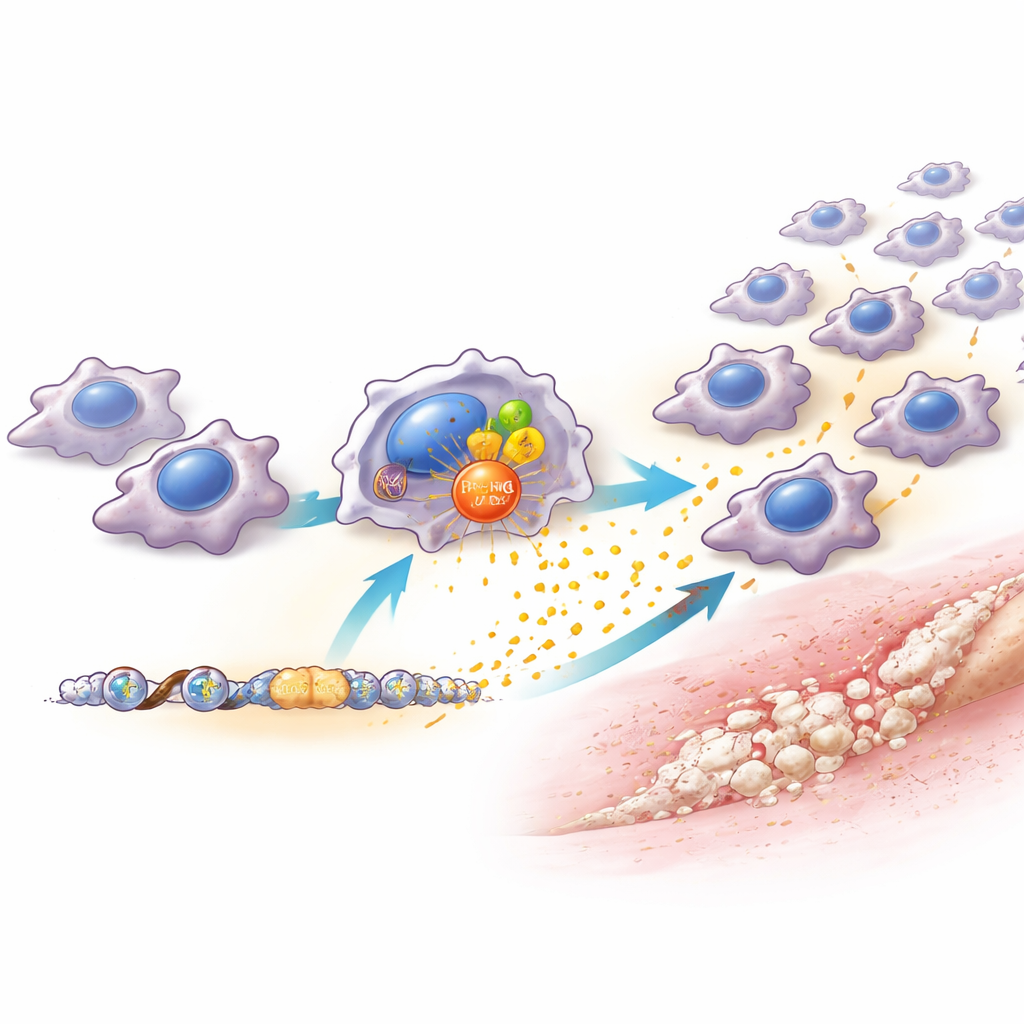
Как один сигнал привлекает множество иммунных клеток
Чтобы понять, как PRMT6 реализует своё действие, учёные подробно изучили макрофаги. При отсутствии PRMT6 эти клетки вырабатывали значительно меньшие количества нескольких хемокинов, особенно одного, названного CCL2, который обычно привлекает моноциты и макрофаги из кровотока в повреждённую ткань. PRMT6 способствует включению гена CCL2 двояко: он взаимодействует с известным регулятором воспаления NF-κB и химически помечает соседние белки, упаковывающие ДНК, делая ген более доступным для чтения. В результате макрофаги с высоким уровнем PRMT6 продуцируют больше CCL2, притягивая дополнительные макрофаги и формируя «центр воспаления», который поддерживает рост кровеносных сосудов и клетки-предшественники, дающие начало кости. При специфическом снижении CCL2 только в макрофагах исход оказался схожим с потерей PRMT6 — меньше макрофагов, ослабленные воспалительные нишы и меньше лишней кости. Восстановление CCL2 частично вернуло приток макрофагов и аномальное образование кости.
Целенаправленный шанс предотвратить нежелательную кость
В совокупности исследование показывает, что PRMT6 в макрофагах действует как ранний эпигенетический усилитель: он повышает ключевой химический сигнал, рекрутирующий больше иммунных клеток, что, в свою очередь, приводит к образованию кости в неподходящем месте. Поскольку блокада PRMT6 только на ранней фазе воспаления резко снижала нежелательное окостенение, при этом не нарушая нормального заживления сухожилий и даже улучшая организацию ткани, этот путь предлагает перспективную новую стратегию. В принципе, короткий, правильно вовремя начатый курс терапии, направленной против PRMT6 после крупной травмы или операции, мог бы предотвратить долгосрочную инвалидность от эктопической кости, не нарушая при этом естественной способности организма к восстановлению.
Цитирование: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Ключевые слова: гетеротопическое окостенение, макрофаги, воспаление, эпигенетическая регуляция, сигнализация CCL2