Clear Sky Science · ru
C/EBPβ регулирует транскрипцию FSHβ после менопаузы, а блокада пути AEP/C/EBPβ облегчает остеопороз
Почему это исследование важно для жизни после менопаузы
Многим женщинам говорят, что снижение эстрогена — главная причина хрупких костей после менопаузы. Это исследование добавляет новый фрагмент к картине: другой гормон, фолликулостимулирующий гормон (FSH), и пара белков в мозге и кости — C/EBPβ и AEP — действуют совместно, ускоряя потерю костной массы. Еще более интригующе, что исследователи показали на мышах: блокада этого пути экспериментальной таблеткой может защищать кости так же эффективно, как одобренный препарат от остеопороза.
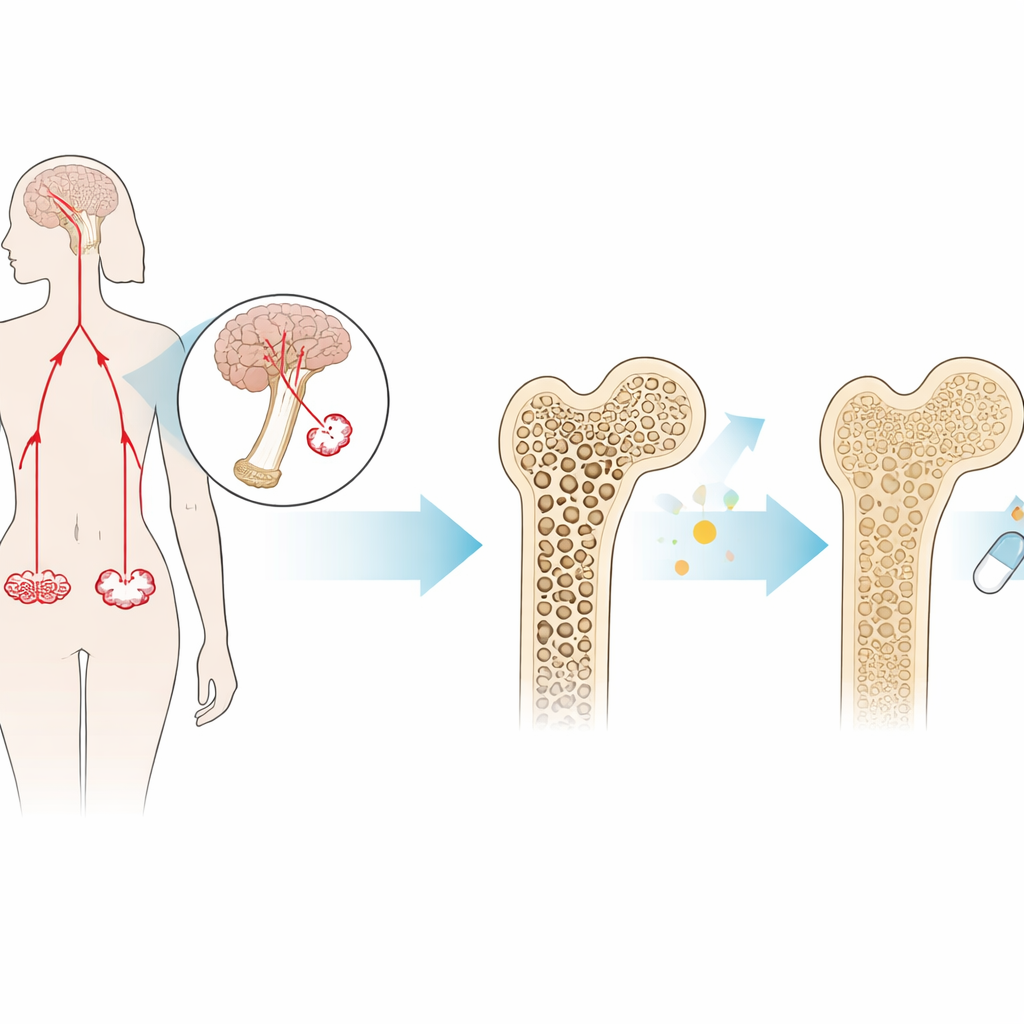
Менее известный гормон с большим влиянием на кость
FSH вырабатывается в гипофизе и наиболее известен своей ролью в фертильности. У женщин, приближающихся к менопаузе, уровни FSH резко повышаются за несколько лет до последней менструации. Помимо репродуктивной функции, FSH может действовать прямо на кость: он связывается с рецепторами на клетках, разрушающих костную ткань (остеокластах), стимулируя их разрушительную активность быстрее, чем кость восстанавливается. Предыдущие работы показали, что мыши, лишенные FSH или его рецептора, защищены от потери костной массы, даже при низком уровне эстрогена. Это указывало на то, что сам FSH, а не только дефицит эстрогена, способен вызывать постменопаузальный остеопороз.
Переключатель в гипофизе
Новое исследование сосредоточено на C/EBPβ, белке, который связывается с ДНК и включает или выключает гены. Авторы обнаружили, что C/EBPβ напрямую связывается с регуляторной областью гена бета-субъединицы FSH — части гормона, определяющей его идентичность — и усиливает его продукцию в гипофизе. В культуре гипофизарных клеток усиление экспрессии C/EBPβ увеличивало уровни FSH, тогда как подавление C/EBPβ снижало FSH, особенно при стимуляции клеток репродуктивным сигналом из мозга, GnRH. У овариэктомированных мышей, моделирующих менопаузу путем удаления яичников, животные с пониженным C/EBPβ вырабатывали значительно меньше FSH в гипофизе и крови. Эти эксперименты выявляют C/EBPβ как ключевой переключатель, определяющий силу подъема FSH после падения эстрогена.
Самоподдерживающаяся петля и новая мишень для лекарств
C/EBPβ также контролирует другой белок — AEP, протеазу, способную активировать или инактивировать другие молекулы. В мозге цепочка C/EBPβ–AEP связывалась с повреждениями, похожими на альцгеймеровские. Здесь команда проверила, не влияет ли та же цепочка на FSH и кость. У мышей без AEP уровни как C/EBPβ, так и FSH в гипофизе снижались, и потеря костной массы после удаления яичников уменьшалась. Блокада AEP малой молекулой под названием #11a дала схожий эффект: после месячной терапии овариэктомированные мыши имели пониженный FSH, более прочные кости при высокоразрешающем сканировании и меньше гиперактивных остеокластов. Другой класс соединений — активаторы TrkB, которые косвенно подавляют AEP — помогали клеткам кости в культурах, но не снижали FSH у животных, отчасти потому, что их целевой рецептор мало представлен в гипофизе. Это различие укрепляет вывод, что прямая ингибиция AEP — более мощный способ выключить ось C/EBPβ–FSH у её источника.
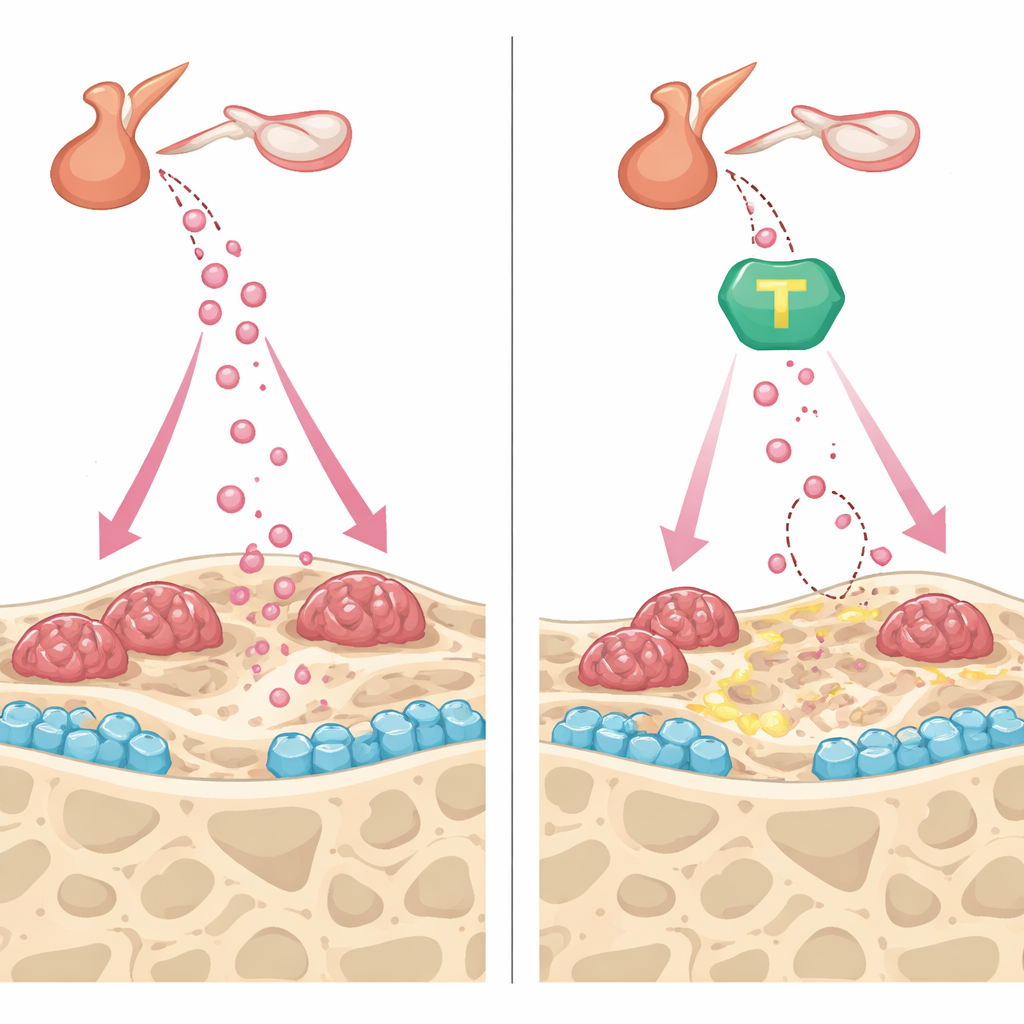
Защита кости с двух сторон
Помимо снижения FSH, #11a и активатор TrkB CF3CN показали дополнительные преимущества непосредственно в кости. В культурах остеобластов оба соединения ускоряли созревание и отложение минерала, отчасти сохраняя фибронектин — структурный белок, который AEP обычно расщепляет, — и усиливали про-остеальные сигналы, такие как остеопротегерин. В остеокластах препараты ослабляли действие ключевого сигнала резорбции, снижая число крупных многоядерных клеток и их способность выточивать лунки в костных срезах. В живых мышах как #11a, так и CF3CN сдерживали быстрый обмен костной ткани, вызванный удалением яичников, стабилизируя плотность и микроархитектонику кости. Поразительно, что при прямом сравнении #11a с терипаратидом — одобренным FDA инъекционным препаратом, стимулирующим образование кости — экспериментальная таблетка сопоставимо восстанавливала объем и прочность кости в этой модели.
Что это может значить для будущего лечения остеопороза
Для неспециалиста ключевая мысль такова: работа выявляет путь с двойным действием, связывающий воспалительные процессы, связанные с менопаузой, с ростом FSH и повреждением кости, и показывает, что мишень AEP может прервать эту цепочку. У мышей пероральный ингибитор AEP не только снижает избыточный FSH, питающий потерю кости, но и прямо смещает баланс в самой кости в сторону строительства, а не разрушения. Хотя эти результаты нужно подтвердить на людях, они указывают на то, что будущие терапии остеопороза могут выйти за рамки простого замещения эстрогена или стимуляции образования кости и вместо этого подавлять недавно описанную гормональную и ферментную цепочку, ведущую к постменопаузной хрупкости костей.
Цитирование: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Ключевые слова: постменопаузальный остеопороз, фолликулостимулирующий гормон, путь C/EBPβ AEP, моделирование кости, терапия, нацеленная на гормоны