Clear Sky Science · ru
Индуцированное TGF-β образование фибротического рубца ограничивает восстановление при повреждении спинного мозга
Почему рубцы в спинном мозге важны
Когда спинной мозг сильно повреждён, многие люди остаются с постоянным параличом или потерей чувствительности, потому что повреждённые нервные волокна не отрастают заново. В этом исследовании поставлен простой, но ключевой вопрос: что именно мешает этому восстановлению — и можно ли безопасно убрать этот барьер? Раскрывая механизм формирования определённого типа рубца внутри поражённого участка, авторы указывают на новый путь, который может помочь нервной системе восстановиться.
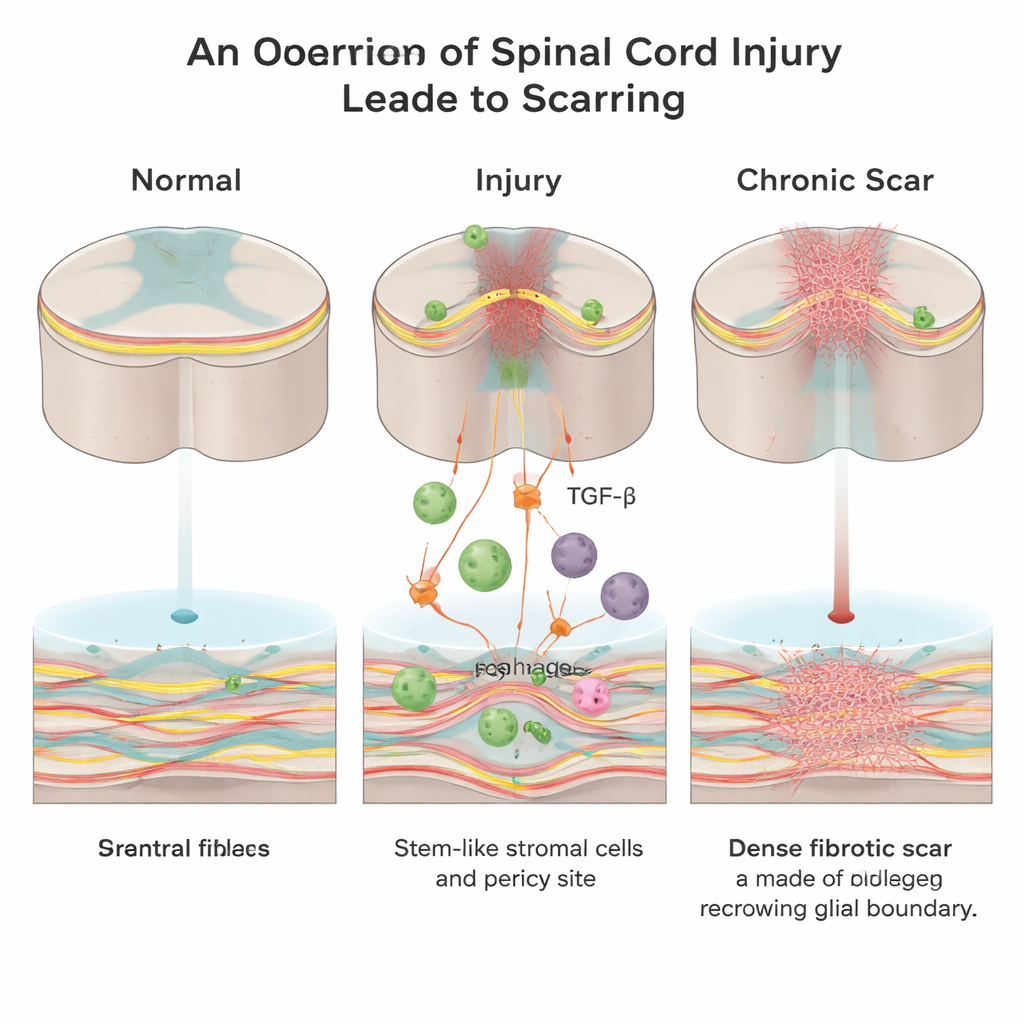
Скрытая стена внутри повреждения
После травмы спинного мозга организм стремится запечатать рану. Образуются два основных вида рубцовой ткани: «глиальный» рубец, созданный опорными клетками — астроцитами, и «фибротический» рубец, богатый коллагеном, фибронектином и фибробластами. Если глиальный рубец может выполнять защитные функции, то фибротический рубец формирует плотную физическую и химическую преграду, через которую растущим нервным волокнам трудно пройти. До сих пор учёные знали гораздо меньше о том, как возникает этот фибротический центр и какие сигналы стимулируют его формирование.
Роль иммунных клеток и мощного сигнала
Работая на взрослых мышах, исследователи сосредоточились на сигнальной молекуле, называемой трансформирующим фактором роста бета (TGF‑β), которая координирует заживление ран по всему организму и часто гиперактивна при фиброзных заболеваниях. Они обнаружили, что после повреждения спинного мозга внедряющиеся иммунные клетки — макрофаги — становятся основным источником активного TGF‑β1 в очаге поражения. Этот всплеск TGF‑β1 привлекает местные мезенхимальные стромальные/стволовые клетки и сосудо‑ассоциированные клетки — перициты — и заставляет их превращаться в фибробласты, те самые клетки, которые откладывают коллаген, образуя фибротический рубец.
Ослабление сигнала, чтобы открыть путь
Чтобы проверить, действительно ли этот путь вызывает вредный рубец, команда использовала несколько генетических приёмов у мышей. При удалении макрофагов или при делеции гена TGF‑β1 исключительно в клетках макрофагоподобной линии количество фибротической ткани в поражённом спинном мозге значительно снижалось, и больше нервных волокон и серотонинергических путей могли пересекать зону повреждения. Аналогично, удаление рецептора TGF‑β специфически в перицитах уменьшало их ответ на TGF‑β, приводило к меньшему накоплению коллагена и улучшало двигательные и сенсорные показатели в поведенческих тестах. Важно, что перициты и связанные со стволовыми клетками популяции сохранялись, но реже превращались в фибробласты, формирующие рубец.
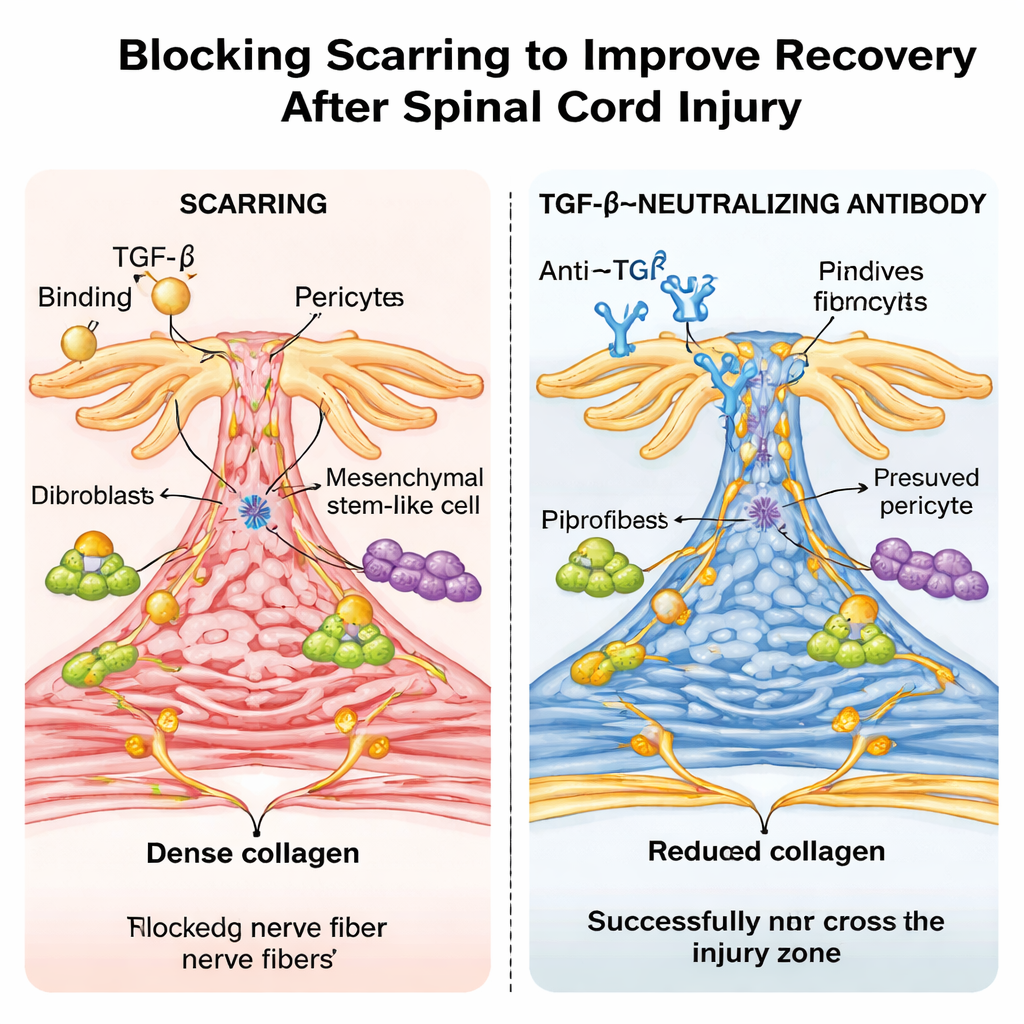
Антитело, похожее на препарат, и неожиданный эффект возраста
Затем исследователи попробовали более клинически релевантный подход: лечили обычных мышей лабораторным антителом, нейтрализующим TGF‑β. Повторные дозы после травмы снижали уровень активного TGF‑β в крови и спинном мозге, уменьшали фибротический рубец и позволяли нервным волокнам эффективнее мостить очаг поражения, с заметным улучшением ходьбы и сенсорных функций. Одноклеточное РНК‑секвенирование подтвердило, что гены, отвечающие на TGF‑β, были сильно активны в клетках, формирующих рубец, у не леченных мышей и были подавлены антителом. Поразительно, что при таком же типе ушиба спинного мозга у новорождённых мышей животные заживали почти без фибротического рубцевания, в очаге не обнаруживалась активация TGF‑β, и восстановление движения было близко к норме — похоже на бесрубцовое восстановление, наблюдаемое у некоторых немлекопитающих животных.
Что это может означать для будущего лечения
В совокупности результаты указывают на то, что чрезмерная активация TGF‑β после повреждения спинного мозга перенаправляет полезные клетки восстановления на строительство жёсткой фибротической стены, которая блокирует отрастание нервов и функциональное восстановление. Предотвращая эту гиперактивацию — посредством нацеливания на продукцию TGF‑β в макрофагах, блокирования его рецептора на перицитах и стромальных клетках или использования нейтрализующего антитела — возможно уменьшить вредный рубец, сохранив или даже усилив более полезные типы тканевого ответа. Хотя перенос этих стратегий на людей потребует тщательного изучения, чтобы избежать побочных эффектов, работа выделяет фибротическое рубцевание, опосредованное TGF‑β, как центральный и потенциально лекарственно доступный барьер для восстановления спинного мозга.
Цитирование: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Ключевые слова: поражение спинного мозга, фибротический рубец, TGF-бета, макрофаги, регенерация нервов