Clear Sky Science · ru
HIF-1α и BMAL1 при регенерации кости: взаимосвязь ответа на гипоксию и циркадного ритма
Почему переломы заживают лучше, чем вы думаете
Когда мы ломаем кость или удаляем зуб, в организме тихо разворачивается удивительно скоординированный процесс восстановления. Глубоко в зоне повреждения уровень кислорода падает, а наш внутренний суточный часы продолжают работать. В этой статье рассматривается, как два управляющих звена — HIF‑1α, чувствительный к низкому содержанию кислорода, и BMAL1, ключевой белок часового механизма — действуют совместно, направляя клетки кости через воспаление, образование новой ткани и восстановление прочности. Понимание этого партнерства может улучшить лечение переломов, остеопороза, артрита и даже удачность дентальных имплантов.
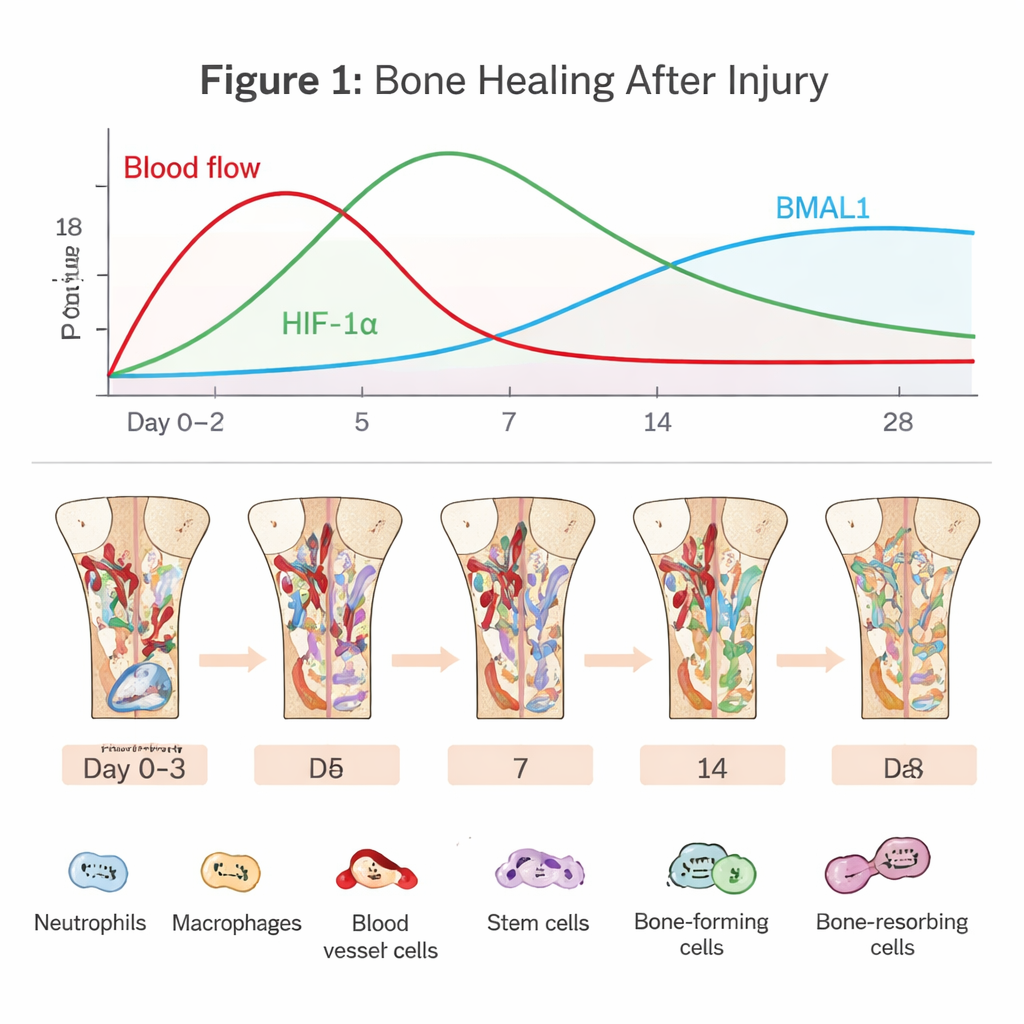
Скрытая драма внутри заживающей кости
Регенерация кости начинается в момент разрыва сосудов. Образуется сгусток, который отсекает большую часть поступления кислорода и создает суровый очаг с пониженным содержанием кислорода. Иммунные клетки, такие как нейтрофилы и макрофаги, устремляются в зону, чтобы убрать обломки и отразить микробов. Одновременно к работе привлекаются стволовые клетки костного мозга и клетки сосудов, чтобы восстановить участок. Эта ранняя «фаза воспаления» — палка о двух концах: короткий, точно скоординированный всплеск воспаления запускает восстановление, но если он длится слишком долго или слишком интенсивен, заживление может затормозиться или сорваться. В статье подчеркивается, что прохождение по этой узкой грани во многом зависит от того, как клетки считывают кислород и время.
Как клетки используют гипоксию себе на пользу
В бедной на кислород зоне перелома белок HIF‑1α стабилизируется и включает гены, которые помогают клеткам адаптироваться. Он стимулирует эндотелиальные клетки к росту новых сосудов, обеспечивая приток свежего кислорода и питательных веществ в дефект. Он также перестраивает метаболизм клеток в сторону гликолиза — способа получения энергии, работающего даже при недостатке кислорода. Для стволовых клеток и остеобластов умеренная активация HIF‑1α может усиливать пролиферацию, миграцию и формирование кости, отчасти за счет увеличения факторов, таких как VEGF, связывающих васкулогенез с образованием новой кости. Но если гипоксия слишком сильна или затяжна, накапливаются стрессовые молекулы и реактивные формы кислорода, что толкает остеобласты к гибели и стимулирует остеокласты, разрушающие кость. Таким образом один и тот же гипоксический сигнал может либо поддержать, либо саботировать заживление — все зависит от его интенсивности и продолжительности.
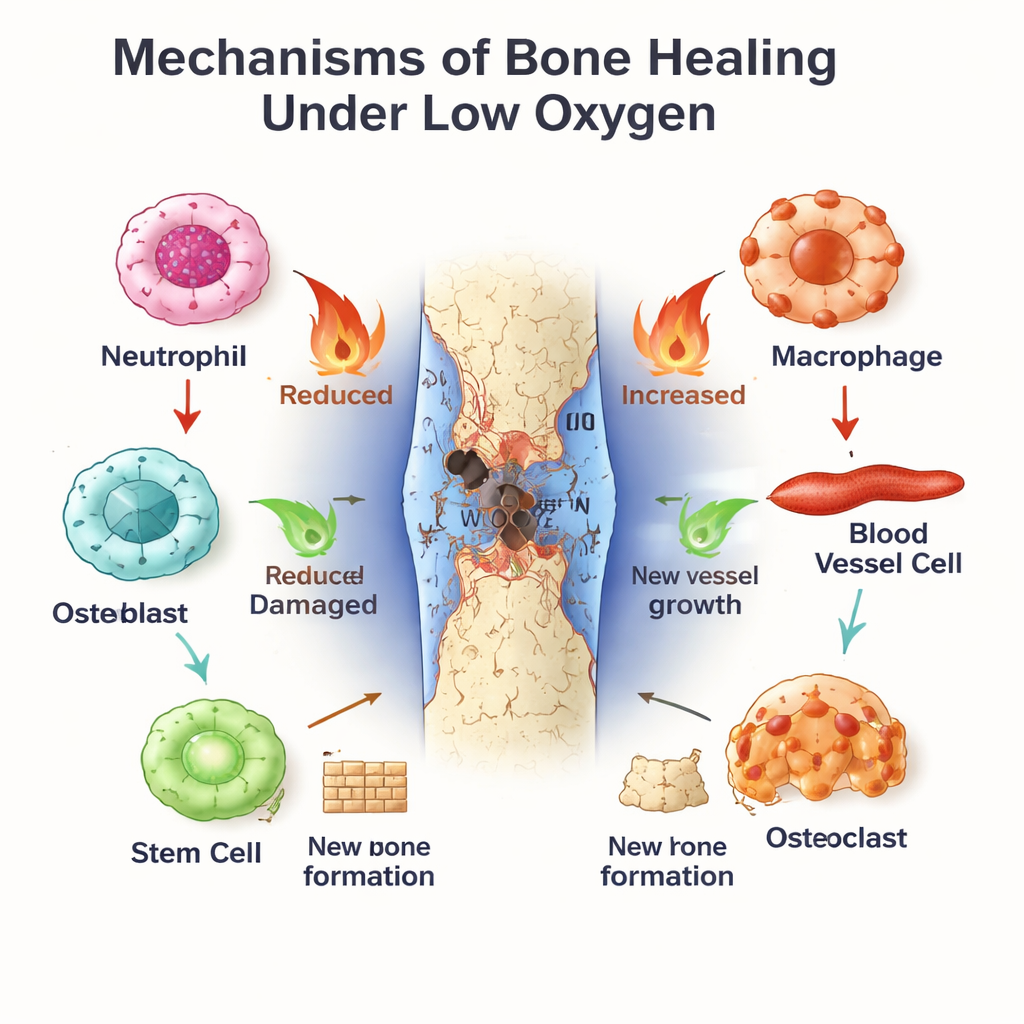
Внутренние часы организма как менеджер восстановления кости
Параллельно работает циркадный метроном — молекулярный хронометр, присутствующий почти в каждой клетке. BMAL1, один из его центральных компонентов, задает суточные ритмы иммунной активности, поведения сосудов и дифференцировки стволовых клеток. Нейтрофилы и макрофаги демонстрируют различия во времени суток в силе ответа на травму и скорости старения или переключения с воспалительного (похожего на M1) на репаративное (похожее на M2) состояния. В клетках сосудов и стволовых клетках костного мозга BMAL1 способствует здоровой пролиферации и упорядоченному формированию кости, отчасти путем настройки сигнальных путей, таких как Wnt и TGF‑β/SMAD. Когда BMAL1 нарушен — вследствие генетических дефектов, сменных графиков работы или метаболических заболеваний — кости склонны терять массу, стволовые клетки истощаются, и баланс между образованием и резорбцией кости смещается в сторону потерь.
Диалог между кислородным сенсором и биологическими часами
Сердцем обзора является появляющаяся «перекличка» между HIF‑1α и BMAL1. Эти два белка имеют сходные структуры и могут физически взаимодействовать, даже образуя смешанные комплексы, которые связываются с ДНК и контролируют пересекающиеся наборы генов. Каждый из них может влиять на производство и стабильность другого, создавая петли обратной связи, связывающие темпы суточного цикла с реакцией клеток на гипоксию. Вместе они также управляют клеточным редокс‑балансом — соотношением образования вредных реактивных форм кислорода и антиоксидантной способности — и совместно регулируют ключевые ферменты, определяющие, полагаются ли клетки больше на кислород‑зависимое дыхание или на анаэробный гликолиз. Это совместное управление помогает решить, будет ли среда перелома способствовать конструктивному восстановлению или приведет к чрезмерному воспалению и резорбции кости.
Что это значит для заболеваний и лечения
То же партнерство HIF‑1α–BMAL1 проявляется при многих состояниях, связанных с костями. У сменщиков сна нарушение режима и светового воздействия, вероятно, изменяет BMAL1, усиливает окислительный стресс и мешает HIF‑1α‑опосредованному восстановлению, что способствует развитию остеопороза. При диабете высокий уровень сахара ослабляет как функцию часов, так и гипоксический сигнал, подрывая рост сосудов и образование кости, опосредованное стволовыми клетками. При остеоартрите потеря BMAL1 в хондроцитах нарушает их ритм и защитные взаимодействия с HIF‑1α, ускоряя разрушение хряща. Вокруг титановых имплантатов контролируемая гипоксия и здоровый циркадный ритм, по-видимому, способствуют лучшей остеоинтеграции, что дает повод предположить, что будущие покрытия имплантов можно будет проектировать так, чтобы мягко активировать и HIF‑1α, и BMAL1. В целом статья делает вывод, что успешная регенерация кости зависит не только от набора клеток, но и от того, как они «читают» кислород и время, и что нацеливание на этот диалог может открыть новые пути к более быстрому и прочному заживлению.
Цитирование: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Ключевые слова: регенерация кости, циркадный ритм, гипоксия, остеопороз, заживление переломов