Clear Sky Science · ru
Умные биоматериалы для восстановления и регенерации скелета при старении
Крепче кости в мире стареющего населения
Многие считают ослабление костей и боли в суставах неизбежными спутниками старения. Но ученые разрабатывают «умные» материалы, которые способны обнаруживать, когда и где кость дает сбой, и помогать ей самовосстанавливаться. Такие материалы призваны надежнее заживлять переломы, замедлять или обращать вспять остеопороз и остеоартроз и снижать потребность в повторных операциях — давая пожилым людям лучший шанс оставаться активными и самодостаточными.
Как кости стареют и почему они легче ломаются
Кость — живая ткань, которая постоянно перестраивается, но с возрастом этот баланс нарушается. Стволовые клетки в костном мозге смещают направление дифференцировки от образования остеобластов к образованию жировых клеток; клетки, строящие кость, устают, а клетки, разрушающие кость, становятся гиперактивными. Поддерживающая матрица из коллагена и минералов становится суше и хрупче, а микроскопическая «арматура» истончается. Гормональные изменения, хроническое низкоуровневое воспаление, избыток реактивных форм кислорода и местная кислотность усугубляют ситуацию. Снаружи это проявляется более тонкой, пористой костью, тугими суставами, искривлением позвоночника и повышенным риском переломов и заболеваний, таких как остеопороз и остеоартроз.
Почему существующих методов лечения недостаточно
Основные современные подходы включают препараты, замедляющие потерю кости или стимулирующие её образование, а также операции и металло- или керамические имплантаты для стабилизации переломов или замены поврежденных суставов. Эти методы спасли множество жизней, но имеют важные недостатки. Системные препараты часто достигают лишь крошечной доли костной ткани и могут вызывать побочные эффекты — от проблем с челюстью и тромбов до повышенного риска рака при длительном применении. Терапии на основе стволовых клеток демонстрируют обещающие результаты в экспериментах на животных, но сталкиваются с проблемами выживания клеток, непредсказуемым поведением и риском образования опухолей. Традиционные имплантаты обеспечивают прочность, но остаются «глупыми» объектами: они не чувствуют окружение, не могут регулировать выделение лекарств и могут давать сбои в хрупкой кости пожилых пациентов.
Умные переносчики лекарств, патрулирующие организм
Умные биоматериалы вносят элемент интеллекта. Одна из ключевых стратегий — системная «умная доставка» препаратов с помощью наночастиц или мягких гелей, которые циркулируют в кровотоке и активируются только в проблемных зонах. Такие носители могут реагировать на внутренние сигналы — кислотность, высокий уровень повреждающих форм кислорода или ферменты, разрушающие кость, — или на внешние воздействия: свет, ультразвук, тепло или магнитное поле. Например, некоторые частицы остаются неповрежденными в нормальной ткани, но раскрываются и высвобождают лекарство в кислой, богатой ферментами среде, где сверхактивные клетки резорбируют кость. Другие улавливают избыток реактивных форм кислорода, одновременно медленно отдавая противовоспалительные препараты, или несут контрастные красители, чтобы врачи могли в реальном времени видеть их распределение. Комбинируя несколько триггеров — например, и pH, и окислители — исследователи повышают точность прицела и снижают побочные эффекты.
Местные каркасы, действующие как временные «умные» кости
Когда у стареющих пациентов возникают большие дефекты кости или сложные переломы, в зазор можно имплантировать местные «умные каркасы». Эти трехмерные структуры из металлов, керамики, полимеров или их сочетаний проектируют так, чтобы соответствовать прочности, пористости и гибкости кости. Их губчатая архитектура позволяет кровеносным сосудам и новой кости прорастать внутрь, в то время как материал постепенно растворяется и замещается собственной тканью пациента. 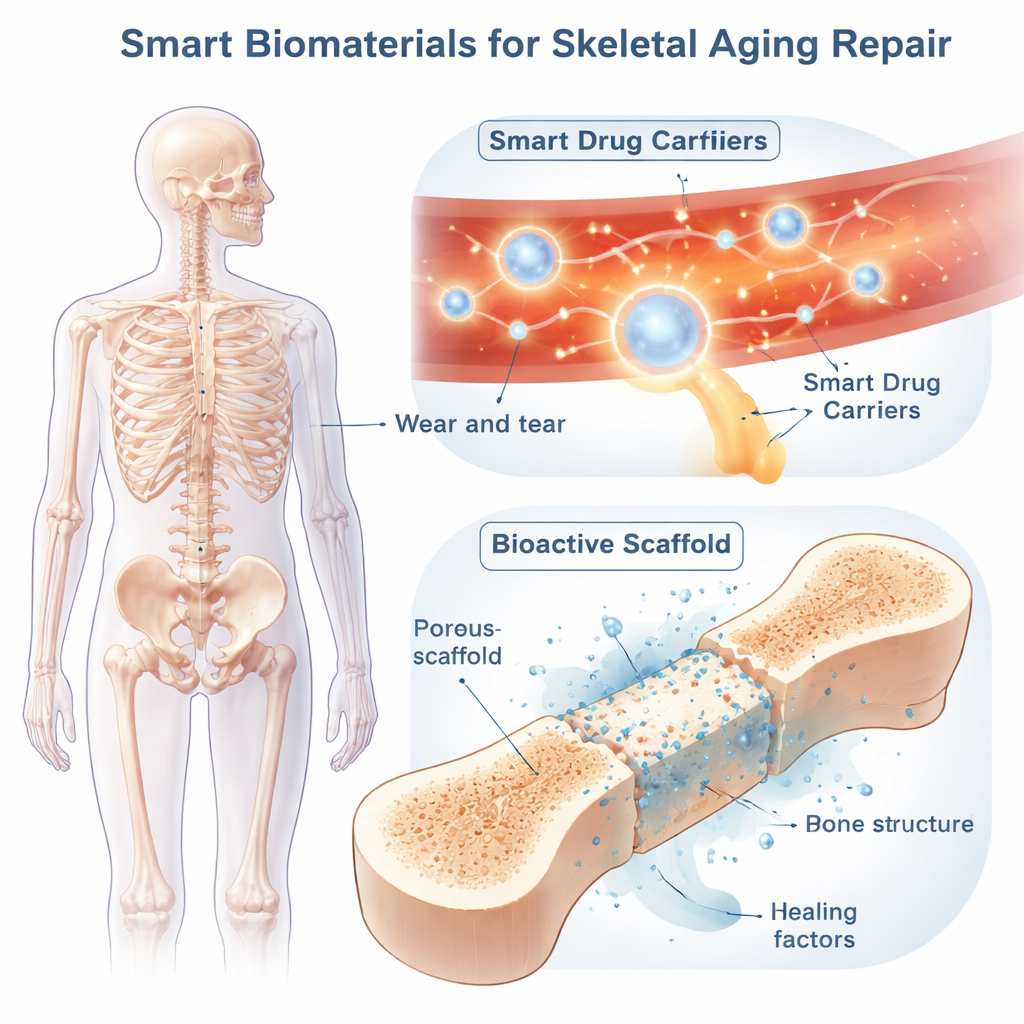
От лаборатории к клинике: инструменты, препятствия и направления развития
Для создания этих сложных систем ученые используют передовые методы производства — 3D-печать и аддитивное производство — чтобы с высокой точностью настраивать размер пор, жесткость и загрузку лекарств. Тем не менее перевод умных биоматериалов в рутинную клиническую практику сопряжен с трудностями. Большинство инъецируемых частиц по-прежнему накапливается в органах, таких как печень и селезенка, а не в кости, и многие животные модели не учитывают сложности стареющего человеческого организма. Массовое производство, контроль качества, регуляторное одобрение и стоимость остаются серьезными барьерами. Исследователи видят перспективы в сочетании умных материалов с искусственным интеллектом для персонализации дизайна каркасов и дозировки препаратов, а также в добавлении встроенных сенсоров, способных отслеживать заживление и автоматически регулировать терапию в «закрытом контуре». 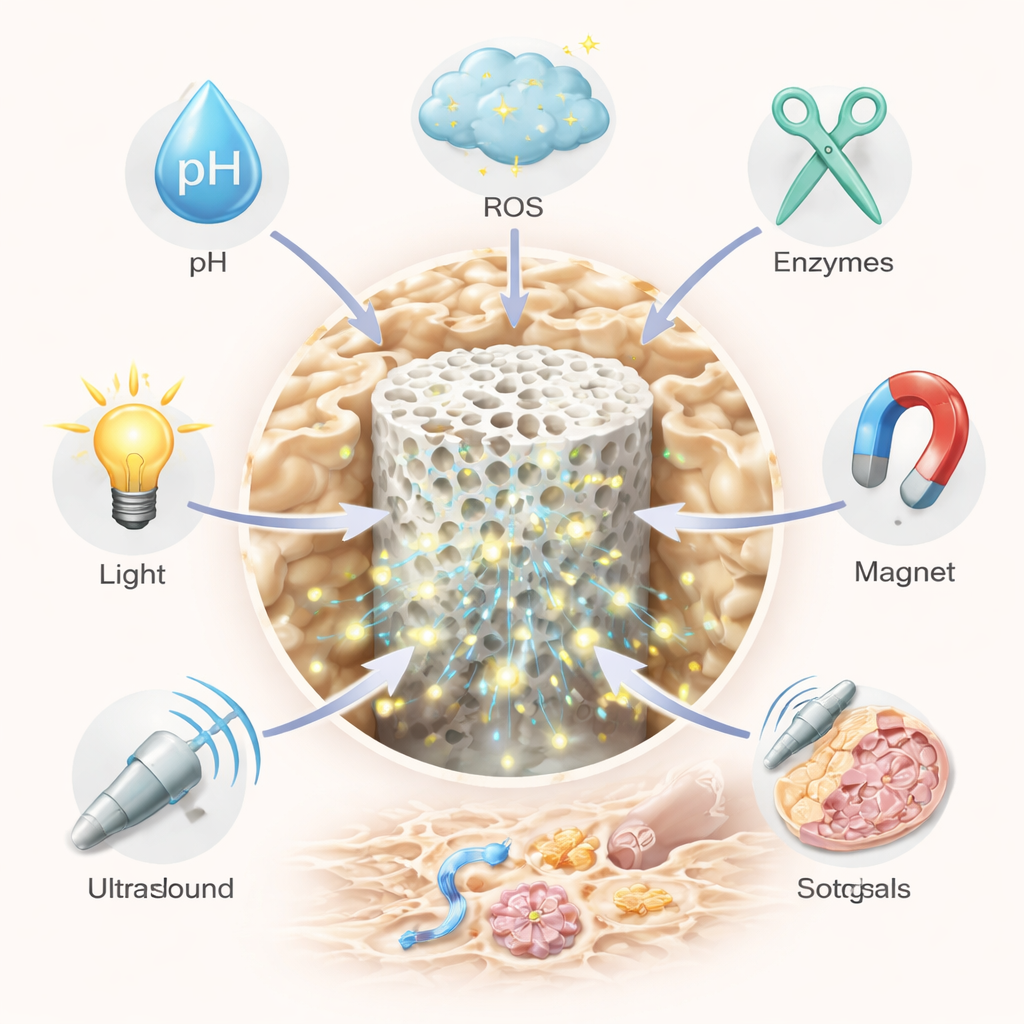
Что это может значить для пациентов
По сути, эти разработки показывают, что хрупкость костей в пожилом возрасте — не просто необратимый упадок, а сложная инженерная задача, которую, возможно, можно решить. Умные биоматериалы действуют как крошечные программируемые ремонтные бригады: патрулируют кровоток, оседают в поврежденных участках и высвобождают ровно то, что нужно, в нужный момент, чтобы восстановить структуру и функцию кости. Хотя эти технологии пока в основном на стадии исследований, они указывают на будущее, в котором переломы заживают быстрее, имплантаты служат дольше, а терапии подбираются под уникальную костную биологию каждого человека — помогая большему количеству людей сохранять подвижность и самостоятельность в преклонном возрасте.
Цитирование: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
Ключевые слова: умные биоматериалы, старение скелета, регенерация кости, остеопороз, реагирующие на стимулы каркасы