Clear Sky Science · ru
Внеклеточные везикулы, происходящие от воспалительных макрофагов синовии, ухудшают повреждения хряща в остеоартрите через выборочную сортировку FMRP
Почему воспаление сустава важно для болящих коленей
Многие представляют остеоартрит как простое «истирание» суставов с возрастом, но накопившиеся данные показывают, что низкоуровневое воспаление внутри сустава может тихо прогрессировать болезнь. В этом исследовании поставлен конкретный вопрос: как иммунные клетки в синовиальной оболочке общаются с хрящевыми клетками, и можно ли прервать этот диалог, чтобы защитить суставы? Ответы выявляют крошечную молекулярную курьерскую систему, которая усугубляет повреждения, но также предлагает новый подход к диагностике и лечению остеоартрита.
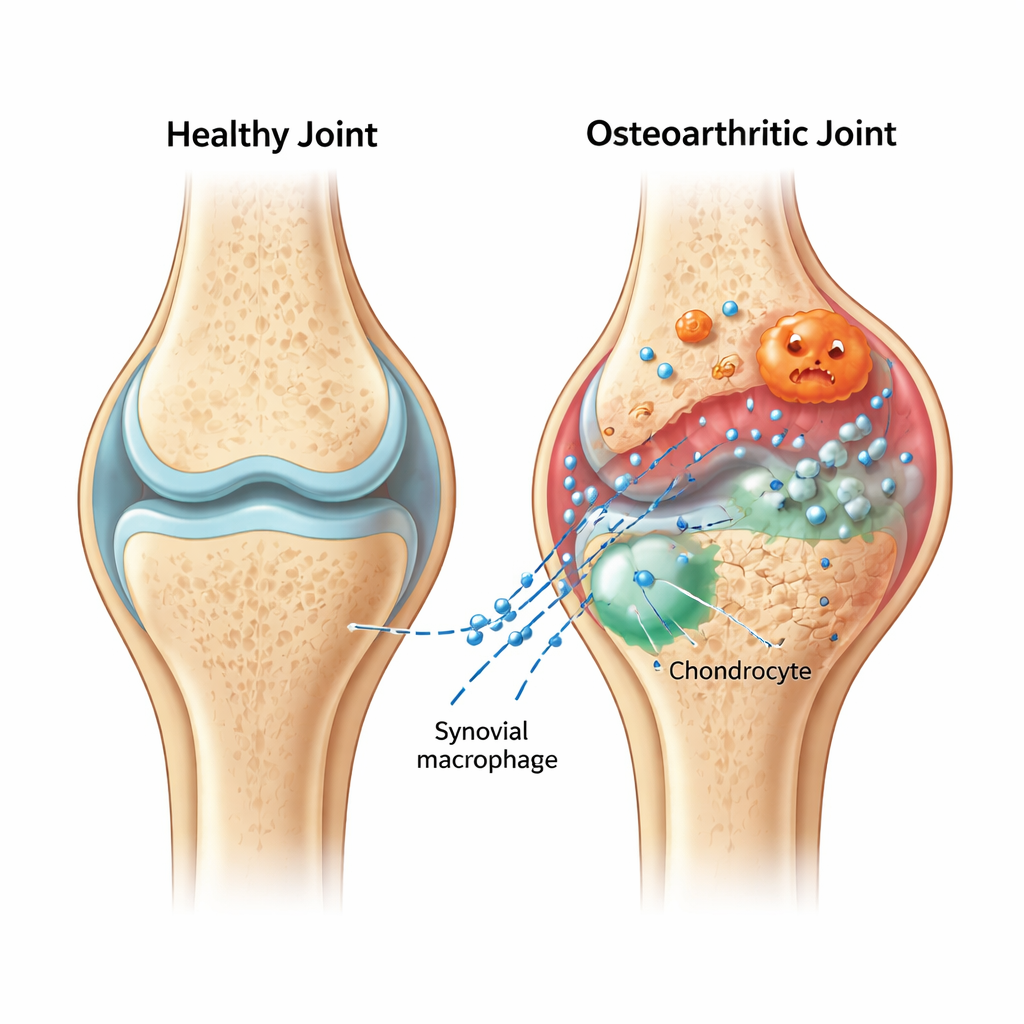
Крошечные посылки, несущие плохие вести
Внутри артритического колена мягкая синовиальная оболочка воспаляется и наполняется иммунными клетками — макрофагами. Авторы сосредоточились на «прокачанных» про‑воспалительных макрофагах и микроскопических пузырьках, которые они выделяют — внеклеточных везикулах. Эти везикулы действуют как запечатанные посылки, перевозящие молекулы между клетками. У крыс с хирургически вызванным остеоартритом команда показала, что везикулы от воспалённых макрофагов направляются в хрящ и усугубляют повреждение: обычно гладкая амортизирующая поверхность становилась более шероховатой и тонкой, ключевые хрящевые белки снижались, а ферменты распада возрастали.
Как воспаление выключает самоподдерживающую очистку хряща
Хрящевые клетки, или хондроциты, полагаются на процесс «домашнего хозяйства» — аутофагию, чтобы перерабатывать изношенные компоненты и оставаться здоровыми на протяжении жизни. Когда исследователи сравнили гены, включённые в хряще, подвергнутом воздействию воспалительных везикул, и в контроле с физиологическим раствором, они обнаружили убедительные признаки подавления аутофагических путей. Под электронным микроскопом хрящ из суставов, леченных везикулами, содержал значительно меньше характерных везикул переработки. В культурах клеток хондроциты, подвергнутые действию макрофагальных везикул, также формировали меньше аутофагосом и аутолизосом, что подтверждает, что их механизмы самочистки выключались одновременно с накоплением повреждений.
Одна микроРНК переключает критический механизм
Углубившись, команда изучила крошечные регуляторные РНК в макрофагальных везикулах. Одна молекула, miR‑155‑5p, выделялась: она была обогащена в везикулах животных с остеоартритом и в тканях суставов людей с остеоартритом, особенно в синовии. Эксперименты показали, что доставляемая везикулами miR‑155‑5p проникает в хондроциты и напрямую нацеливается на белок GSK‑3β, который в норме помогает сдерживать сигнальный путь контроля роста mTORC1. При подавлении GSK‑3β mTORC1 гиперактивируется, аутофагия снижается, и хрящевые клетки становятся менее устойчивыми к стрессу. Блокирование miR‑155‑5p специальным «антагомиром» у крыс восстановило аутофагию, сохранило структуру хряща и уменьшило признаки остеоартрита, тогда как мыши, генетически лишённые miR‑155 в своих макрофагах, развивали более лёгкую форму болезни и меньше синовита.
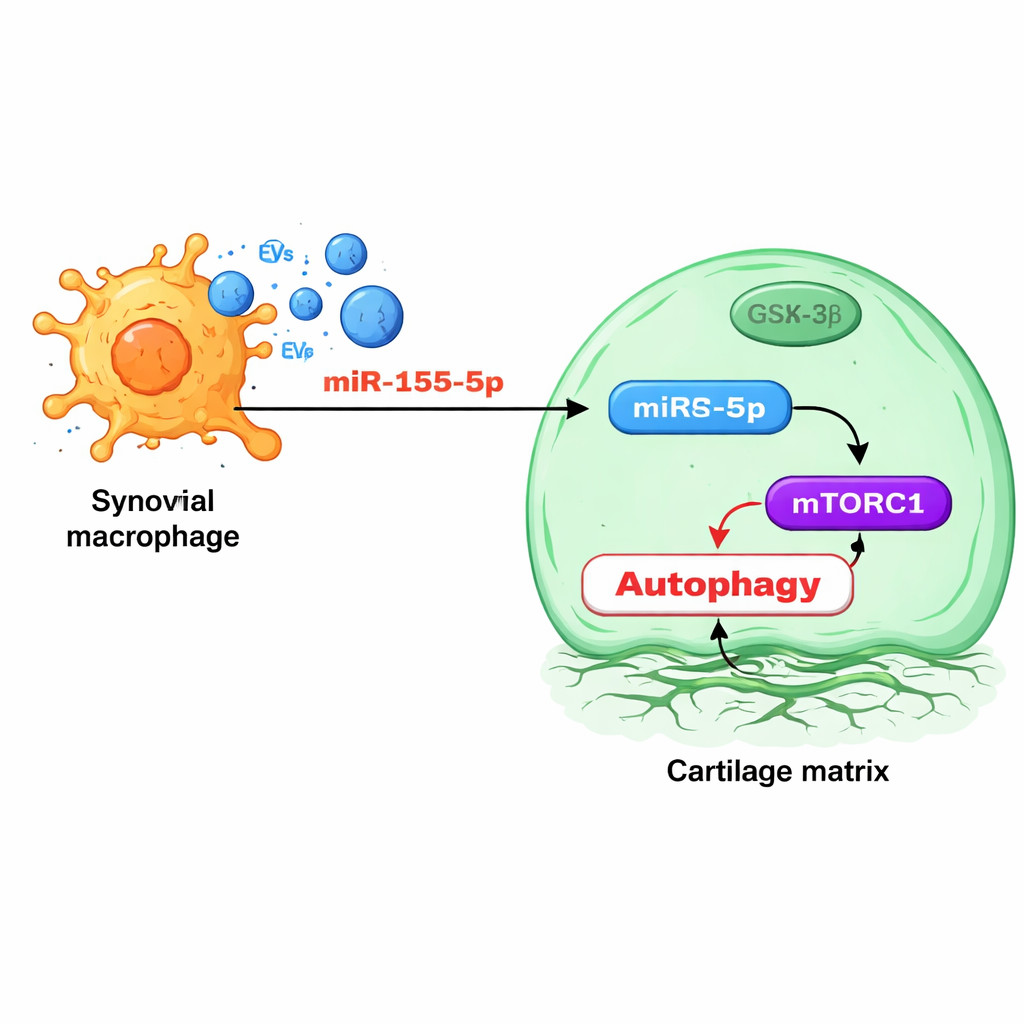
Сортировка и нацеливание повреждающего сигнала
Любопытно, что исследование выявило, что макрофаги используют специфический РНК‑связывающий белок FMRP для селективной загрузки miR‑155‑5p в везикулы. При повышении уровней FMRP везикулы несли больше miR‑155‑5p и сильнее повреждали хондроциты; при уменьшении FMRP везикулы становились менее токсичными, и аутофагия хондроцитов восстанавливалась. Уровни FMRP в везикулах, циркулирующих в крови, росли по мере прогрессирования остеоартрита и у крыс, и у пациентов, что указывает на то, что этот белок или везикулы с ним могут служить маркером активности болезни в крови, без необходимости визуализации или инвазивных процедур.
Безклеточная терапия, нацеленная на нужные клетки
Опираясь на эти механистические данные, исследователи создали потенциальную терапию, использовав везикулы от стромальных клеток, полученных из адипозной ткани — типа стволоподобных клеток жировой ткани. Они «украшали» эти везикулы небольшим пептидом, действующим как направляющее устройство для про‑воспалительных макрофагов, и загружали их антагомиром‑155‑5p. У крыс с остеоартритом повторные инъекции таких нацеленных везикул уменьшали синовиальное воспаление, смещали макрофаги в более «восстановительное» состояние, снижали уровни miR‑155‑5p в суставе, восстанавливали GSK‑3β и улучшали структуру и состав хряща сильнее, чем ненаправленные везикулы. При обработке образцов человеческой синовиальной ткани в лаборатории эти сконструированные везикулы также снижали маркеры воспаления и усиливали противовоспалительные сигналы.
Что это значит для людей с остеоартритом
Эта работа переосмысливает остеоартрит не только как заболевание механического износа, но и как молекулярный диалог между воспалёнными клетками синовии и хрящом. Про‑воспалительные макрофаги отправляют везикулы, загруженные miR‑155‑5p, которые подавляют системы самовосстановления хондроцитов через путь GSK‑3β/mTORC1 и ускоряют распад ткани. Блокируя этот сигнал — генетически или с помощью нацеленных терапевтических везикул — исследователи смогли ослабить и воспаление, и повреждение хряща в модельных животных и в образцах тканей человека. Хотя до клинического применения ещё далеко, исследование открывает новые возможности: анализ крови на основе содержимого везикул для мониторинга болезни и точечные безклеточные лечения, которые утихомиривают вредное воспаление и одновременно помогают хрящу защищать себя.
Цитирование: Zhao, S., Wang, J., Xue, M. et al. Synovial inflammatory macrophage-derived extracellular vesicles exacerbate cartilage lesions with a FMRP-selectively sorted manner in osteoarthritis. Bone Res 14, 26 (2026). https://doi.org/10.1038/s41413-025-00502-4
Ключевые слова: остеоартрит, внеклеточные везикулы, макрофаги, хрящ, микроРНК-155