Clear Sky Science · ru
MicroRNA-132/212 отрицательно модулирует опиоидное вознаграждение, нацеливаясь на транспортёр дофамина в вентральной части покрышки
Почему это исследование важно для повседневной жизни
Опиоидные обезболивающие и родственные препараты могут приносить облегчение, но также несут серьёзный риск зависимости. В этом исследовании заглянули под капот системы вознаграждения мозга, чтобы выявить крошечные генетические переключатели, которые влияют на то, насколько сильно опиоиды воспринимаются как вознаграждение. Поняв эти переключатели, учёные надеются разработать более умные методы лечения, которые снимают боль или уменьшают зависимость, не захватывая при этом центры удовольствия мозга.
Малые молекулы с большим влиянием
Наши мозги полагаются на химическое вещество под названием дофамин, которое сигнализирует об удовольствии и мотивирует нас искать вознаграждающие переживания — от вкусной пищи до наркотиков. Сила и продолжительность этого сигнала частично контролируются белком под названием транспортёр дофамина, который действует как пылесос, всасывая дофамин обратно в нервные клетки. Авторы сосредоточились на двух очень маленьких фрагментах генетического материала — микроРНК-132 и микроРНК-212 — которые могут понижать производство определённых белков. Ранее эти микроРНК связывали с употреблением кокаина и стрессом. Здесь команда спросила, формируют ли они также реакцию мозга на опиоидные препараты, в частности на морфин.
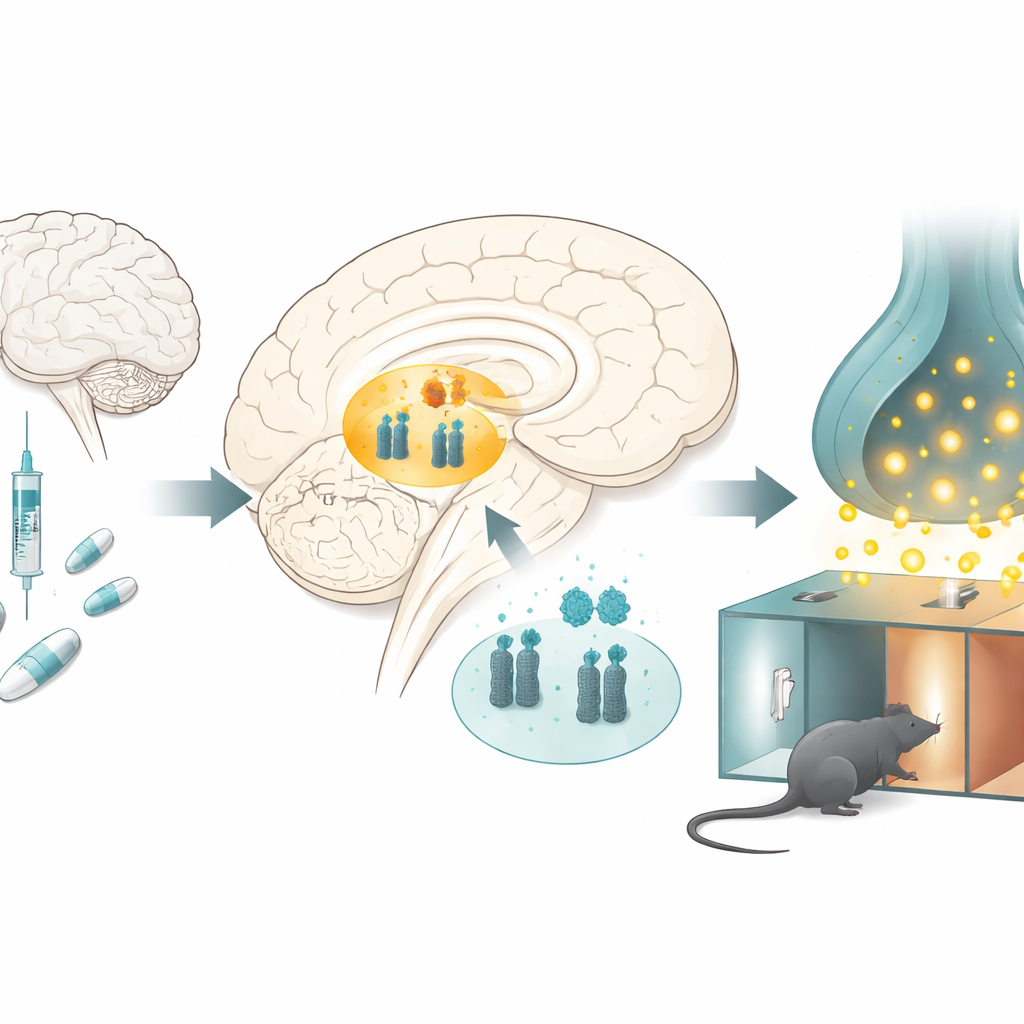
Как опиоиды меняют центр вознаграждения мозга
Исследователи изучали крыс, получавших повторные дозы морфина, в классическом тесте на вознаграждение наркотика, в котором животные учатся предпочитать комнату, связанную с препаратом. Через несколько дней крысы, получавшие морфин, проводили больше времени в камере, связанной с морфином, что свидетельствует о появлении вознаграждающего эффекта. При изучении ключевой области вознаграждения глубоко в мозге — вентральной части покрышки — они обнаружили поразительную картину: уровни микроРНК-132 и микроРНК-212 были снижены, а уровни транспортёра дофамина — повышены. Похожие изменения отмечались и у крыс, получавших морфин без задачи с изучением места, что свидетельствует о том, что хроническое воздействие препарата само по себе смещает это молекулярное равновесие.
Выявление прямой молекулярной связи
Чтобы узнать, действительно ли эти микроРНК контролируют транспортёр дофамина, команда обратилась к человеческим нервоподобным клеткам в лаборатории. Искусственное повышение микроРНК-132 или микроРНК-212 привело к снижению как генетического послания (мРНК), так и белка транспортёра. Блокировка микроРНК вызывала обратный эффект. Затем они сконструировали репортёр, в котором светопродуцирующий фермент был связан с регуляторным хвостом транспортёра. Добавление микроРНК уменьшало световой сигнал, но этот эффект исчезал при мутации нескольких ключевых оснований в сайте связывания. В совокупности эти эксперименты показали, что микроРНК-132 и микроРНК-212 непосредственно связываются с посланием транспортёра и подавляют его продукцию.
От молекул к уровням дофамина и поведению
Далее исследователи спросили, как этот молекулярный контроль проявляется в живых клетках мозга. В культивируемых нервных клетках повышение уровня микроРНК снижало захват дофамина, тогда как их блокада улучшала очищение дофамина. При искусственном увеличении или уменьшении уровней транспортёра дофамина влияние микроРНК соответственно усиливалось или ослабевало, что подтверждает роль транспортёра как основного посредника. В живых крысах повышение микроРНК-132 в вентральной части покрышки увеличивало уровни дофамина, просачивающегося в связанные области, что отражает ослабление активности транспортёра. С поведенческой точки зрения использование вирусных инструментов для «впитывания» (sponge) микроРНК-132 или микроРНК-212 в этой области мозга заставляло крыс сильнее формировать предпочтение к морфину и сопровождалось повышением уровней транспортёра. Напротив, навязывание дополнительной микроРНК-132 в ту же область снижало уровни транспортёра и ослабляло предпочтение к морфину у самцов, самок и подростков, не влияя на подвижность или удовольствие от естественных вознаграждений, таких как подслащенная вода.
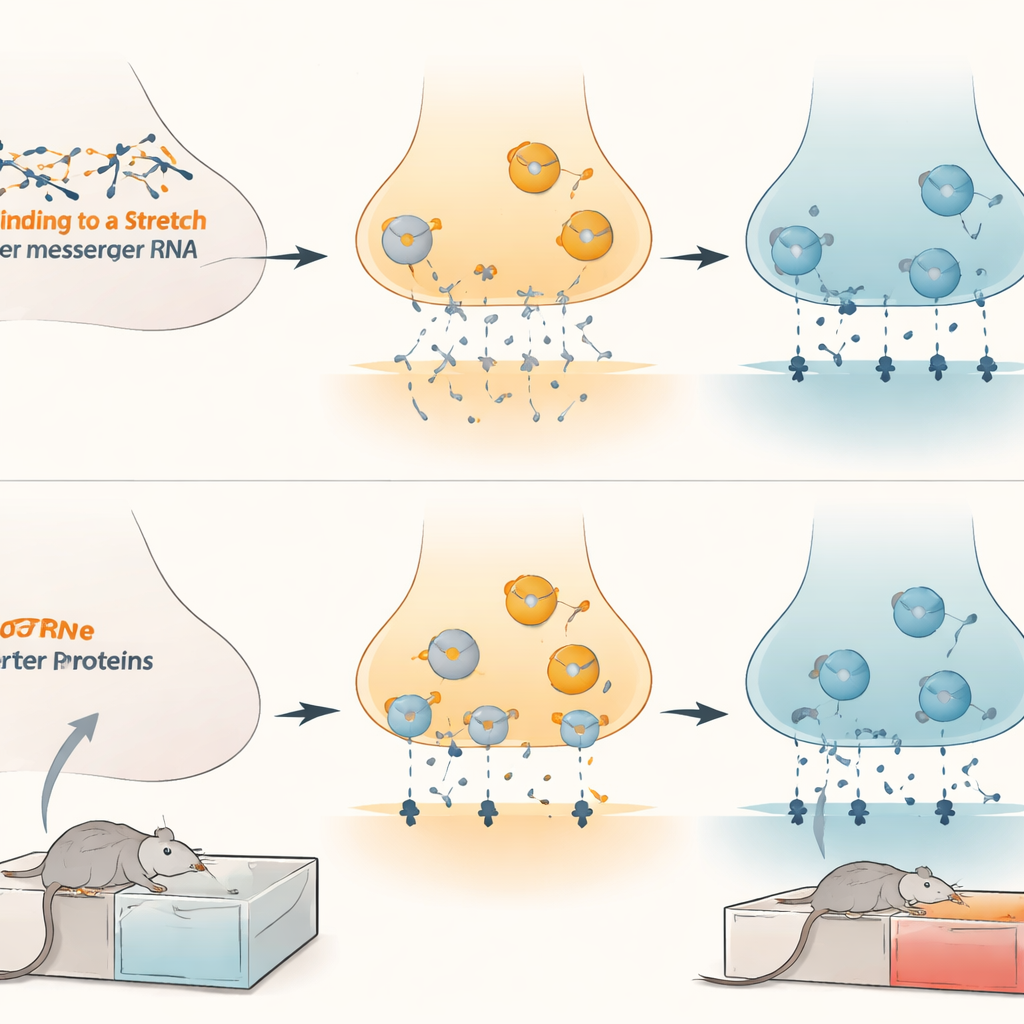
Последствия для лечения опиоидной зависимости
Эти результаты выявляют тонко настроенную тормозную систему в цепях вознаграждения мозга: микроРНК-132 и микроРНК-212 сдерживают транспортёр дофамина, формируя то, насколько сильно опиоиды воспринимаются как вознаграждение. Хронический морфин, по-видимому, ослабляет этот тормоз, понижая уровни микроРНК и позволяя уровням транспортёра повышаться, что помогает закреплять сигналы, связанные с наркотическим вознаграждением. Восстановление или имитация действия этих микроРНК специально в вентральной части покрышки может смягчить влияние опиоидного вознаграждения, не подавляя при этом в целом удовольствие или движение. Хотя до тестирования таких стратегий на людях ещё далеко, это исследование указывает на новый, высоко специфичный путь для будущих методов лечения, которые будут бороться с зависимостью на уровне молекулярных регуляторов мозга.
Цитирование: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Ключевые слова: опиоидная зависимость, транспортёр дофамина, микроРНК-132, вентральная часть покрышки, морфиновое вознаграждение