Clear Sky Science · ru
Функциональная нейровизуализация ингибирования жирнокислотной амидной гидролазы при посттравматическом стрессовом расстройстве: рандомизированное клиническое исследование
Почему химия мозга важна для восстановления после травмы
Многие люди, пережившие травму, развивают посттравматическое стрессовое расстройство (ПТСР) — состояние, характеризующееся ночными кошмарами, флешбэками и постоянным напряжением. Наиболее обоснованные методы лечения — это формы психотерапии, которые аккуратно подвергают человека воспоминаниям о травме в безопасной обстановке, помогая мозгу усвоить, что прошедшая опасность больше не актуальна. Учёные надеялись, что добавление препарата, усиливающего собственные успокаивающие каннабиноидоподобные вещества мозга, может облегчить это обучение и повысить эффективность терапии. В этом исследовании эта идея была подвергнута строгой проверке, а также изучали, что именно происходит внутри мозга.
Обнадёживающая идея из каннабиноидной системы мозга
Организм вырабатывает каннабиноидоподобные вещества, называемые эндоканнабиноидами, которые участвуют в регуляции стресса, страха и эмоционального обучения. Один из них, анандамид, выглядит особенно важным для «угашения страха» — процесса обучения тому, что ранее угрожавший сигнал теперь безопасен. В исследованиях на животных и здоровых добровольцах повышение уровня анандамида улучшает это обучение безопасности и снижает стрессовые реакции. Ключевой фермент, жирнокислотная амидная гидролаза (FAAH), расщепляет анандамид. Блокирование FAAH препаратом увеличивает уровень анандамидов в организме и, как надеялись исследователи, в тех областях мозга, которые контролируют страх и эмоции.
Исходя из этого, команда провела двойное слепое рандомизированное клиническое исследование у 100 взрослых с ПТСР. В течение 12 недель участники получали либо препарат, блокирующий FAAH, либо плацебо, а через 4 недели все начали программу интернет-адаптированной когнитивно-поведенческой терапии (iCBT), ориентированную на работу с травмой. Ранее опубликованные данные этого исследования показали, что, вопреки ожиданиям, ингибитор FAAH в ходе лечения не снижал симптомы ПТСР более эффективно, чем плацебо. Настоящая статья заглядывает в мозговые сканы, чтобы ответить на вопрос: а изменил ли препарат по крайней мере активность мозга или взаимодействие между ключевыми областями эмоций, даже если симптомы не улучшились?
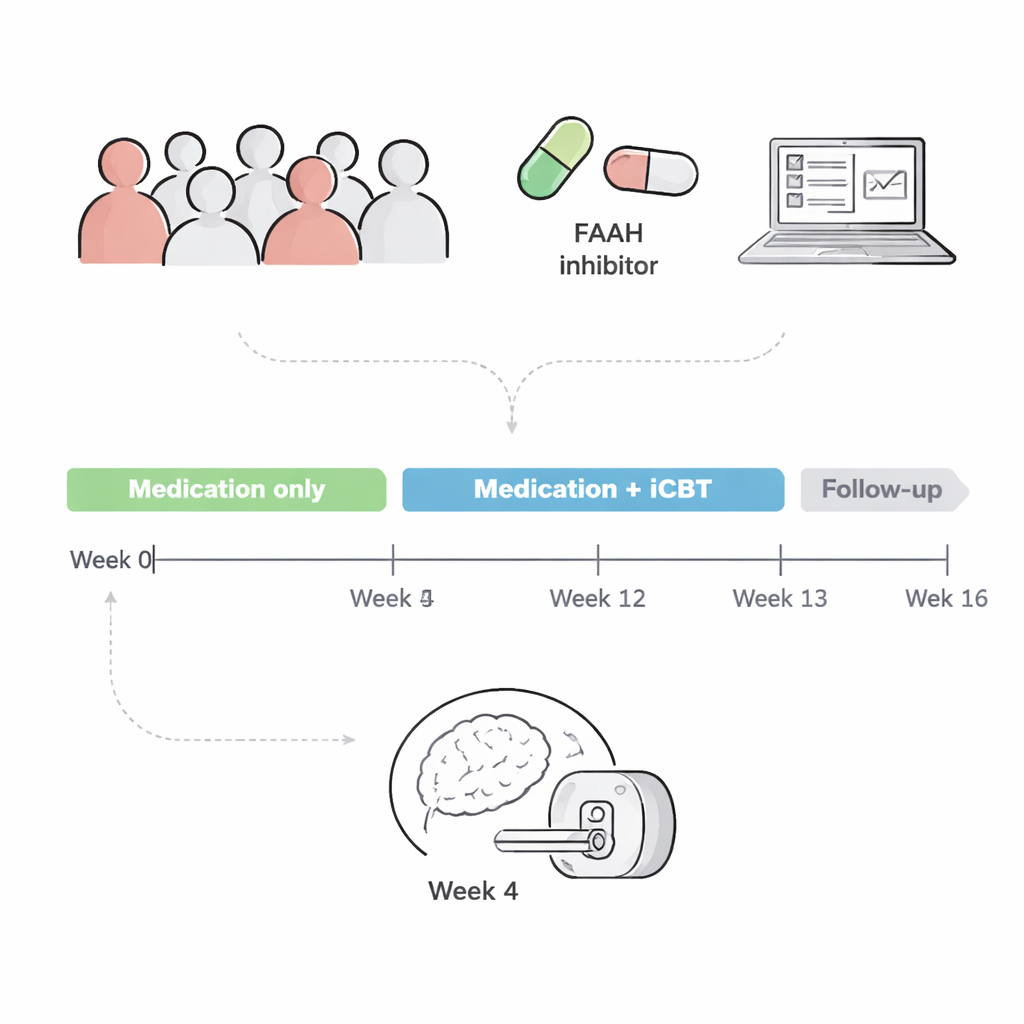
Заглядывая в спокойный и эмоциональный мозг
Семьдесят шесть участников прошли функциональную МРТ после 4 недель приёма препарата или плацебо, прямо перед началом терапии. Исследователи собрали два типа данных о мозге. Во-первых, «сканирование в состоянии покоя» измеряло, насколько синхронно колеблется активность разных областей мозга — признак их функциональной связи. Во-вторых, во время задачи «эмоционального конфликта» участники смотрели на лица и эмоциональные слова, которые иногда совпадали, а иногда противоречили друг другу — некий эмоциональный аналог теста Струпа. Эта задача ранее связывалась с тем, насколько хорошо люди отвечают на терапию при ПТСР.
Команда сосредоточилась на сети, давно вовлечённой в ПТСР: миндалине, которая обнаруживает угрозу и эмоциональную значимость; вентромедиальной префронтальной коре (vmPFC), участвующей в обучении безопасности и регулировании эмоций; и дорсолатеральной префронтальной коре (dlPFC), связанной с сознательным контролем и копингом. Они также исследовали область, называемую передней островковой корой, которая помогает интегрировать телесные ощущения с эмоциональными состояниями. Соотнося показатели мозга с оценками ПТСР, полученными как клиницистами, так и самими пациентами, исследователи искали паттерны, которые могли бы отличать людей, у которых в ходе исследования наблюдалось большее улучшение.
Что изменилось в мозге — и что не изменилось
Препарат, блокирующий FAAH, ясно выполнил свою биохимическую задачу: уровни анандамида в крови были выше у получавших его участников. Тем не менее, при сравнении групп «препарат» и «плацебо» существенных различий в покоящейся связности или в активации мозга во время задачи обнаружено не было. Желаемого усиления в цепях, связанных со страхом и эмоциями, просто не проявилось на сканах. Вместо этого выявились другие закономерности, связанные с тяжестью симптомов и степенью улучшения с течением времени, независимо от того, какую таблетку принимал человек.
У людей, которые на момент сканирования сообщали о более тяжёлом ПТСР, наблюдалась более сильная функциональная связь между vmPFC и обширными областями, связанными с вниманием, а также между миндалиной и областями, вовлечёнными в восприятие и движения тела. Более сильные связи между vmPFC и передней островковой корой также ассоциировались с более высокими самосообщаемыми симптомами. Интересно, что большее клиническое улучшение в течение всех 12 недель оказалось связано с более низкой активацией правой dlPFC во время задачи эмоционального конфликта и с ослабленной покоящейся связностью между vmPFC и той же областью dlPFC. Это предполагает, что пациенты, у которых в итоге наблюдалось большее улучшение, возможно, меньше полагались на усилия сознательного контроля и больше использовали другие, возможно более автоматические, формы эмоциональной обработки.
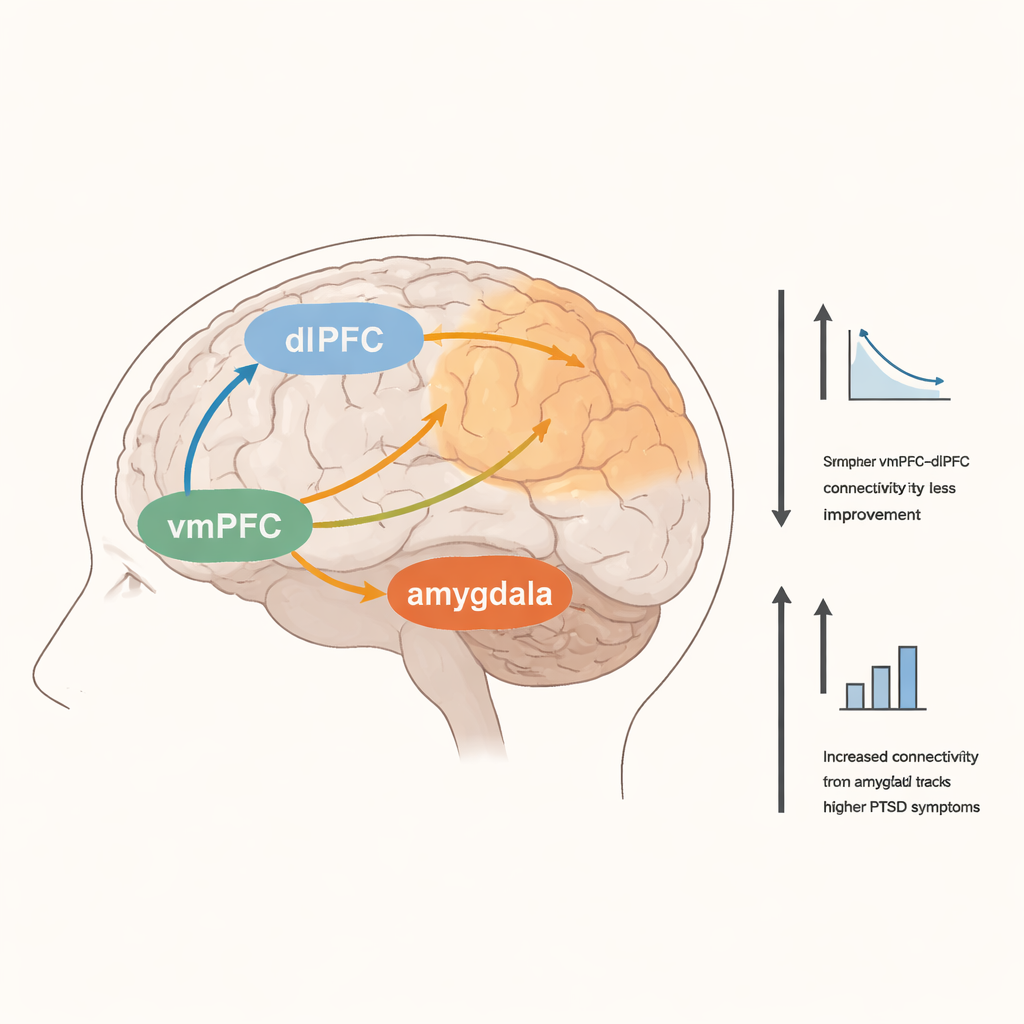
Что это значит для будущего лечения ПТСР
Ключевой вывод в бытовом изложении таков: простого повышения уровня одного из каннабиноидоподобных веществ мозга — анандамида — оказалось недостаточно, чтобы улучшить терапию или перестроить ключевые цепи страха и эмоций у людей с ПТСР, по крайней мере в этой преимущественно женской, некомбатной выборке. Однако исследование выделяет dlPFC как возможный маркер того, кто с большей вероятностью выиграет от экспозиционно-ориентированной терапии, и подчёркивает, что ПТСР включает широкие изменения в взаимодействии сетей эмоций и внимания. Для пациентов и клиницистов эти результаты служат напоминанием о том, что многообещающие идеи из исследований на животных и ранних человеческих работ не всегда прямо переносятся в эффективные лечения, и что понимание сложной реакции мозга на травму потребует взгляда за пределы одиночных химических мишеней в пользу паттернов всего мозга и индивидуальных различий.
Цитирование: Tansey, R., Perini, I., Petrie, G.N. et al. Functional neuroimaging of fatty acid amide hydrolase inhibition in posttraumatic stress disorder: a randomized clinical trial. Transl Psychiatry 16, 95 (2026). https://doi.org/10.1038/s41398-026-03864-3
Ключевые слова: ПТСР, эндоканнабиноид, ингибитор FAAH, функциональная МРТ, угашение страха