Clear Sky Science · ru
Модификация m6A, опосредованная METTL3, регулирует CDKN1A и ослабляет нарушение когнитивных функций и гибель нейронов, вызванные хроническим недосыпанием у крыс
Почему бессонные ночи могут вредить вашей памяти
Многие относятся к хронической потере сна как к нормальной части современной жизни, но наука показывает: недосып может незаметно повреждать области мозга, ответственные за обучение и память. В этом исследовании у крыс авторы проникают на уровень отдельных молекул внутри нейронов гиппокампа и выделяют конкретный химический переключатель — METTL3 — который, по-видимому, защищает клетки мозга от вредных последствий хронического недосыпания. Понимание этого механизма может в будущем указать пути для сохранения памяти у людей, которым трудно избежать потери сна, например у вахтовых рабочих, опекунов и пациентов с нарушениями сна.
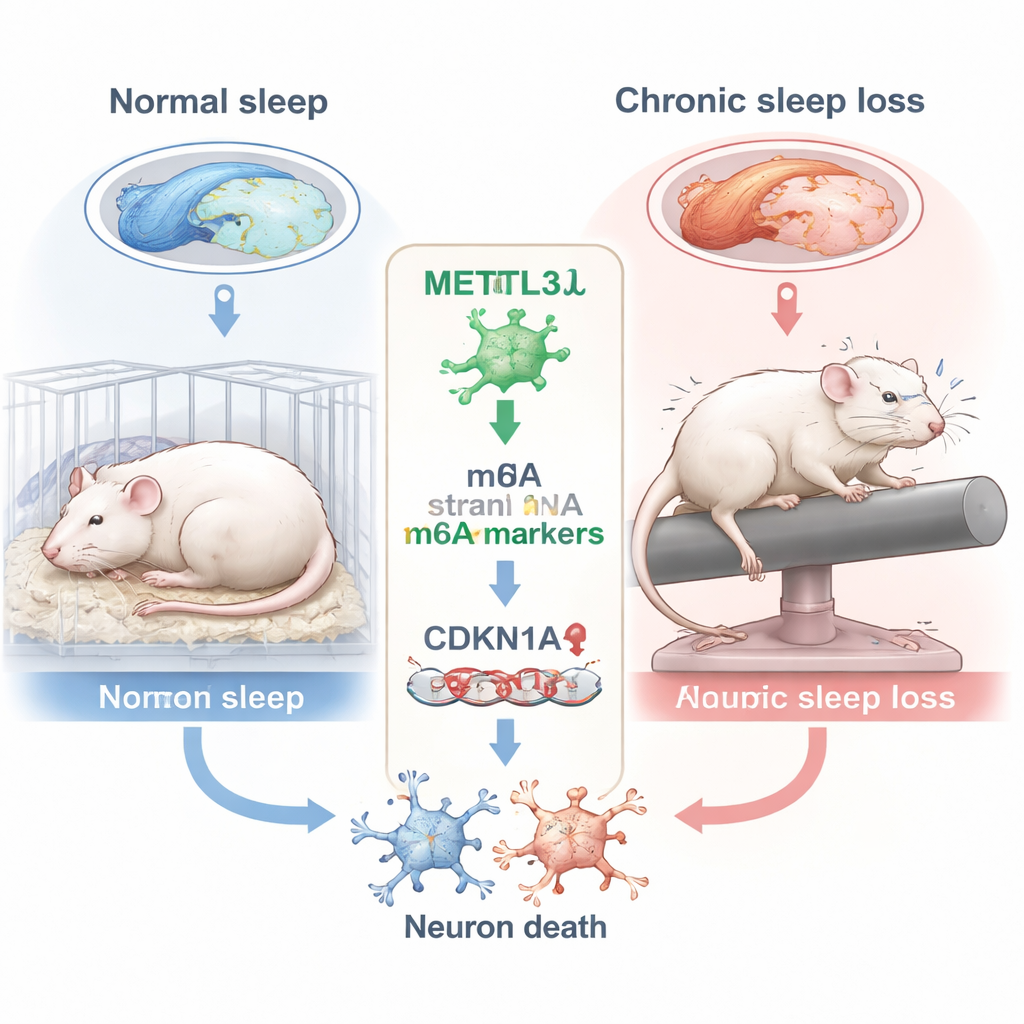
Как длительный недосып повреждает центр памяти
Исследователи сосредоточились на гиппокампе — области мозга в форме морского конька, необходимой для формирования новых воспоминаний. Внутри гиппокампа они подробно изучали подрегион CA3, который участвует в кодировании и извлечении пространственной информации — навыка, проверяемого задачами вроде поиска скрытой платформы в воде. Крыс будили по 10 часов в день в течение шести недель с помощью мягкого вращающегося валика, который неоднократно прерывал их сон. В тесте Морриса на способность ориентироваться в воде лишённые сна животные выбирали менее прямые маршруты, реже пересекали место прежней платформы и проводили меньше времени в целевом квадранте — всё это признаки ухудшения пространственной памяти по сравнению с хорошо выспавшимися животными.
Химический ярлык на РНК, который пропадает
Чтобы понять, что происходило внутри нейронов CA3, команда проанализировала химическую метку на РНК, известную как m6A — одну из наиболее распространённых внутренних меток на информационной РНК. Эти метки помогают контролировать, как долго молекулы РНК существуют и насколько эффективно они используются для синтеза белков. Ключевой фермент, добавляющий метки m6A, — METTL3. С помощью массового секвенирования m6A и анализа экспрессии генов учёные обнаружили, что хроническое недосыпание значительно снижает уровень METTL3 в области CA3. Это снижение подтвердили как на уровне РНК, так и на уровне белка. Паттерн затронутых генов указывал на нарушение контроля клеточного цикла и реакций на стресс, что намекало на то, что потеря сна может сдвигать нейроны в нездоровое состояние.
От молекулярных изменений к гибели нейронов
Чтобы увидеть, как снижение METTL3 влияет на нейроны непосредственно, исследователи использовали культуры гиппокампальных клеток мышей в чашках Петри. Когда они подавили METTL3 с помощью малых интерферирующих РНК, клетки стали значительно более уязвимы к повреждающему воздействию рапамицина — лекарства, создающего стресс для нейронов. В клетках с дефицитом METTL3 повысился уровень классических белков «клеточного самоубийства», таких как Bax и кливированный каспаз-3, а также больше клеток было отмечено как апоптотические при проточной цитометрии. Глубокий анализ РНК выявил один ключевой ген — CDKN1A (кодирующий белок p21): при подавлении METTL3 уровень CDKN1A резко возрастал.
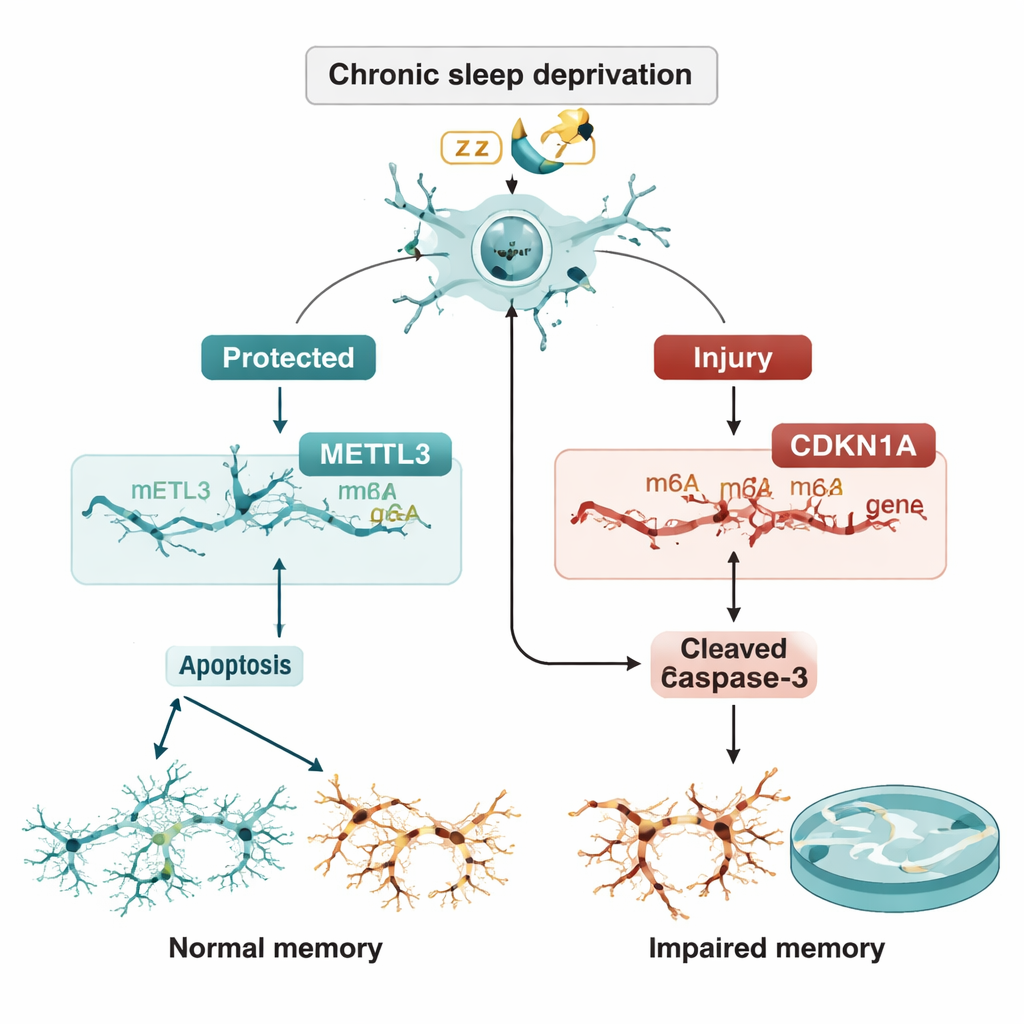
Хрупкое равновесие между защитой и самоуничтожением
Затем команда проверила, контролирует ли METTL3 CDKN1A через метки m6A. Они показали, что снижение METTL3 уменьшает количество меток m6A на РНК CDKN1A и делает эту РНК более стабильной, поэтому её уровень накапливается вместо того, чтобы разрушаться. Более высокий уровень CDKN1A, в свою очередь, тянет нейроны к апоптозу. Критически важно, что при подавлении самого CDKN1A дополнительная гибель клеток, вызванная потерей METTL3, в значительной мере обращалась вспять. В живых крысах введение дополнительного METTL3 непосредственно в область CA3 с помощью вирусного вектора снижало уровень CDKN1A, уменьшало содержание белков апоптоза, сохраняло структуру нейронов при окрашивании тканей и улучшало результаты в водном лабиринте, несмотря на продолжающийся недосып.
Что это значит для людей, которые не могут высыпаться
Проще говоря, хроническое недосыпание, по-видимому, подавляет защитный фермент METTL3 в критическом блоке памяти мозга. Когда METTL3 падает, он больше не может корректно помечать определённые РНК, особенно ту, что кодирует CDKN1A. Эта РНК затем накапливается, толкая нейроны к программируемой гибели и способствуя проблемам с памятью. Восстановление METTL3 позволяло снизить CDKN1A, уменьшить потерю нейронов и восстановить память у лишённых сна крыс. Несмотря на то что работа пока проведена на животных, она выделяет путь METTL3–CDKN1A как перспективную мишень для будущих препаратов, направленных на защиту мозга от когнитивных последствий хронической потери сна.
Цитирование: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Ключевые слова: хроническое недосыпание, гиппокамп, метилирование РНК, апоптоз нейронов, нарушение памяти