Clear Sky Science · ru
Разнообразные и локально‑специфичные роли PlexinA2, PlexinA4 и NCAM в формирующихся ворсинчатых волокнах гиппокампа
Как нервные пути формируют цепи памяти
Гиппокамп, область мозга, критичная для формирования и извлечения воспоминаний, формируется из тонких нервных волокон, которые в раннем возрасте должны точно ориентироваться. Это исследование задаёт на первый взгляд простейший вопрос: как растущие волокна узнают, куда именно идти — и что происходит, когда их система ориентировки даёт сбой, что может способствовать таким состояниям, как шизофрения, аутизм или эпилепсия?
Две магистрали в центр памяти
Внутри гиппокампа нейроны в области, называемой зубчатой извилиной, посылают длинные отростки — ворсинчатые волокна — в область CA3. По входе в CA3 эти волокна обычно разделяются на две отдельные «магистрали»: одна пролегает над слоем тел клеток CA3, другая — под ним. Каждая магистраль соединяется с разными частями клеток CA3 и помогает устанавливать баланс активности в этой цепи памяти. Если эти пути не разделяются должным образом, волокна могут оказаться не в тех местах и нарушить поток информации через гиппокамп.
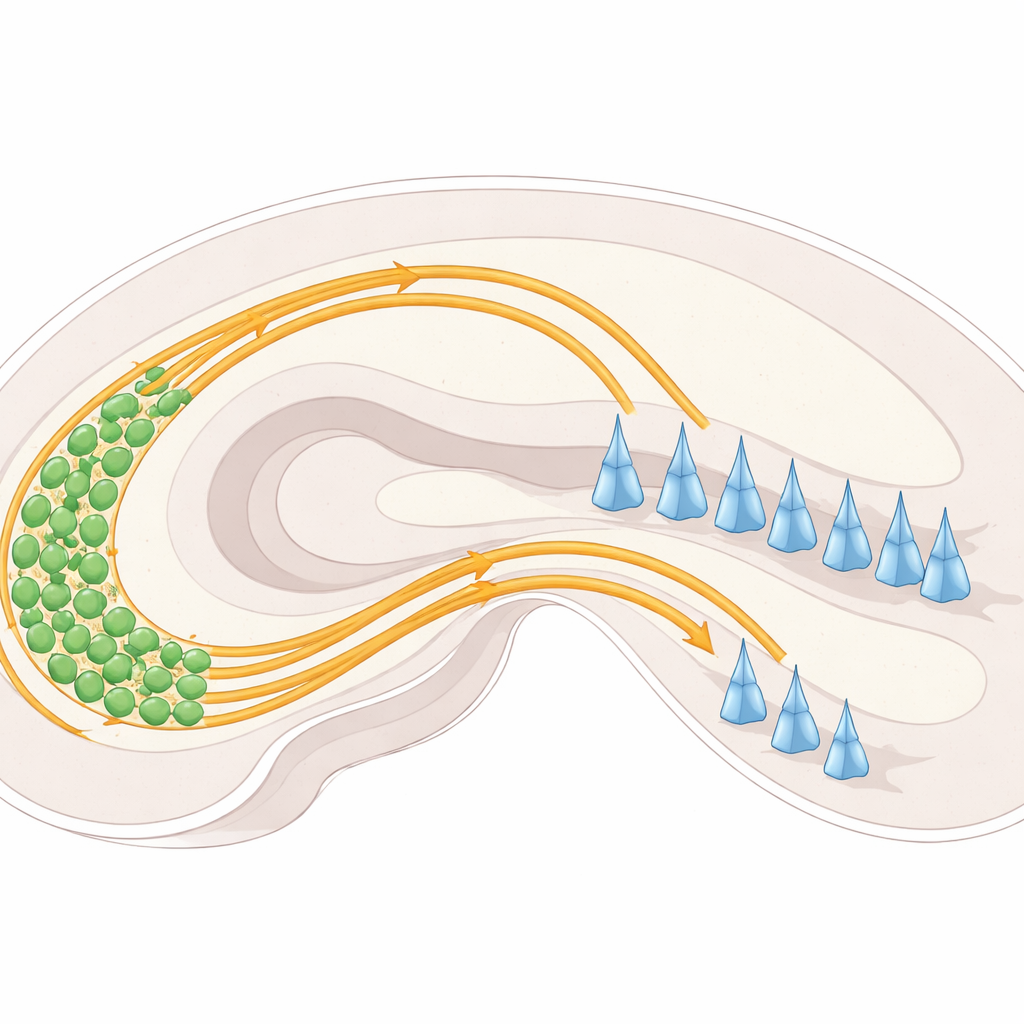
Навигационные сигналы: отталкивание, притяжение и клеточная «ручка»
Исследователи сосредоточились на наборе молекулярных ориентиpов и поверхностных «ручек» на нейронах, которые направляют ворсинчатые волокна. Семейство белков, называемых плексинами (PlexinA2 и PlexinA4), располагается на поверхности нейронов и реагирует на партнёрные молекулы — семафорины, в частности Sema6A. Эти взаимодействия могут работать как сигналы «въезд запрещен», отталкивая волокна от определённых регионов, либо тонко регулировать, насколько прочно соседние волокна слипляются друг с другом. Другой поверхностный белок, NCAM, ведёт себя скорее как липучка, способствуя адгезии и помогая сращиваться пучкам волокон. Изучая, где эти белки экспрессируются и что происходит при их удалении или изменении у мышей, команда картировала их кооперацию в живом мозге, а не только в изолированных клетках.
Разделение ролей с помощью дизайнерских мышей
Чтобы выделить роль каждого компонента, учёные создали и комбинировали 27 различных линий мышей. Некоторые полностью лишались Sema6A, другие — PlexinA2 или PlexinA4, а в ещё некоторых были внесены тонкие точечные мутации, отключающие лишь специфическое «ферментативное ядро» плексинов, сохраняя остальную часть молекулы. Также они выборочно удаляли Sema6A или NCAM только в определённых типах клеток, например в гранулярных клетках зубчатой извилины, чтобы проверить, где сигнал действительно важен. У мышей, у которых Sema6A отсутствовал в этих гранулярных клетках, ворсинчатые волокна не разделялись чисто на верхний и нижний пучки, а нижний пучок перерастал и заходил дальше обычной точки остановки. Похожие, но не тождественные ошибки проводки наблюдались у мышей без PlexinA2 или PlexinA4, что показало: эти белки действуют на разных контрольных этапах одного и того же пути.
Углубление в механизмы и партнёрства
Когда авторы отключили каталитическое ядро PlexinA4, многие — но не все — те же дефекты, что и при полном нокауте PlexinA4, снова проявились. Это показало, что PlexinA4 часто опирается на это ядро, чтобы перестраивать внутренний цитоскелет растущих волокон, помогая им правильно формировать пучки и останавливаться на нужном слое. PlexinA2 оказался иным: некоторые его функции зависели от каталитического ядра, а другие — нет, что указывает на дополнительные, неферментативные пути сигнализации. Затем команда применила технику пометки соседних белков для выявления молекул, находящихся рядом с PlexinA2 в молодых нейронах гиппокампа. Вышли на несколько молекул клеточной адгезии, среди которых выделилась NCAM. Снижение экспрессии как PlexinA2, так и NCAM одновременно вызывало более выраженные ошибки траектории ворсинчатых волокон, чем уменьшение любого из них по‑отдельности, что показывает: эти две системы сотрудничают — NCAM обеспечивает адгезию, тогда как отталкивающие сигналы, исходящие от PlexinA2, калибруют разделение волокон на верхние и нижние дорожки и степень вырастания нижней дорожки.
Когда сигналы работают в обратном направлении
Что примечательно, Sema6A действует не только как внешний «знак», читаемый плексинами; он также может выступать приёмником на самих ворсинчатых волокнах. Исследователи изучали мышей, у которых удалён внутренний хвост Sema6A при сохранённой внешней части. У этих животных некоторые дефекты ориентации сохранялись — особенно перерастание нижнего пучка — что указывает на то, что сигналы, идущие внутрь через хвост Sema6A («обратная сигнализация»), необходимы для нормальной обрезки и формирования ворсинчатых волокон. Этот обратный режим, по‑видимому, работает наряду с более привычной плексин‑опосредованной сигнализацией в зависимости от стадии и локализации.
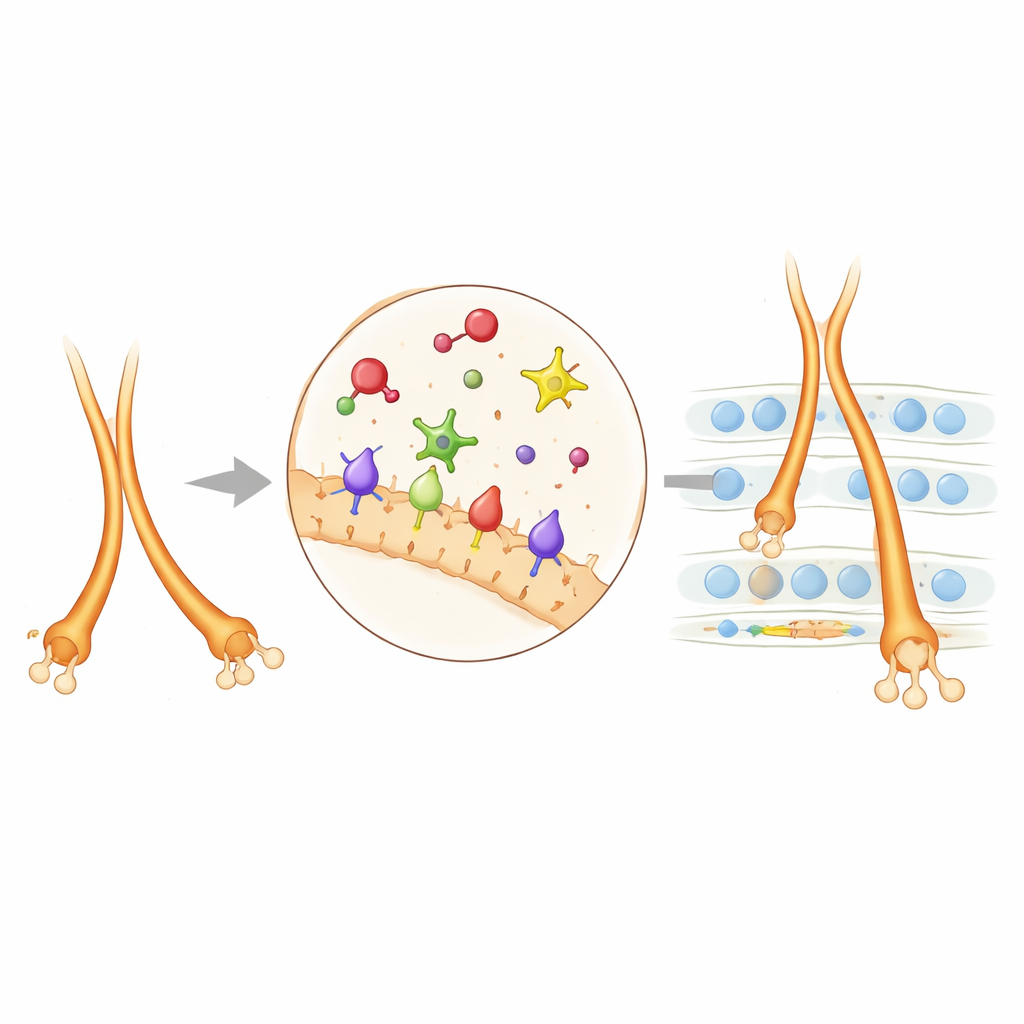
Почему эта проводка важна для здоровья мозга
Мутации в человеческих версиях PLXNA2, SEMA6A и NCAM1 связывали с нейроразвивательными и психиатрическими состояниями — от умственной отсталости до шизофрении и аутизма. Показывая, как именно эти молекулы сотрудничают при формировании ворсинчатых путей у мышей, исследование предлагает конкретную модель того, как тонкие генетические изменения могут нарушать образование, разделение и обрезку ключевых цепей памяти. Проще говоря, работа показывает, что набор инструментов ориентировки мозга использует точно скоординированную смесь сигналов «отталкивания», «притяжения» и «липучести» для построения схемы проводки гиппокампа — и что даже небольшие сбои в этом наборе могут привести к изменениям в обучении, памяти и психическом здоровье.
Цитирование: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Ключевые слова: ворсинчатые волокна гиппокампа, навигация аксонов, семафорин‑плексин сигналы, NCAM и клеточная адгезия, нарушения нейроразвития