Clear Sky Science · ru
Дисфункция ГАМКергических интернейронов лежит в основе изменённых нейронных сетевых осцилляций, связанных с эпилептиформной активностью у мышей с дефицитом PPT1
Когда мозговые ритмы дают сбой
Припадки — это не просто внезапные бури активности мозга; они часто развиваются из тонких изменений в том, как нейроны общаются друг с другом. В этом исследовании рассматривается редкое детское заболевание мозга — болезнь CLN1 — и задаётся простой, но далеко идущий вопрос: что происходит с внутренними «хронометристами» мозга, когда отсутствует один фермент, PPT1? Прослеживая эти изменения у мышей с течением времени, учёные показывают, как небольшие ранние нарушения ингибиции могут перерасти в припадки и широкомасштабное повреждение мозга.
Стражи баланса мозга
Наш мозг опирается на два крупных типа нейронов. Возбуждающие клетки, такие как пирамидальные нейроны гиппокампа, продвигают активность вперёд. Тормозящие клетки, называемые интернейронами, действуют как тормоза, сдерживая эту активность и формируя электрические ритмы мозга. Среди них два важных класса — интернейроны, положительные по парвальбумину (PV+), и интернейроны, положительные по соматостатину (SST+). Они помогают генерировать и координировать ритмические колебания мозга, такие как тета- и гамма-осцилляции, которые поддерживают функции, например обучение и память. При болезни CLN1 у детей отсутствует фермент PPT1, который обычно удаляет жирные группы с белков. Авторы использовали модель мыши с той же мутацией, что и у пациентов, чтобы выяснить, как потеря PPT1 влияет на интернейроны и ритмы мозга, которые они регулируют.
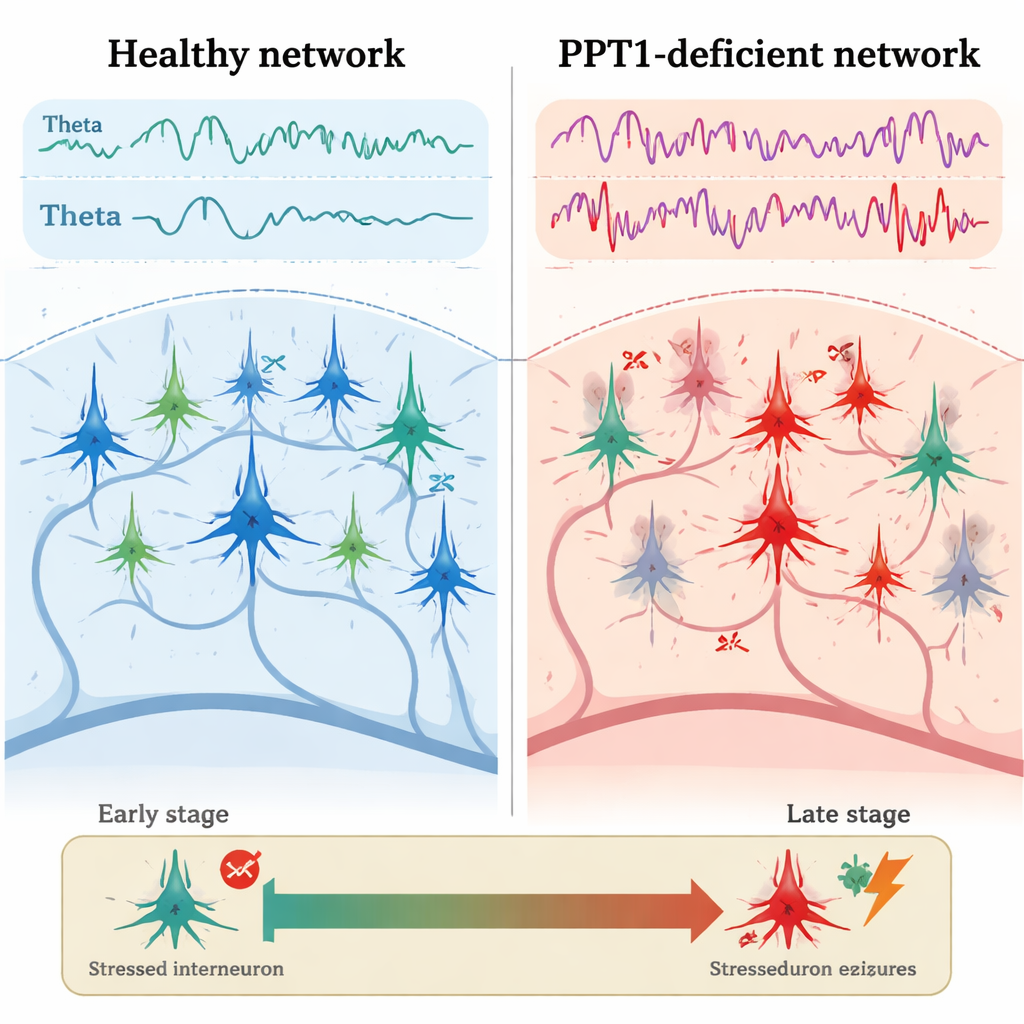
Ранние трещины в системе ингибиции
У молодых взрослых мутантных мышей, примерно трёх-четырёх месяцев, первая очевидная проблема проявилась в PV+ интернейронах. Электрические записи из гиппокампа показали, что эти тормозящие клетки генерировали импульсы реже, чем у здоровых мышей, в то время как соседние пирамидальные нейроны стреляли чаще и с более короткими паузами между спайками. Микроскопия выявила, что у многих PV+ интернейронов активировался каспаза-3, ключевой исполнитель программируемой смерти, хотя их общее число ещё не уменьшилось. Одновременно увеличилась мощность тета- и гамма-колебаний, а кальциевое изображения показало усиление активности нейронов гиппокампа во время перемещений животных. Важно, что нормальное «взаимодействие» между тета- и гамма-ритмами — когда более медленные волны помогают упорядочить более быстрые — ослабло, что указывает на ранний сбой в тонком временном согласовании сетевой активности.
От нарушенных ритмов к припадочным вспышкам
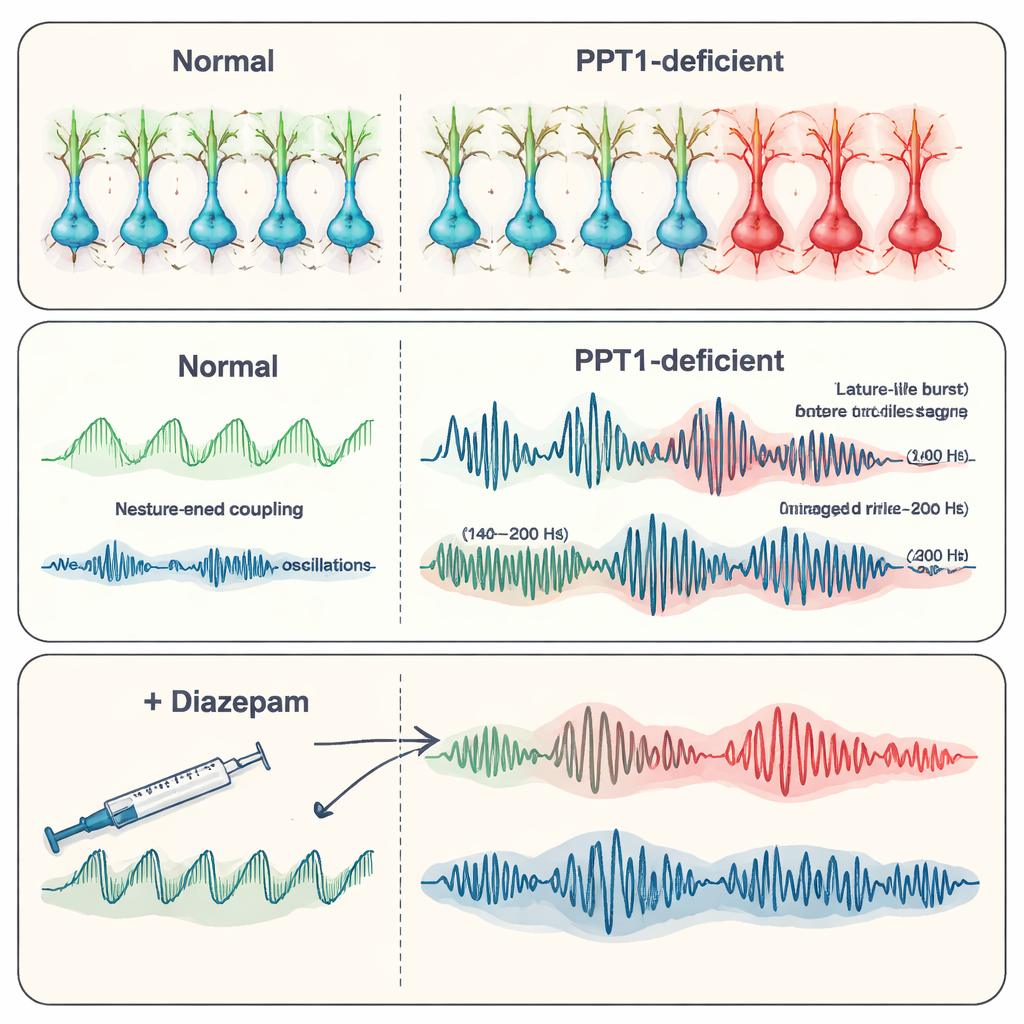
К шести-семи месяцам состояние ухудшилось. Многие PV+ интернейроны исчезли, и теперь у SST+ интернейронов также появились признаки активации каспазы-3. Записи из гиппокампа выявили спонтанные эпилептиформные разряды — краткие аномальные вспышки активности, связанные с припадками. Команда сосредоточилась на высокочастотных «рипплах» — быстрых осцилляциях, которые обычно участвуют в консолидации памяти. У мутантных мышей физиологические рипплы (приблизительно 140–200 герц) стали реже, но большего амплитудного роста, тогда как ещё более быстрые «патологические» рипплы (200–500 герц), тесно связанные с эпилепсией, усилились и стали встречаться чаще. В совокупности эти изменения указывают на смещение от организованных, связанных с памятью ритмов к хаотичным, склонным к припадкам паттернам по мере утраты ингибиторного контроля.
Нейроны изнашиваются и диазепам вмешивается
По мере прогрессирования болезни гиппокамп начал деградировать. Кальциевые сигналы в нейронах уменьшились, окраска по Гольджи показала более тонкие и менее ветвистые дендритные деревья, и стало меньше маленьких шипиков, где формируются синапсы. Подсчёты нейронов в ключевых областях гиппокампа (CA1 и CA3) подтвердили широкомасштабную потерю клеток, и в электрических записях регистрировалось меньше активных единиц. Исследователи затем опробовали диазепам, широко используемый противоэпилептический препарат, который усиливает действие тормозного нейромедиатора ГАМК. У старших мутантных мышей диазепам уменьшал частоту эпилептических разрядов и частично восстанавливал более нормальные осцилляционные паттерны, включая поведение рипплов, хотя не устранял утрату рецепторов. Это указывает на то, что усиление оставшихся ингибирующих сигналов всё ещё способно успокоить сеть, по крайней мере временно.
Почему эти результаты важны
Для непрофессионального читателя главный вывод таков: болезнь CLN1 — это не просто накопление отходов в клетках мозга. Потеря PPT1 запускает цепную реакцию: сперва специализированные ингибирующие интернейроны испытывают стресс и начинают отказывать, что приводит к гиперактивности пирамидальных нейронов и искажению ритмов мозга. Со временем этот дисбаланс вызывает припадки и в конечном счёте приводит к масштабной утрате клеток и связей. Исследование указывает на окно возможностей на ранней стадии болезни, когда защита или восстановление PV+ интернейронов — возможно, путём блокирования активации каспаз — может предотвратить последующие припадки и дегенерацию. Хотя диазепам не лечит CLN1, его способность подавлять аномальные ритмы в этой модели подчёркивает более общую идею: восстановление ингибиции может быть мощной стратегией при эпилепсии и родственных расстройствах мозга.
Цитирование: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Ключевые слова: эпилепсия, интернейроны, гиппокамп, мозговые осцилляции, лиsozомная накопительная болезнь