Clear Sky Science · ru
Ранние функциональные изменения и плазменный GFAP в шведских семьях с мутациями аутосомно-доминантной болезни Альцгеймера
Почему это исследование важно для семей
Болезнь Альцгеймера часто кажется приходящей внезапно, но на самом деле вредные изменения в мозге накапливаются бесшумно в течение многих лет. В редких семьях с наследуемыми («аутосомно-доминантными») мутациями Альцгеймера учёные могут предсказать, когда вероятно начнутся симптомы, и проследить ранние изменения. В этом исследовании наблюдали шведские семьи с такими мутациями, чтобы понять, как использование энергии мозгом, когнитивные способности и кровяной маркер клеток поддержки мозга (GFAP) меняются задолго до появления проблем с памятью — и как эти изменения различаются в зависимости от гена.
Отслеживание «часов болезни» в семьях с высоким риском
Поскольку у людей с аутосомно-доминантной болезнью Альцгеймера (ADAD) симптомы обычно развиваются в относительно предсказуемом возрасте, исследователи могут вычислить «оценочные годы до начала симптомов» (EYO) — сколько лет человек находится до или после ожидаемого начала заболевания. Команда изучила 45 взрослых из шведских семей с мутациями в генах APP или PSEN1, а также родственников без мутаций. В среднем более семи лет участники проходили сканирование мозга, измеряющее, сколько глюкозы использует мозг (FDG PET), подробные тесты на мышление и память и, у подгруппы, анализы крови на GFAP — белок, высвобождаемый, когда поддерживающие клетки мозга, называемые астроцитами, становятся реактивными. Такой дизайн позволил учёным выстроить различные биологические изменения вдоль общего временного ряда болезни, а не просто сравнивать людей в один момент времени.
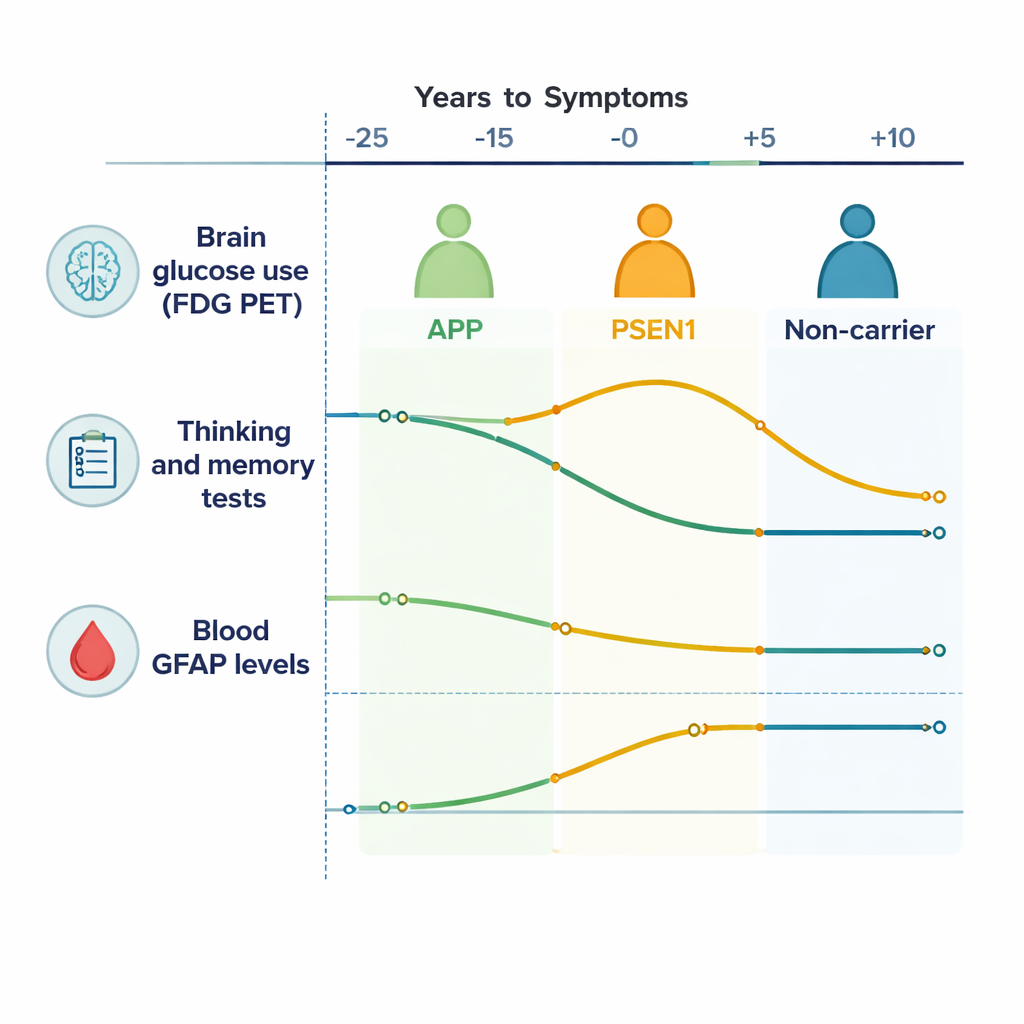
Отслеживание энергетики мозга и мышления во времени
По всей коре головного мозга у носителей мутаций Альцгеймера наблюдалось постепенное снижение сигнала FDG PET по сравнению с родственниками без мутаций — то есть их мозг с течением времени использовал меньше глюкозы, что является признаком нарушения работы нервных клеток. Подкорковые области глубоко в мозге, особенно хвостатое ядро и таламус, также демонстрировали снижение активности, главным образом у носителей мутаций APP. Тесты на мышление и память ухудшались в нескольких областях, включая эпизодическую память и познавательную гибкость, начиная примерно за 10–15 лет до ожидаемого начала симптомов. Другими словами, даже когда люди ещё ощущали себя и функционировали нормально в повседневной жизни, чувствительные тесты и сканы показывали, что их мозг уже работал с трудом и менее эффективно.
Разные паттерны при разных генах Альцгеймера
Ключевой вывод заключался в том, что две основные группы мутаций — APP и PSEN1 — не следовали одинаковым траекториям. У носителей PSEN1 исследователи наблюдали ранний период, примерно за 20–10 лет до ожидаемых симптомов, когда в некоторых участках мозга фактически фиксировалось необычно высокое потребление глюкозы («гиперметаболизм»), сопровождавшееся лучшими результатами в тестах, прежде чем последовало снижение. Это, вероятно, отражает временную фазу компенсации, когда мозг и его поддерживающие клетки увеличивают активность, чтобы справиться с нарастающим повреждением. Носители APP, напротив, демонстрировали более прямолинейное и постепенное падение метаболизма мозга без этого раннего всплеска. Эти специфичные для генов паттерны указывают на то, что «болезнь Альцгеймера» — не единая биологическая история, даже в наследуемых формах, а семейство родственных процессов, разворачивающихся по-разному в зависимости от исходной мутации.
Что показывает анализ крови о раннем стрессe мозга
GFAP, измеряемый в простом образце крови, открывал окно в реакцию астроцитов на ранние изменения, связанные с Альцгеймером. Уровни GFAP, как правило, повышались по мере приближения человека к ожидаемому возрасту появления симптомов как у носителей мутаций, так и у не-носителей, но взаимосвязи между GFAP, метаболизмом мозга и когнитивными показателями были специфичны для гена. У носителей APP более высокий GFAP связывался с падением потребления глюкозы в глубоких областях мозга и с ухудшением результатов по большинству когнитивных тестов, что указывает на тесную связь активации астроцитов с ранним повреждением и потерей функции. У носителей PSEN1 эти связи были слабее или отсутствовали, что вновь указывает на разные биологические пути, ведущие к одному клиническому итогу — деменции.
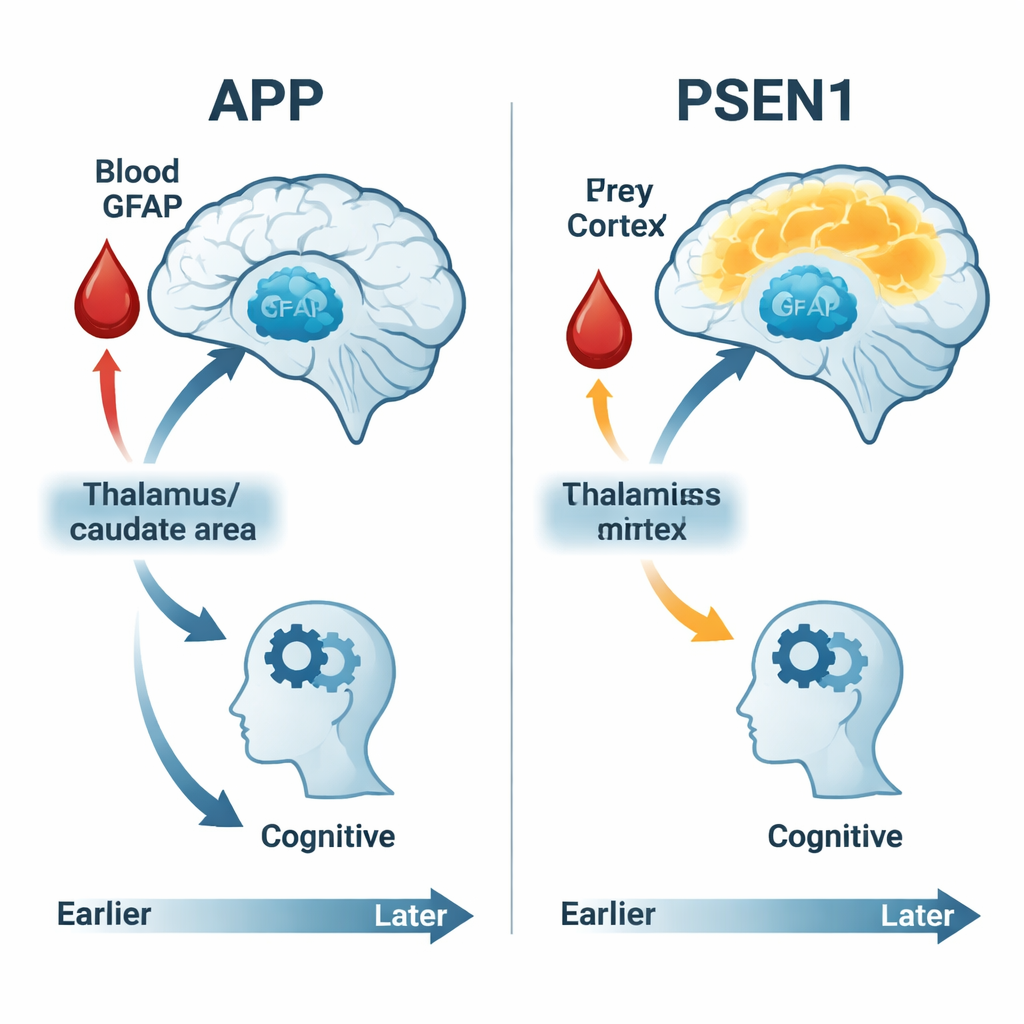
Что это значит для раннего обнаружения и лечения
Для неспециалиста основной посыл таков: в этих семьях с высоким риском изменения, связанные с Альцгеймером, начинаются за десятилетия до явной потери памяти — и они не одинаковы для всех. Сканирование потребления глюкозы мозгом, детализированные когнитивные тесты и один маркер в крови, такой как GFAP, вместе могут выявить, когда мозг начинает испытывать трудности и как быстро прогрессирует это напряжение. Важно, что люди с разными генетическими формами Альцгеймера показывают разные последовательности изменений: у некоторых сначала наблюдается фаза повышенной активности, у других — стабильное снижение, а маркер стресса астроцитов сильнее связан с повреждением в одних группах, чем в других. Признание этих различных траекторий может помочь лучше адаптировать будущие препараты и клинические испытания к нужным людям в нужный момент, а также подтверждает перспективу использования анализов крови, таких как GFAP, для более раннего выявления болезни Альцгеймера — до того, как симптомы лишат людей независимости.
Цитирование: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Ключевые слова: аутосомно-доминантная болезнь Альцгеймера, биомаркер GFAP в крови, метаболизм глюкозы в мозге, астроциты и нейродегенерация, раннее выявление болезни Альцгеймера