Clear Sky Science · ru
Подавление митохондриального производства энергии пептидом купредоксина из фотосинтезирующей бактерии тормозит рост опухолей
Преобразование бактерий в борцов с раком
Раковые клетки жадны до энергии. Они полагаются на крошечные внутренние «электростанции» — митохондрии, которые вырабатывают энергию, необходимую для роста, распространения и устойчивости к лечению. В этом исследовании рассматривается неожиданный союзник в борьбе с раком: короткий фрагмент белка, изначально найденного в фотосинтезирующих бактериях. Исследователи показывают, что этот дизайнерский пептид может проникать в раковые клетки, отключать их источник энергии и существенно усиливать эффект радиотерапии — при этом в значительной мере избегая повреждения нормальных клеток.
Крошечный пептид с большой задачей
Команда исходила из предыдущего открытия, что бактериальный белок азурин может замедлять рост опухолей, действуя через хорошо известный супрессор опухолей p53. Затем они изучали бактерии, обитающие вблизи человеческих опухолей, сосредоточив внимание на фотосинтезирующих микробах, которые используют свет для получения энергии. Эти бактерии несут родственный семейство белков — купредоксины. Сравнивая их структуры и эволюционную историю, исследователи выделили один купредоксин — аурацианин B — и вырезали из него короткий участок длиной 28 аминокислот, который назвали aurB. Этот фрагмент хорошо растворим в воде, может пересекать клеточные мембраны и имеет форму, указывающую на возможное взаимодействие с ключевыми компонентами клеточной энергетики.
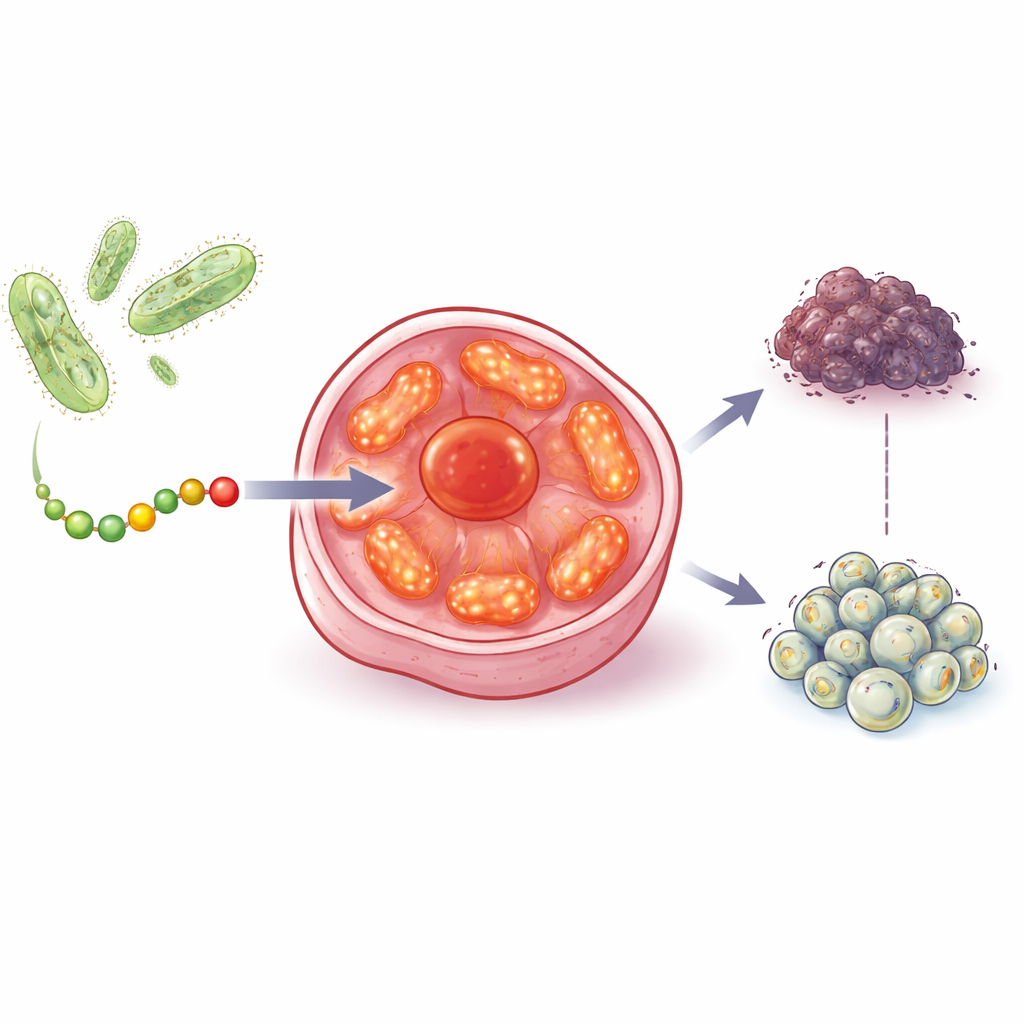
Нахождение и поражение энергетических центров рака
В лабораторных тестах aurB снижал выживаемость линий клеток рака молочной, предстательной, толстой кишки и яичников, даже когда в этих клетках отсутствовал функциональный p53 или гормональные рецепторы, необходимые для многих современных препаратов. Важно, что aurB оказывал гораздо более слабое воздействие на нормальные клетки простаты, сердца и мышц, хотя эти здоровые клетки богаты митохондриями. Визуализационные эксперименты показали, что aurB преимущественно проникает в раковые клетки и затем концентрируется в их митохондриях. Электронная микроскопия с использованием aurB, присоединённого к крошечным золотым меткам в качестве визуального маркера, подтвердила накопление пептида внутри этих органелл.
Перекрытие поставок энергии
Попав в митохондрии, aurB связывался с конкретным компонентом АТФ-синтазы — молекулярной турбины, производящей АТФ, основной энергетической валюты клетки. Биохимические эксперименты по вытягиванию комплексов и масс-спектрометрия идентифицировали партнёра как ATP5C, часть центрального ядра фермента. Измерения методом поверхностного плазмонного резонанса показали, что aurB прочно связывается с ATP5C с умеренной аффинностью и медленным диссоциированием, что согласуется со стабильным взаимодействием. Функциональные анализы затем выявили последствия этого связывания: aurB резко снижал митохондриальный уровень АТФ в клетках рака простаты, замедлял потребление кислорода и блокировал как респирацию, так и запасной путь — гликолиз. По мере краха производства энергии раковые клетки демонстрировали признаки программируемой гибели, опосредованной каспазой-3, ключевым ферментом‑«исполнителем».
Остановка опухолей и усиление действия радиации
Далее исследователи проверили aurB в мышиных моделях агрессивного рака простаты. У животных с подкожно имплантированными человеческими опухолями регулярные инъекции aurB уменьшали рост опухолей примерно на две трети — сопоставимо или лучше, чем химиотерапевтический препарат паклитаксел, но без заметной потери веса или признаков стресса. Образцы опухолей из обработанных мышей содержали меньше делящихся клеток и значительно больше умирающих клеток. Во второй модели, имитирующей метастазирование в кость — частое и смертельное проявление рака простаты — aurB в одиночку замедлял рост опухоли в кости ноги и уменьшал число метастазов в лёгких. Однако при комбинировании с умеренной дозой облучения эффект оказался драматическим: опухоли в обработанной конечности почти полностью исчезли, а число лёгочных метастазов сократилось более чем на 90 процентов по сравнению с контролем.
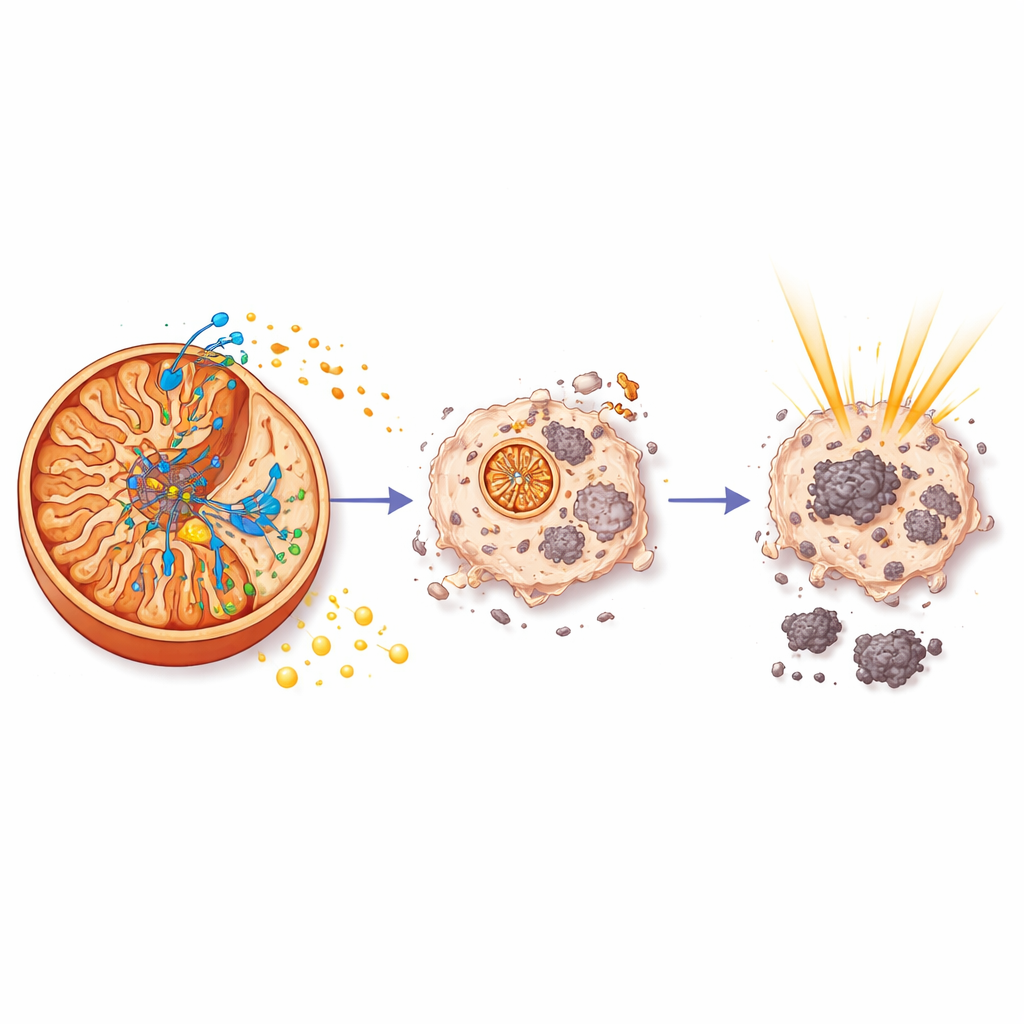
Почему энергия важна для радиотерапии
Чтобы понять, почему aurB делает радиацию более эффективной, команда изучила активность генов в опухолях обработанных мышей. Они обнаружили, что aurB, в отличие от одного только облучения, подавлял сеть генов, контролируемых HIF‑1 — главным регулятором, который помогает раковым клеткам адаптироваться к низкому уровню кислорода и способствует устойчивости к лечению. В условиях энергического дефицита, вызванного aurB, ключевые пути роста и выживания, управляемые PI3K и c‑Myc, оказались ослабленными, а гликолитический механизм, позволяющий опухолям выживать в жестких условиях, также подавлялся. По сути, путём саботажа производства АТФ непосредственно на митохондриальной турбине aurB ввергал раковые клетки в энергетический кризис, делая их значительно более уязвимыми к повреждению радиацией.
Новый класс точечных блокаторов энергии
Эта работа предлагает новую стратегию в терапии рака: разработку небольших пептидов, вдохновлённых бактериальными белками, которые нацеливаются на митохондриальные энергетические системы, изменённые в опухолях. AurB, полученный из белка фотосинтезирующей бактерии, селективно нацелен на компонент АТФ‑синтазы, часто гиперактивный при таких опухолях, как рак простаты, молочной железы, яичников и мозга. Путём прямого лишения раковых клеток энергии и ослабления их защитных механизмов, особенно против радиации, такие пептиды могут дополнять существующие подходы и предлагать опции там, где иммунные методы оказываются малоэффективны. Хотя перед клиническим применением предстоит ещё много работы, исследование демонстрирует, что древние бактериальные энергетические белки могут быть переосмыслены как современные, высокоточечные противораковые инструменты.
Цитирование: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
Ключевые слова: митохондриальная АТФ-синтаза, метаболизм рака, терапевтические пептиды, рак простаты, сенсибилизация к облучению