Clear Sky Science · ru
Сигнальный путь циклического гуанозинмонофосфата — протеинкиназы G ослабляет кальцификацию аортального клапана через аутофагию, опосредованную ULK1
Почему «ржавчина» сердечного клапана имеет значение
С возрастом аортальный клапан — главный выходной клапан сердца — может постепенно становиться жестким и покрываться кальцием, состояние, называемое кальцифицирующим заболеванием аортального клапана. Это «окаменение» заставляет сердце работать сильнее и может приводить к боли в груди, обморокам, сердечной недостаточности или необходимости замены клапана хирургическим путем. В настоящее время нет лекарства, которое надежно замедляло бы этот процесс; врачи могут лишь ждать, пока клапан не будет серьёзно поврежден, и затем оперировать. В этом исследовании изучается встроенный клеточный путь, который, как кажется, защищает клапан от кальцификации, и проверяется современное лекарство для лечения сердечной недостаточности как возможный способ восстановить эту защиту.
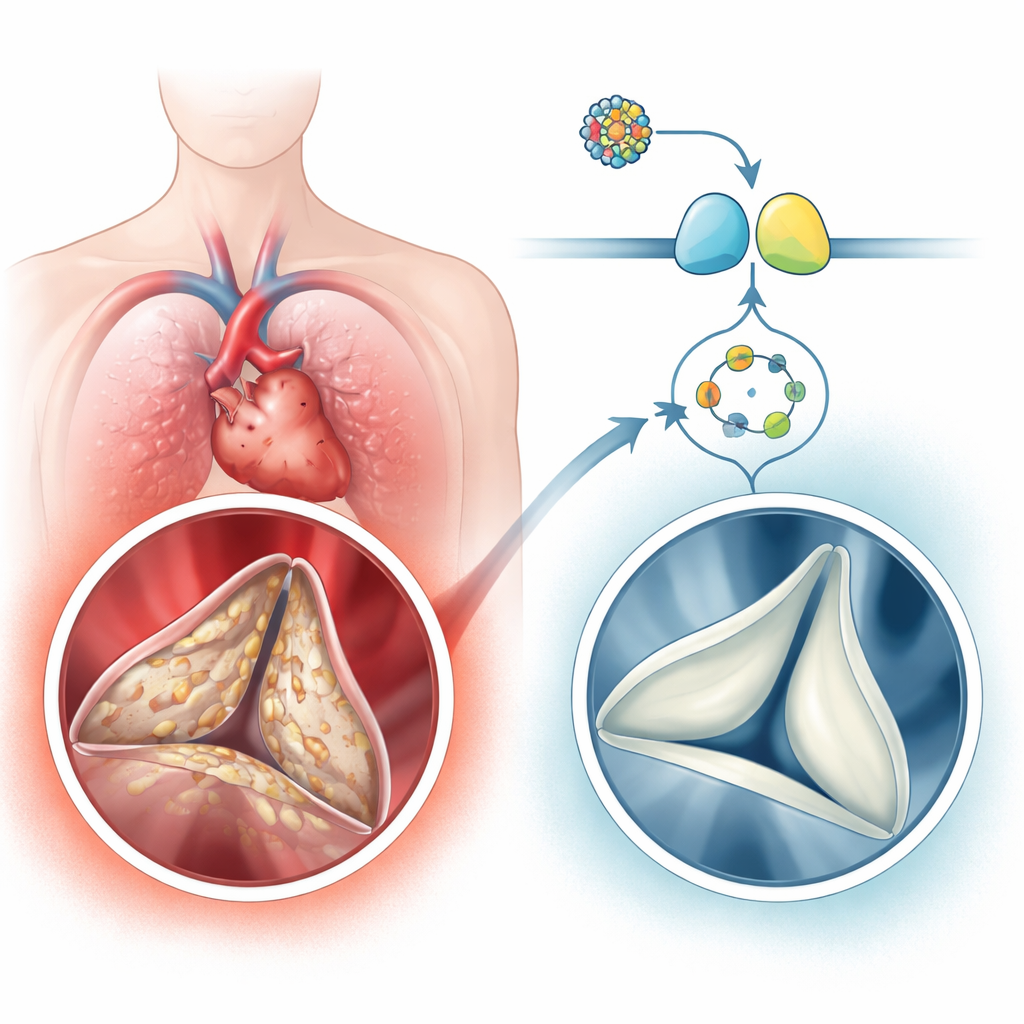
Распространенная, но недооцененная сердечная проблема
Кальцифицирующее заболевание аортального клапана удивительно часто встречается у пожилых людей: оно поражает несколько процентов лиц старше 65 лет и до одного из десяти старше 75 лет. Заболевание — это не просто пассивный «износ». Мягкие клетки соединительной ткани клапана, известные как вальвулярные интерстициальные клетки, переходят в состояние, напоминающее заживление ран и образование кости. Они откладывают лишний коллаген, а затем накапливают кальций, превращая когда‑то гибкие створки в жесткие, камнеподобные пластины. Авторы проанализировали ткань человеческих клапанов и крупные наборы данных экспрессии генов и обнаружили, что сигнальная ветвь, основанная на малой молекуле cGMP и ее партнерном ферменте протеинкиназе G (PKG), последовательно ослаблена в кальцифицированных клапанах, тогда как гены и белки, связанные с формированием кости, были активированы. У людей с выраженной кальцификацией клапана также были снижены уровни cGMP в крови, что коррелировало со степенью сужения и обструкции клапана.
Защитный сигнал, который исчезает
Чтобы проверить причинно‑следственную связь, команда использовала мышей и культивированные человеческие клетки клапана. Мыши, генетически модифицированные с пониженным уровнем PKG, развивали более утолщенные и интенсивно кальцифицированные створки клапана после контролируемой травмы аортального клапана, и в их клапанах были повышены уровни ключевого белка, определяющего формирование кости. В человеческих клетках клапана, выращенных в чашке Петри в условиях, способствующих накоплению кальция, снижения активности PKG с помощью генетических инструментов ускоряло этот костеподобный переход. Эти результаты указывают на то, что сигнальная система cGMP–PKG обычно действует как тормоз вредной перепрограммировке клеток в клапане — и когда этот тормоз ослабевает, кальцификация ускоряется.
Переназначение лекарства от сердечной недостаточности
Далее исследователи задали вопрос, может ли усиление этого пути замедлить или обратить кальцификацию. Они испытали три препарата, повышающие уровень cGMP разными способами, включая верицигуат — одобренное лекарство для определенных пациентов с сердечной недостаточностью. Во всех трех препаратах наблюдалось уменьшение отложений кальция и маркеров костеподобного превращения в человеческих клетках клапана, при этом верицигуат проявил наибольший эффект. Верицигуат также снизил кальцификацию в крошечных кусочках человеческой клапанной ткани, поддерживаемой живой вне организма. В двух моделях на мышах — одна вызвана диетой с повышенным содержанием холестерина, другая — механическим повреждением клапана — ежедневное лечение верицигуатом привело к образованию более тонких, менее кальцифицированных створок и улучшенному кровотоку через клапан, без ослабления сократительной функции сердца. Однако при генетическом снижении PKG эффективность верицигуата в основном исчезала, что указывает на то, что PKG является ключевым звеном вниз по потоку.
Клеточная уборка — здоровые клапаны
Глубже исследование показало, что верицигуат и PKG защищают крошечные энергостанции клеток клапана — митохондрии. В условиях, приводящих к кальцификации, клетки накапливали повреждающие реактивные формы кислорода, теряли мембранный потенциал митохондрий и вырабатывали меньше энергии. Верицигуат восстановил функцию митохондрий и снизил окислительный стресс. Масштабное картирование белков и фосфорилирования подвело исследователей к аутофагии — внутриклеточной системе очистки и переработки. В кальцифицированных человеческих клапанах микроскопия и белковые маркеры показали сниженное образование и активность аутофагосом — «мусорных мешков» аутофагии. В одно‑клеточных анализах несколько подтипов клеток клапана из больных клапанов демонстрировали широкое подавление программ, связанных с аутофагией. В культивированных клетках блокада аутофагии устраняла защитный эффект активации PKG, что подразумевает, что PKG в значительной степени действует через восстановление этой системы очистки.
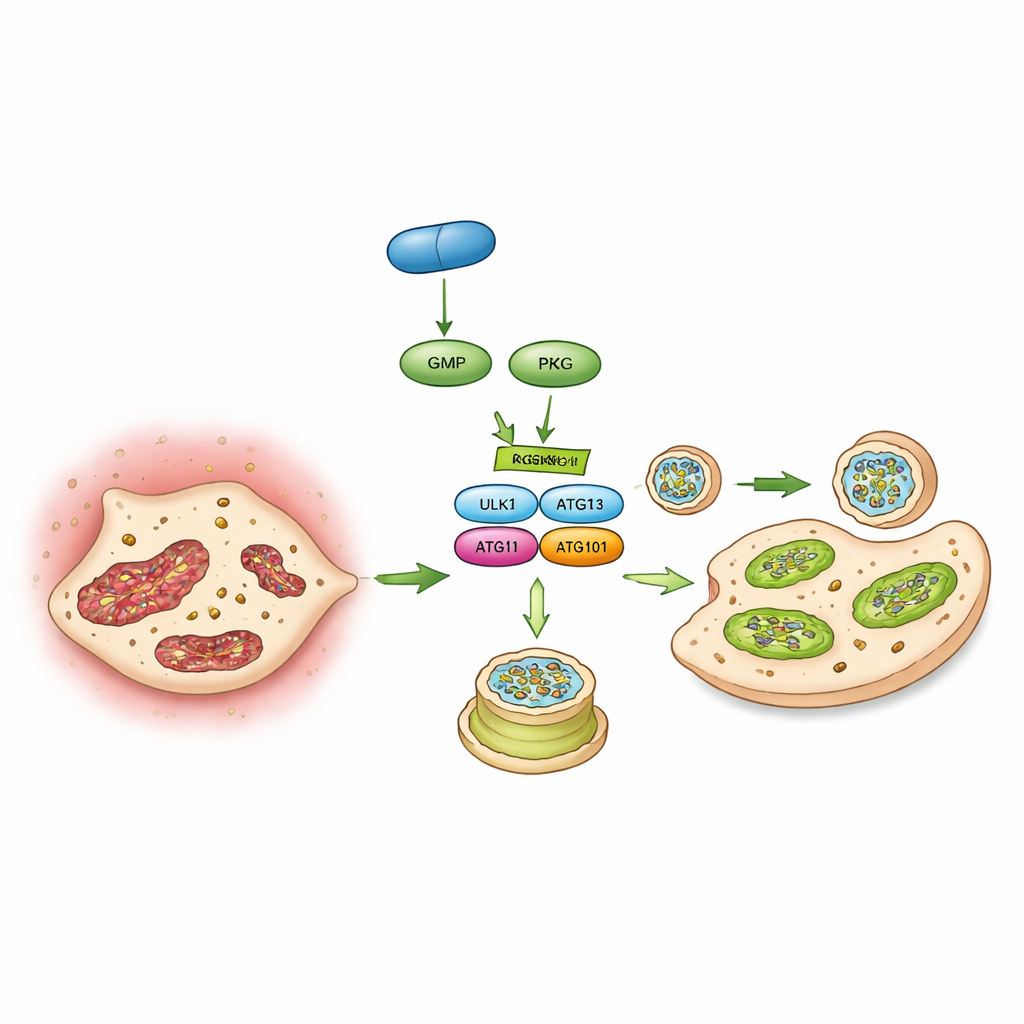
Переключатель на молекулярном уровне
Наконец, авторы определили конкретный молекулярный переключатель, который связывает PKG с аутофагией: белок ULK1, запускающий формирование аутофагосом. С помощью фосфопротеомики, исследований взаимодействий и тестов in vitro на активность киназы они показали, что PKG непосредственно фосфорилирует ULK1 в определенном месте (аминокислоте серин 556). Когда это место было мутировано так, что его уже нельзя было модифицировать, PKG переставал усиливать аутофагию и блокировать кальцификацию в клетках клапана. У мышей индуцированная экспрессия этого нечувствительного варианта ULK1 в клетках клапана также уничтожала способность верицигуата защищать клапан. В совокупности эти данные описывают цепочку событий: верицигуат стимулирует cGMP, который активирует PKG, который переключает ULK1, что возобновляет аутофагию, сохраняет митохондрии и предотвращает превращение клеток клапана в костеподобные клетки.
Что это может означать для пациентов
Эта работа позиционирует ось cGMP–PKG–ULK1–аутофагия как встроенную систему защиты от «ржавления» аортального клапана. При кальцифицирующем заболевании клапана эта защита ослабевает, позволяя клеткам накапливать повреждения и склоняться к костеподобной идентичности. Фармакологическое восстановление сигнала с помощью препарата, уже применяемого в клиниках при сердечной недостаточности, замедлило кальцификацию в нескольких экспериментальных моделях. Хотя для валидации в клинике при заболевании клапана потребуются исследования на людях, исследование предлагает четкую, проверяемую идею: аккуратное усиление этой клеточной системы очистки может однажды отсрочить или уменьшить необходимость замены клапана у пожилых пациентов с риском аортального стеноза.
Цитирование: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Ключевые слова: кальцифицирующее заболевание аортального клапана, сигнализация cGMP PKG, верицигуат, аутофагия, кальцификация сердечного клапана