Clear Sky Science · ru
Эффективность и иммуномодулирующий эффект имуноускоренных CAR-T-клеток, специфичных к Claudin18.2 и секретирующих IL-7/XCL1, при раке пищеварительного тракта: доклинический и клинический анализ
Обращение иммунной системы против опухолей пищеварительного тракта
Рак желудка и поджелудочной железы входят в число самых смертоносных опухолей, отчасти потому что часто не поддаются хирургии, химио- и радиотерапии. В этом исследовании изучается новый способ борьбы с этими опухолями — усиление собственных иммунных клеток организма, чтобы они могли проникать в солидные опухоли, выживать там и привлекать подкрепления. Перепроектируя Т‑лимфоциты для выделения полезных иммунных сигналов, авторы стремятся не только непосредственно атаковать опухоль, но и пробудить остальную иммунную систему внутри враждебной для нее опухолевой среды.
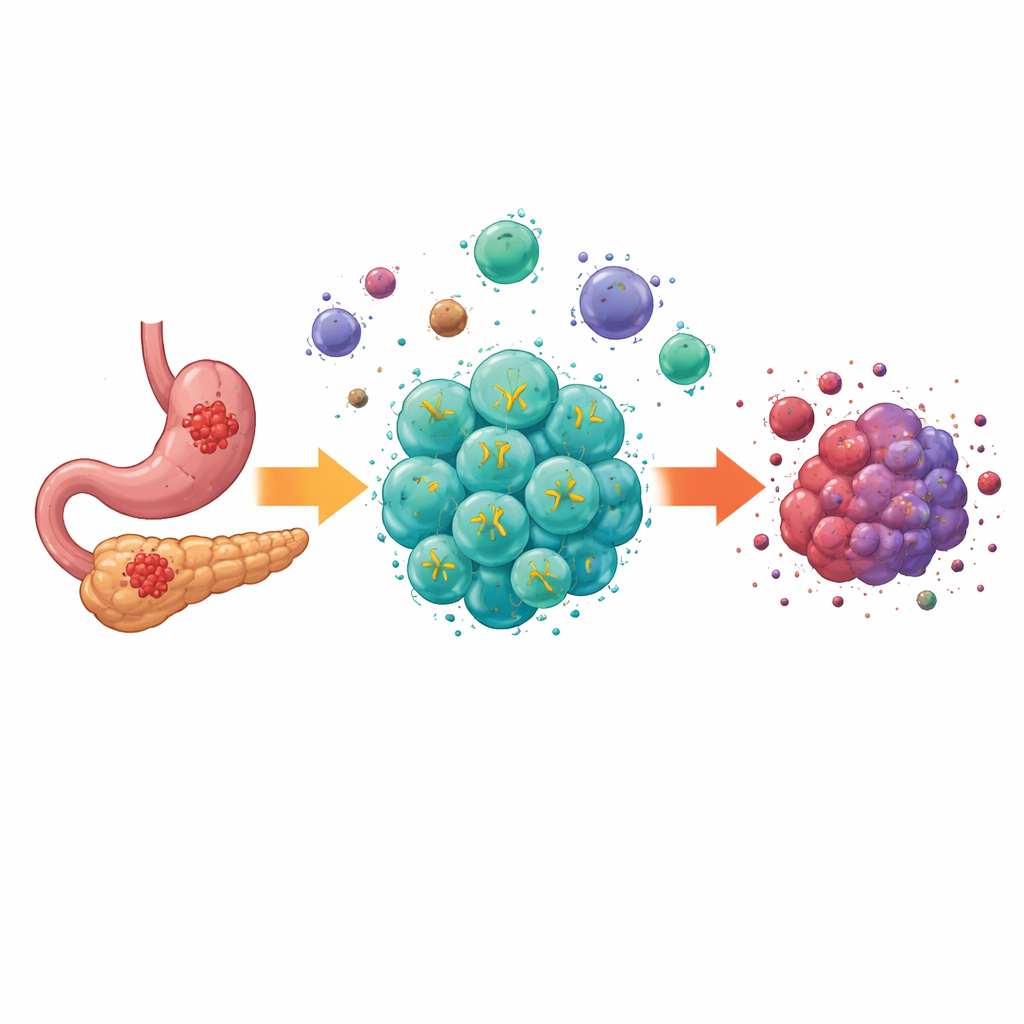
Почему солидные опухоли трудно лечить
Современные клеточные терапии, называемые CAR‑T, дали впечатляющие результаты при гемопоэтических злокачественных новообразованиях, излечивая некоторых пациентов, у которых не было других вариантов. Но солидные опухоли, в том числе опухоли пищеварительного тракта, создают дополнительные препятствия. Их клетки неоднородны по пространству, внутренняя часть опухоли лишена питательных веществ и кислорода, а сочетание подавляющих клеток и сигнальных молекул притупляет иммунную атаку. Ранние поколения CAR‑T могли распознавать целевые молекулы на раковых клетках пищеварительного тракта, но часто не умели эффективно расширяться, сохраняться и функционировать в этой суровой среде, что ограничивало их клинический эффект.
Более умная конструкция инженерных Т‑клеток
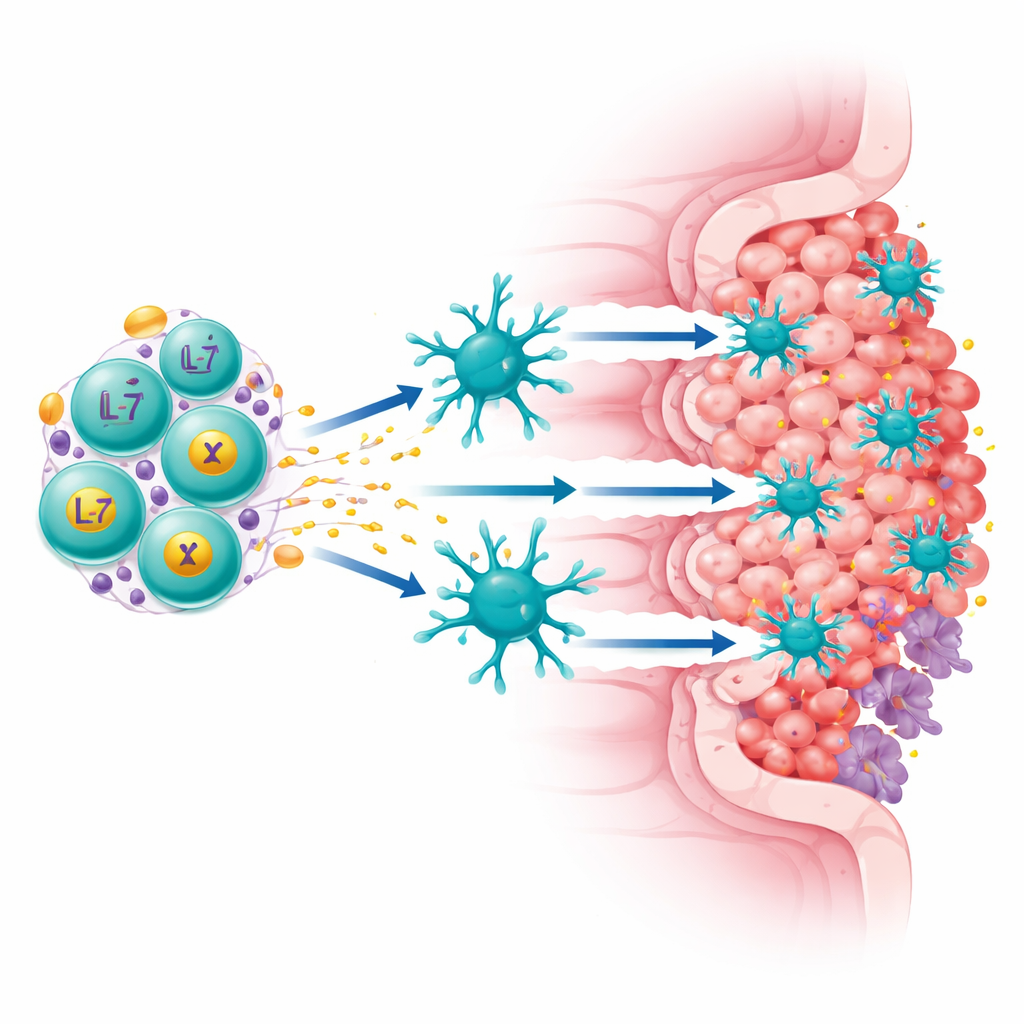
Исследователи сосредоточились на белке Claudin18.2, который выражается в больших количествах на многих клетках рака желудка и поджелудочной железы, но в нормальных тканях почти отсутствует. Они создали «четвертое поколение» CAR‑T‑клеток, выполняющих две задачи одновременно: распознавание Claudin18.2 на опухолевых клетках и постоянную секрецию двух иммуноподдерживающих факторов — IL‑7 и XCL1. IL‑7 помогает Т‑клеткам выживать и поддерживать долговременное, стволоподобное состояние, тогда как XCL1 служит маяком для привлечения редкого, но мощного типа дендритных клеток cDC1, особенно эффективных в активации киллерных Т‑клеток. Эти усовершенствованные клетки, названные ExCAR‑T или RD07, спроектированы не просто для уничтожения увиденных целей, но и для перестройки иммунной среды опухоли.
Мощный контроль опухоли в доклинических моделях
В мышиных моделях раков пищеварительного тракта ExCAR‑T проявили себя лучше, чем обычные CAR‑T, лишенные IL‑7 и XCL1. В лабораторных культурах инженерные клетки убивали больше раковых клеток и содержали больше долговременных клеток памяти, похожих на стволовые. У животных с опухолями, положительными по Claudin18.2, лечение ExCAR‑T глубже уменьшало размеры опухолей и продлевало выживаемость по сравнению со стандартными CAR‑T. Усиленные клетки лучше расширялись в крови и вызывали более широкую иммунную активность, включая сигналы, привлекающие дополнительные иммунные клетки, при одновременном снижении факторов, связанных с метастазированием. Впечатляюще, мыши, излеченные ExCAR‑T, отвергли повторную инъекцию раковых клеток, лишенных мишени Claudin18.2, что указывает на то, что терапия вызвала длительную иммунную память против всего панорамы опухоли, а не узконаправленный ответ только на один антиген.
Ранние результаты клинического испытания у пациентов
Воодушевленные этими данными, исследователи запустили первое в человеке испытание RD07 у 12 пациентов с прогрессирующим раком желудка, локализацией в гастроэзофагеальном переходе или раком поджелудочной железы, которым уже не помогли стандартные методы лечения. Побочные эффекты в целом контролировались: наиболее серьезные проблемы были связаны с падением показателей крови из‑за прединфузионной химиотерапии, наблюдались только легкие реакции высвобождения цитокинов; серьезных токсичностей со стороны центральной нервной системы не было. Среди 10 пациентов, поддававшихся оценке, у 7 наблюдалось измеримое уменьшение опухоли, у 2 — частичный ответ. Пациенты с умеренным и высоким уровнем Claudin18.2 в опухолях особенно хорошо отвечали: у всех таких пациентов отмечалась по крайней мере стабилизация заболевания, а некоторые жили значительно дольше ожидаемого. У ответивших модифицированные Т‑клетки сильнее расширялись в крови, а уровни IL‑7 и XCL1 в плазме повышались, что соответствовало замыслу терапии.
Заглядывая внутрь иммунного микроокружения опухоли
Чтобы понять, как действует RD07 у людей, команда исследовала образцы опухоли на уровне отдельных клеток до и после лечения. Они увидели уменьшение доли Claudin18.2‑положительных раковых клеток у ответивших пациентов, подтверждающее, что терапия достигает целевой мишени. Одновременно отмечено расширение разнообразных клонов Т‑клеток, в том числе активных киллерных и тканево‑резидентных клеток памяти, что свидетельствует о более широкой иммунной атаке. Специализированные дендритные клетки демонстрировали признаки повышенной активности и усиленных взаимодействий с пролиферирующими Т‑клетками, согласуясь с ролью XCL1 в их привлечении в опухоль. Изображения среза опухоли одного пациента показали меньше опухолевых и подавляющих миелоидных клеток после лечения, больше Т‑ и В‑клеток и реорганизацию ткани в зоны, насыщенные иммунными клетками — признаки «более горячего», воспаленного микроокружения.
Что это может значить для будущей терапии рака
В совокупности доклинические и ранние клинические данные указывают, что RD07 делает больше, чем просто добавляет очередной таргетный препарат к арсеналу против рака. Сочетая распознавание опухоли с встроенной иммунной поддержкой, эти инженерные Т‑клетки могут дольше выживать, привлекать ключевых партнеров и помогать обучать собственную иммунную систему пациента контролировать опухоль, даже если первоначальная мишень теряется. Хотя испытание было небольшим и проводилось среди пациентов с множественной предварительной терапией, последовательное уменьшение опухолей, приемлемая безопасность и глубокая перестройка иммунитета выглядят многообещающими. При подтверждении в больших исследовательских программах этот подход может открыть новую главу в лечении опухолей пищеварительного тракта, где укрепление иммунной экосистемы внутри опухоли становится столь же важным, как и начальная атака на раковые клетки.
Цитирование: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Ключевые слова: терапия CAR-T клетками, рак пищеварительного тракта, опухолевая микроокружение, Claudin18.2, иммунотерапия