Clear Sky Science · ru
M6A-модифицированный circArhgap26 ослабляет ишемически‑реперфузионное повреждение сердца, подавляя пальмитоилирование плакопкиллина‑1
Почему важно защищать сердце после инфаркта
Когда у человека случается инфаркт, врачи стремятся как можно скорее восстановить проходимость закупоренной артерии и вернуть кровоток. Этот спасительный шаг сохраняет жизни, но у него есть и обратная сторона: внезапное возвращение крови может дополнительно повредить сердце — явление, известное как ишемическо‑реперфузионное повреждение. В этом обзоре рассматривается неожиданный природный защитник внутри сердечных клеток — кольцевая РНК circArhgap26, которая помогает оградить сердечную мышцу от этой вторичной волны повреждений. Понимание того, как работает эта маленькая молекула, может указать путь к новым методам лечения и анализам крови для больных сердечными заболеваниями.
Скрытое кольцо в генетическом тексте сердца
Большинство из нас представляют гены как прямые цепочки ДНК и РНК, но клетки также синтезируют кольцевые молекулы РНК, называемые circular RNA, которые отличаются повышенной стабильностью и способны тонко регулировать многие клеточные процессы. Исследователи искали в сердцах мышей кольцевые РНК, уровни которых меняются при повреждении, и сфокусировались на одной — circArhgap26, уровень которой резко падал при прекращении и последующем восстановлении кровотока. Они подтвердили, что эта РНК действительно образует замкнутую петлю, в основном локализуется в цитоплазме и не служит матрицей для синтеза белка. Вместо этого она, по-видимому, действует как регулятор, взаимодействуя с другими молекулами и влияя на то, выживет ли кардиомиоцит или погибнет после стресса. 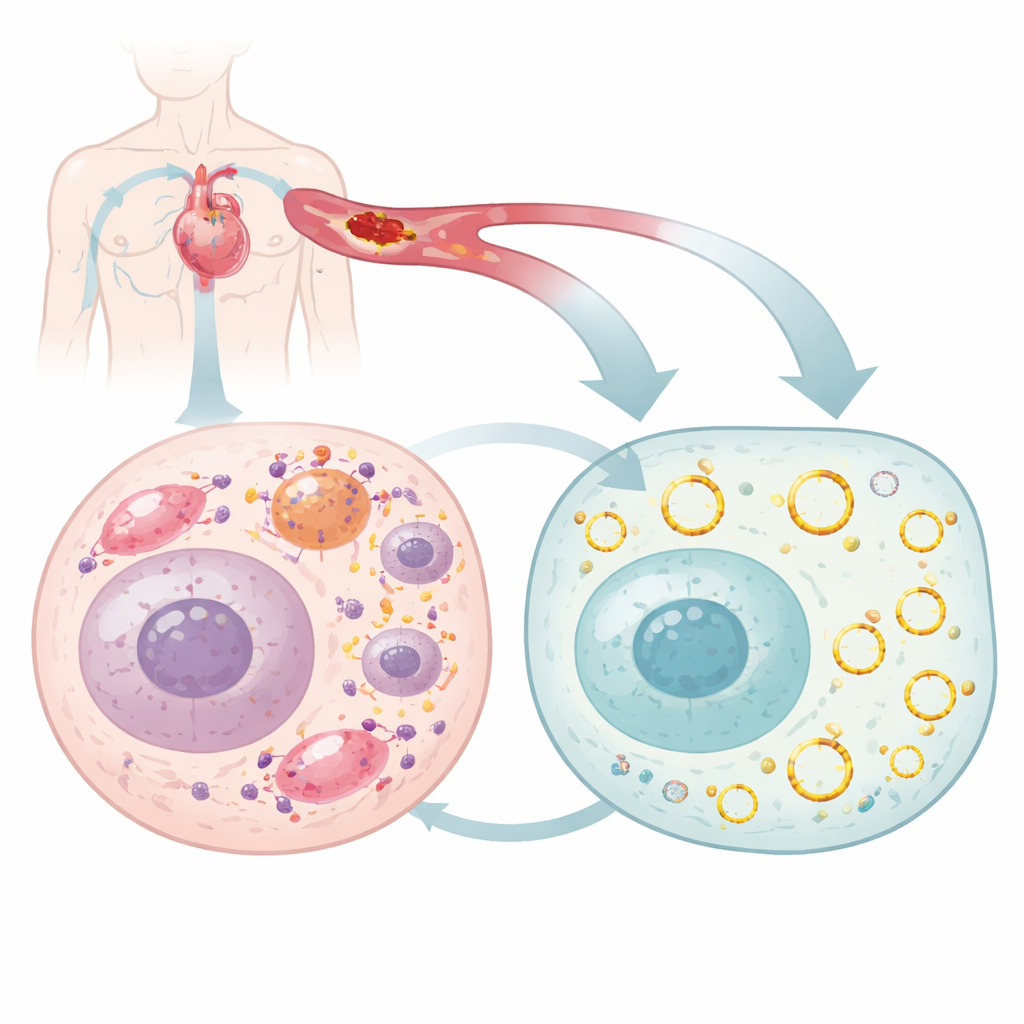
Доказательства защитной роли кольцевой РНК
Чтобы выяснить функцию circArhgap26, команда либо повышала, либо снижала её уровни в сердцах мышей. При использовании вирусного вектора для повышения экспрессии circArhgap26 специально в кардиомиоцитах у животных с временной окклюзией коронарной артерии и последующим восстановлением кровотока наблюдалась более сильная сократительная функция сердца, меньшие зоны повреждения и меньше клеток, подвергшихся гибели. Классические биомаркеры повреждения в крови и ткани сердца также были снижены. Обратный эффект отмечали при заглушении этой кольцевой РНК: даже без искусственно вызванного инфаркта функция сердца ухудшалась, увеличивался уровень клеточной гибели, и эти проблемы усугублялись при добавлении ишемии‑реперфузии. Похожие защитные эффекты были получены и в лабораторных моделях человеческих кардиомиоцитов, что указывает на консервацию механизма между мышами и людьми.
Вредный белок‑партнёр под контролем
Углубившись в механизм, исследователи выяснили, как circArhgap26 обеспечивает защиту. С помощью биохимических «рыболовных» подходов они обнаружили, что она напрямую связывается со структурным белком плакопкиллин‑1 (PKP1), который влияет на адгезию клеток и на их склонность к программируемой гибели. В повреждённых сердцах и при стресс‑нагрузках уровни PKP1 повышались и ассоциировались с худшими исходами. Заглушение PKP1 снижало повреждение и клеточную гибель, в то время как вынужденная экспрессия усугубляла ситуацию. При увеличении уровня circArhgap26 количество белка PKP1 уменьшалось несмотря на отсутствие изменений на уровне транскрипции, что указывает на посттранскрипционный контроль. Эксперименты показали, что circArhgap26 ускоряет деградацию белка PKP1, мешая жирорастворимой модификации — пальмитоилированию, которая обычно стабилизирует PKP1.
Молекулярная перетягивание каната вокруг сигналов смерти
Пальмитоилирование выполняется семейством ферментов; один из них, ZDHHC1, оказался ответственным за присоединение жирных групп к PKP1 и тем самым увеличивал его стабильность. CircArhgap26 связывается с тем же участком PKP1, который использует ZDHHC1, создавая молекулярную борьбу за место. Когда выигрывает кольцевая РНК, к PKP1 прикрепляется меньше жирных меток, он становится менее стабильным и быстрее деградирует. Это запускает каскад: PKP1 обычно усиливает синтез другого белка, APAF1, взаимодействуя с контролирующим участком его РНК. APAF1 — ключевой компонент машины, активирующей каспазу‑9 и каспазу‑3, центральных исполнителей клеточной смерти. При снижении стабильности PKP1 продукция APAF1 уменьшается, сигналы запуска апоптоза ослабляются, и кардиомиоциты с большей вероятностью выживают при восстановлении кровотока. 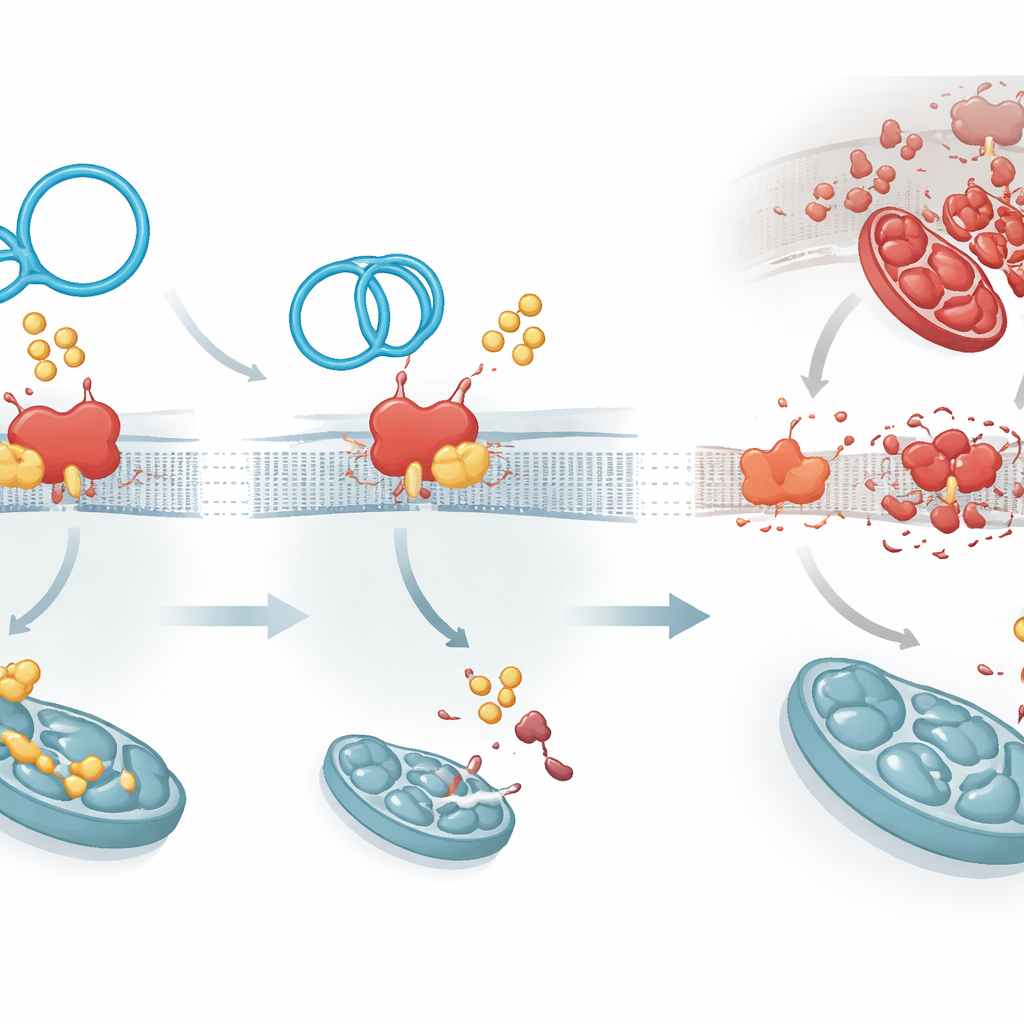
Тонкая настройка кольца и его потенциал для пациентов
Исследование также показывает, как сам circArhgap26 подавляется при повреждении. На эту кольцевую РНК в стрессовых сердцах накапливается распространённая химическая метка на РНК — m6A. Рецепторный белок YTHDF2 распознаёт эту метку и способствует деградации circArhgap26, ослабляя естественную защиту сердца именно в момент, когда она наиболее нужна. Важно, что человеческая версия этой кольцевой РНК очень похожа на мышиную и её уровень заметно ниже в крови пациентов, проходящих процедуры по восстановлению проходимости артерий, по сравнению со здоровыми добровольцами. В сумме полученные данные указывают, что восстановление или имитация действия circArhgap26 может служить и маркером риска в крови, и новым терапевтическим подходом. Проще говоря, работа выявляет небольшую кольцевую молекулу, действующую как страж против реперфузионного повреждения, обезвреживая смертельную цепную реакцию внутри сердечных клеток.
Цитирование: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Ключевые слова: ишемическо‑реперфузионное повреждение, кольцевая РНК, инфаркт миокарда, апоптоз кардиомиоцитов, РНК‑терапия