Clear Sky Science · ru
Синергия хемо‑ и фототермальной терапии пробуждает антитуморный иммунитет через ферроптоз
Превращая тепло и свет тела в оружие против рака
Химиотерапевтические препараты могут уменьшать опухоли, но часто сопровождаются тяжёлыми побочными эффектами и не всегда предотвращают рецидив. В этом исследовании изучается новый способ заставить уже существующий препарат — доксетаксел — работать эффективнее и умнее: упаковать его в крошечные частицы, реагирующие на нагрев, и активировать ближним инфракрасным светом. Цель — не только точнее уничтожать опухолевые клетки, но и пробудить иммунную систему, чтобы она распознавала опухоль по всему телу и предотвращала будущие рецидивы. 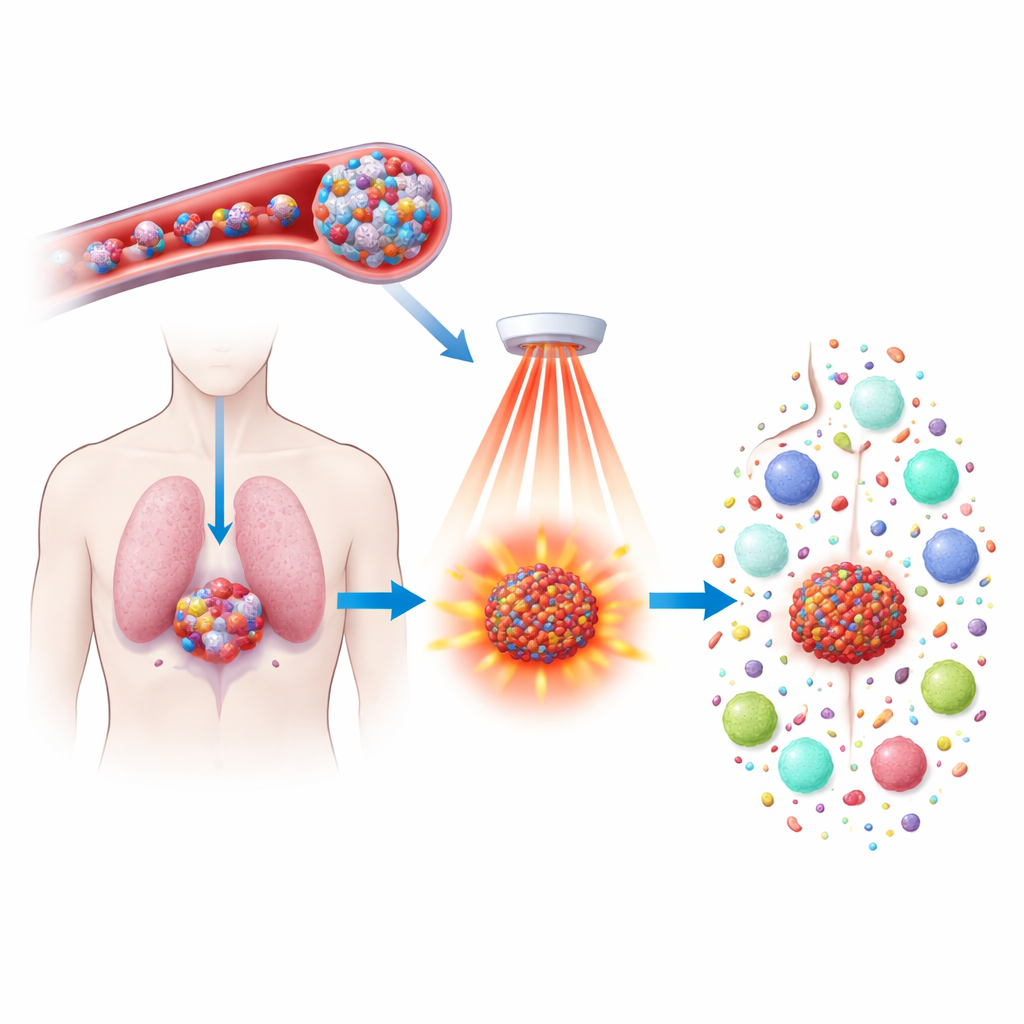
Крошечные курьеры, которые знают, куда идти
Исследователи создали новый тип наночастиц из полимера, содержащего ферроцен — железосодержащее соединение, которое активно реагирует с пероксидом водорода, сильным окислителем, встречающимся в опухолях в больших количествах по сравнению с нормальными тканями. Эти полимеры самособираются в водорастворимые сферы, способные нести как доксетаксел, так и светопоглощающий краситель IR808. После введения в кровь частицы достаточно малы и стабильны, чтобы циркулировать и проникать в опухоль через её проницаемые сосуды; высокая концентрация пероксида водорода и пористые капилляры начинают ослаблять частицы и медленно высвобождать груз. Такая конструкция концентрирует лечение в опухоли и ограничивает повреждение здоровых органов.
Использование света для усиления локального воздействия
Ближний инфракрасный свет, который безопасно проникает в ткани, направляют на область опухоли. IR808 внутри наночастиц поглощает этот свет и превращает его в тепло, одновременно генерируя реакционноспособные формы кислорода. Совместное действие опухолевого пероксида водорода и свет‑индуцированных окислителей заставляет частицы распадаться быстрее и быстро освобождать препарат прямо там, где он нужен. Одновременно железо в сегменте ферроцена помогает превращать эти окислители в особенно агрессивные формы, которые атакуют липидные компоненты клеточных мембран. Такое целенаправленное химическое и термическое воздействие значительно увеличивает убойную силу по сравнению с применением только доксетаксела или только света. 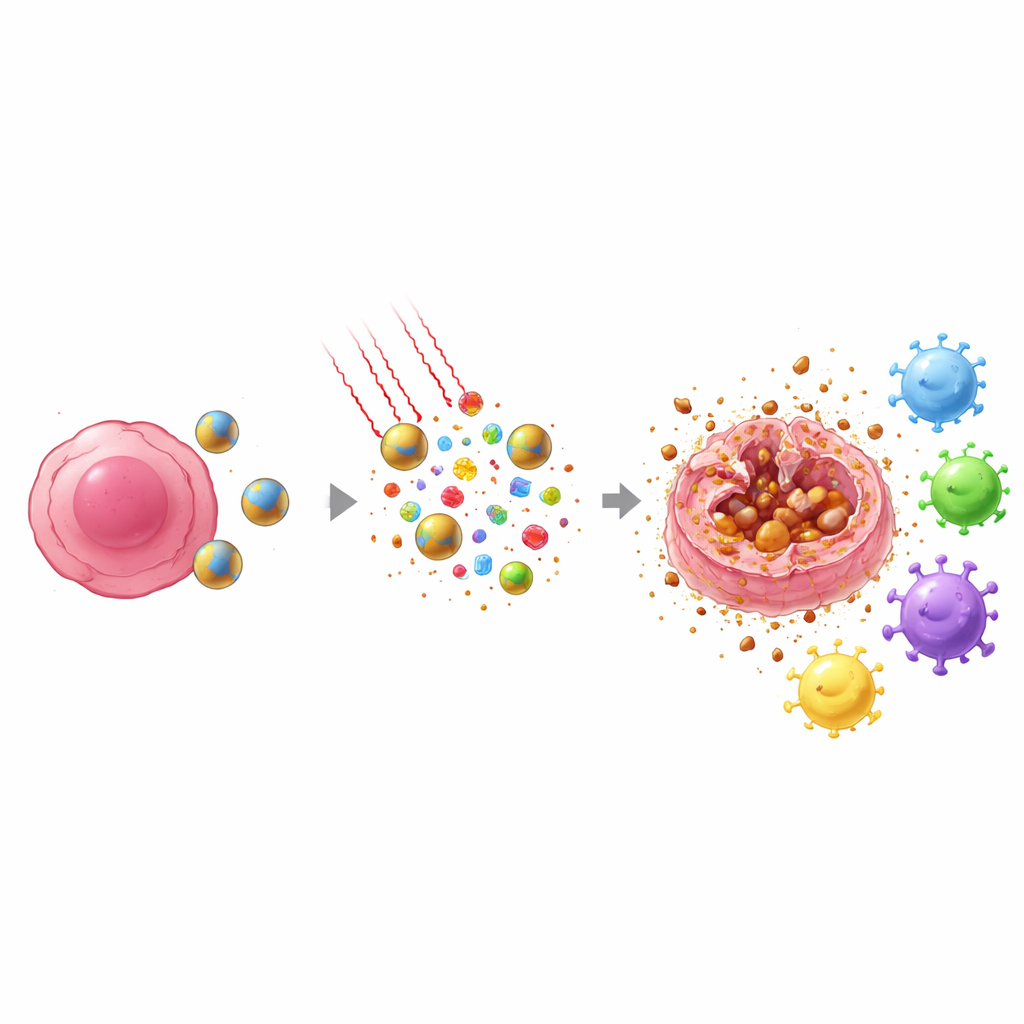
Контролируемое «сожжение», которое сигнализирует иммунной системе
Важно, что способ гибели опухолевых клеток при этом лечении отличается от обычной химиотерапии. Вместо тихого распада на аккуратные фрагменты многие клетки проходят процесс, называемый ферроптозом — форма смерти, вызванная железом и повреждением липидов, при котором наружная мембрана разрывается. Когда это происходит, клетки выбрасывают внутренние сигнализирующие молекулы и фрагменты, специфичные для опухоли, в окружающую среду. При этом доксетаксел способствует смещению ключевого ядерного белка HMGB1 к краю клетки, подготавливая его к высвобождению. В совокупности тепло, окислители и действие препарата создают всплеск опасностных и антигенных сигналов, которые могут улавливать близлежащие иммунные стражи — дендритные клетки — и нести их в лимфоузлы.
От локальной атаки к защите всего организма
В опухолевых моделях на мышах комбинированная хемо‑фототермальная терапия не только эффективнее уменьшала прогретые опухоли по сравнению с любым отдельным компонентом, но и меняла иммунный ландшафт. В опухолях обнаруживали больше зрелых дендритных клеток и больше киллерных Т‑клеток как в самих опухолях, так и в дренирующих лимфоузлах. У некоторых иммунокомпетентных мышей первичные опухоли исчезали уже после двух циклов лечения. Когда ученые позже имплантировали новые опухоли в отдалённых участках или на противоположном боку, эти вторичные очаги росли медленнее или подавлялись, что указывает на формирование у животных специфической противоопухолевой иммунной памяти. Добавление антитела, блокирующего контрольные точки и предотвращающего истощение Т‑клеток, дополнительно снижало метастазирование в лёгких и продлевало выживаемость, что говорит о том, что этот локальный подход можно сочетать с современными иммунотерапиями.
Почему это важно для будущего лечения рака
Для неспециалиста ключевая мысль такова: этот подход превращает доксетаксел из грубого системного токсина в элемент умной, многоступенчатой антикарциногенной стратегии. Упаковывая препарат в светочувствительные наночастицы с содержанием железа, которые реагируют на собственную химию опухоли, терапия доставляет больше повреждений внутрь опухолей и бережнее относится к здоровым тканям. Особая картина гибели клеток, которую она вызывает, действует как вакцина изнутри опухоли, обучая иммунную систему распознавать и запоминать рак. Если эти результаты подтвердятся у людей, такие хемо‑фототермальные системы могут помочь превратить резистентные «холодные» опухоли в «горячие», гораздо лучше отвечающие на иммунную терапию, что может снизить рецидивы и улучшить долгосрочный контроль болезни.
Цитирование: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Ключевые слова: наномедицина против рака, фототермическая терапия, ферроптоз, иммунотерапия рака, доставка доксетаксела