Clear Sky Science · ru
Устранение DUSP6 восстанавливает работоспособность CAR‑T клеток, нарушенную потерей CD58 опухолью, через активацию сигнального пути AP‑1
Почему усиление клеток, борющихся с раком, важно
Генно модифицированные иммунные клетки, называемые CAR‑T, преобразили лечение некоторых кровяных онкозаболеваний, но многие пациенты все ещё сталкиваются с рецидивами, потому что их опухоли находят способы уклоняться от атаки. В этом исследовании обнаружена скрытая уязвимость некоторых опухолей, которая тихо выводит CAR‑T клетки из строя изнутри, — и показано, как прицельная генетическая правка может восстановить выносливость этих клеток, их энергоресурсы и способность убивать. Для читателя это — взгляд на то, как терапия следующего поколения может стать более прочной и эффективной для большего числа людей.
Отсутствующая «ручка» на опухолевых клетках
CAR‑T клетки нуждаются в прочном «рукопожатии» с мишенью, чтобы работать эффективно. Многие опухолевые клетки демонстрируют на поверхности молекулу CD58, которая служит «ручкой» для иммунных клеток, помогая им захватываться и формировать плотную контактную зону. Ранее было показано, что при потере CD58 CAR‑T клетки испытывают трудности с образованием такого контакта и становятся менее эффективными. В этом исследовании авторы задали более глубокий вопрос: помимо механической проблемы «рукопожатия», как потеря CD58 перенастраивает внутреннюю биологию CAR‑T клеток, снижая их работоспособность со временем?
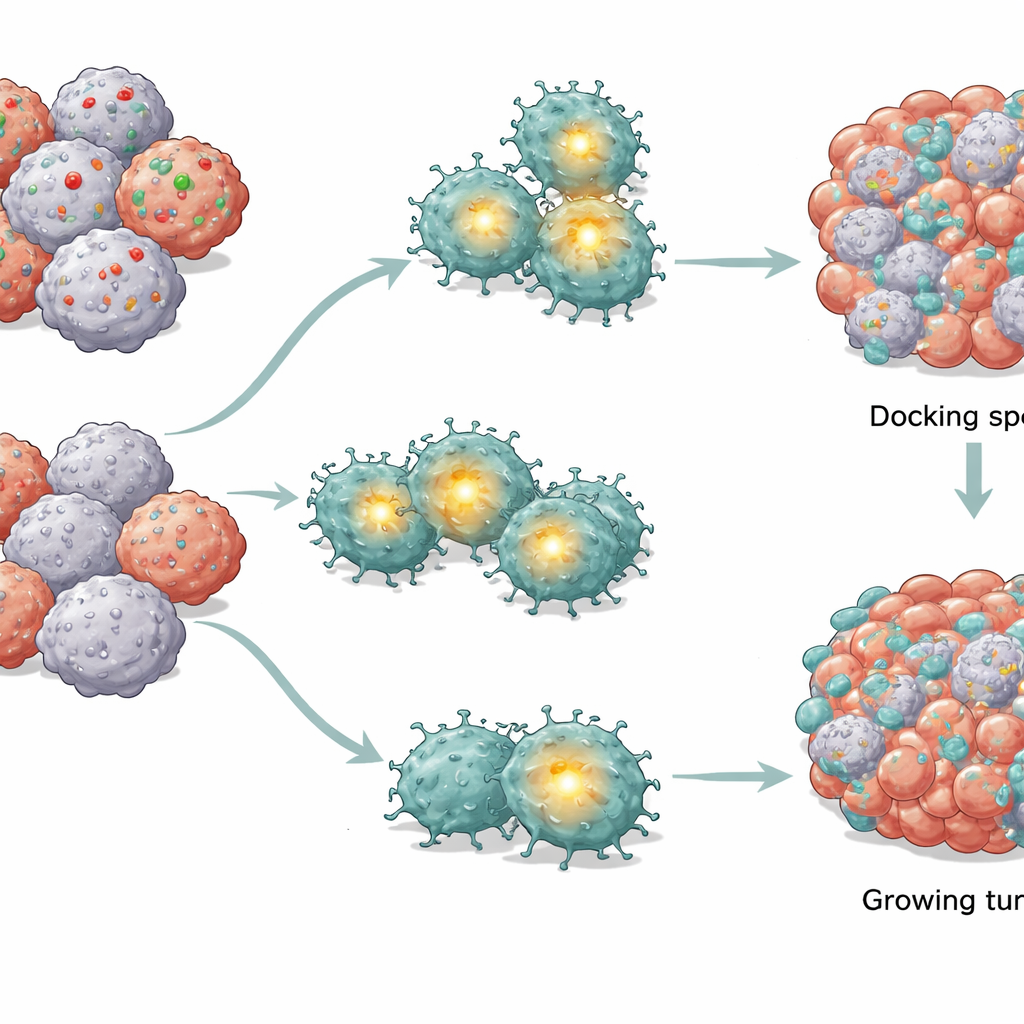
Укороченная проводка внутри CAR‑T клеток
Сравнивая CAR‑T клетки, подвергшиеся воздействию нормальных опухолей, и тех, что сталкивались с опухолями, лишёнными CD58, команда обнаружила, что ключевой управляющий узел внутри T‑клеток — называемый AP‑1 — был избирательно ослаблен, тогда как другие важные сигнальные пути в целом оставались целыми. AP‑1 — это комплекс белков, который включает гены, отвечающие за активацию и выживание. Когда активность AP‑1 снижалась, CAR‑T клетки демонстрировали характерные признаки внутреннего энергетического кризиса: меньшее число и меньшие по размеру митохондрий (их электростанций), сниженная способность потреблять кислород и использовать сахар, потерю электрического заряда на мембранах митохондрий. Одновременно накапливались вредные реактивные формы кислорода. В совокупности эти изменения толкали CAR‑T клетки к программам самоуничтожения, основанным на повреждении их собственных митохондрий, даже без внешних сигналов смерти.
Отключение внутреннего тормоза
Чтобы понять, почему AP‑1 был настолько подавлен, исследователи искали сверху молекулярные «тормоза», которые могли быть сверхактивны. Они обнаружили, что CAR‑T клетки, столкнувшиеся с опухолями без CD58, усиливали экспрессию нескольких фосфатаз — ферментов, выключающих сигнальные пути — особенно одной, называемой DUSP6. С помощью препаратов, а затем точного редактирования генома для блокирования этих ферментов, они показали, что удаление DUSP6 сильнее всего возвращало активность AP‑1. CAR‑T клетки с редактированным DUSP6 лучше размножались, образовывали больше митохондрий, эффективнее потребляли топливо, производили больше молекул, убивающих раковые клетки, и были менее склонны к апоптозу, особенно при многократно повторяющихся столкновениях с CD58‑дефицитными опухолевыми клетками.
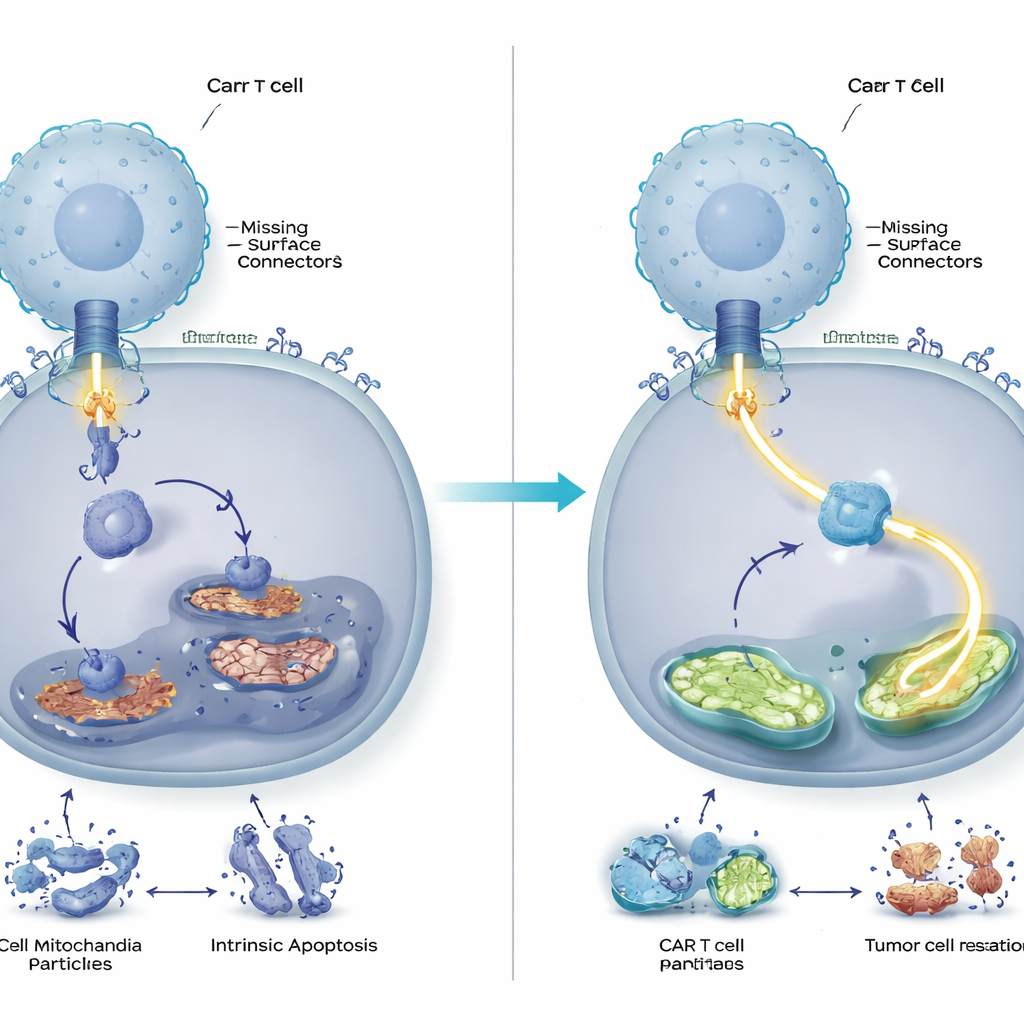
Более мощный и длительный контроль опухоли у животных
Затем команда проверила, имеет ли эта молекулярная корректировка значение в живом организме. У мышей с пересаженными человеческими клетками кровяного рака, которые либо имели, либо не имели CD58, CAR‑T клетки без DUSP6 эффективнее очищали опухоли и дольше удерживали их под контролем по сравнению с обычными CAR‑T клетками. Модифицированные клетки сильнее размножались, демонстрировали меньше маркеров истощения и секретировали более высокие уровни ключевых иммунных медиаторов. Примечательно, что преимущества удаления DUSP6 наблюдались не только при отсутствии CD58 у опухолей, но и при его наличии, что указывает на то, что эта модификация может в целом улучшать CAR‑T терапии, а не быть узко направленным решением для редкого подтипа опухолей.
Подсказки из данных пациентов
Чтобы проверить релевантность у людей, исследователи проанализировали данные экспрессии генов у пациентов, лечившихся CAR‑T терапией или препаратами, блокирующими контрольные точки. У пациентов с диффузной крупноклеточной B‑клеточной лимфомой, получавших двухмишенную CAR‑T терапию, более низкий уровень DUSP6 в CD8‑T клетках до или вскоре после инфузии ассоциировался с более высокими показателями полного ответа. В отдельной когорте пациентов с раком кожи, лечившихся анти‑PD‑1 антителами, истощённые CD8‑T клетки у неответчиков, как правило, экспрессировали больше DUSP6, чем у ответчиков. В совокупности эти наблюдения указывают на то, что DUSP6 выступает отрицательным маркером «фитнеса» T‑клеток при разных видах иммунотерапии, и что его подавление может улучшить результаты лечения.
Что это значит для будущих терапий рака
Для непрофессионального читателя суть такова: некоторые опухоли уходят от атаки CAR‑T клеток не только скрывшись от распознавания, но и саботируя их внутренние «двигатели». Потеря «ручки» CD58 на опухолевых клетках тихо снижает сигналы AP‑1 в CAR‑T клетках, опустошая их митохондрии, увеличивая токсичные побочные продукты и подталкивая к преждевременной гибели. Убрав тормоз DUSP6, учёные могут восстановить утраченную сигнализацию, восстановить здоровье митохондрий и дать CAR‑T клеткам большую выносливость и убойную силу, даже против устойчивых опухолей. Хотя необходимы дополнительные проверки безопасности и клинические испытания, абляция DUSP6 выглядит многообещающей инженерной стратегией для создания более мощных, долговечных и потенциально применимых у широкой группы пациентов живых лекарственных клеток.
Цитирование: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Ключевые слова: CAR‑T клетки, CD58, DUSP6, иммунотерапия рака, метаболизм T‑клеток