Clear Sky Science · ru
Раскрытие потенциала биметаллической «нанобомбы», активирующей путь STING, для усиления биспецифического T‑клеточного энгейджера в фото-иммунотерапии рака толстой кишки
Вернуть иммунную систему в борьбу с раком толстой кишки
Рак толстой и прямой кишки распространён и часто смертелен, отчасти потому, что опухоли учатся прятаться от иммунной системы. В этом исследовании рассматривается новая стратегия, которая объединяет несколько противопраковых приёмов в одной крошечной «нанобомбе», чтобы пробудить защиту организма, помочь иммунным клеткам найти опухоль и предотвратить рецидивы или метастазирование.
Почему современным иммунным препаратам нужен апгрейд
Одно перспективное направление в онкологии — биспецифические T‑клеточные энгейджеры — действует как биологические свахи: один конец захватывает T‑клетку (ключевого бойца иммунной системы), а другой прикрепляется к маркеру на клетке опухоли, принуждая их к контакту, чтобы T‑клетка могла убить цель. Несмотря на успех в гематологических опухолях, эти препараты с трудом работают при солидных опухолях, таких как рак толстой кишки. Их быстро выводят из организма, они могут поражать здоровые ткани с тем же маркером и часто сталкиваются с «холодными» опухолями, в которых недостаточно иммунных клеток для эффективности терапии. Врачи и учёные поэтому ищут способы более безопасной доставки этих препаратов и превращения холодных опухолей в «горячие», насыщенные активированными иммунными клетками.
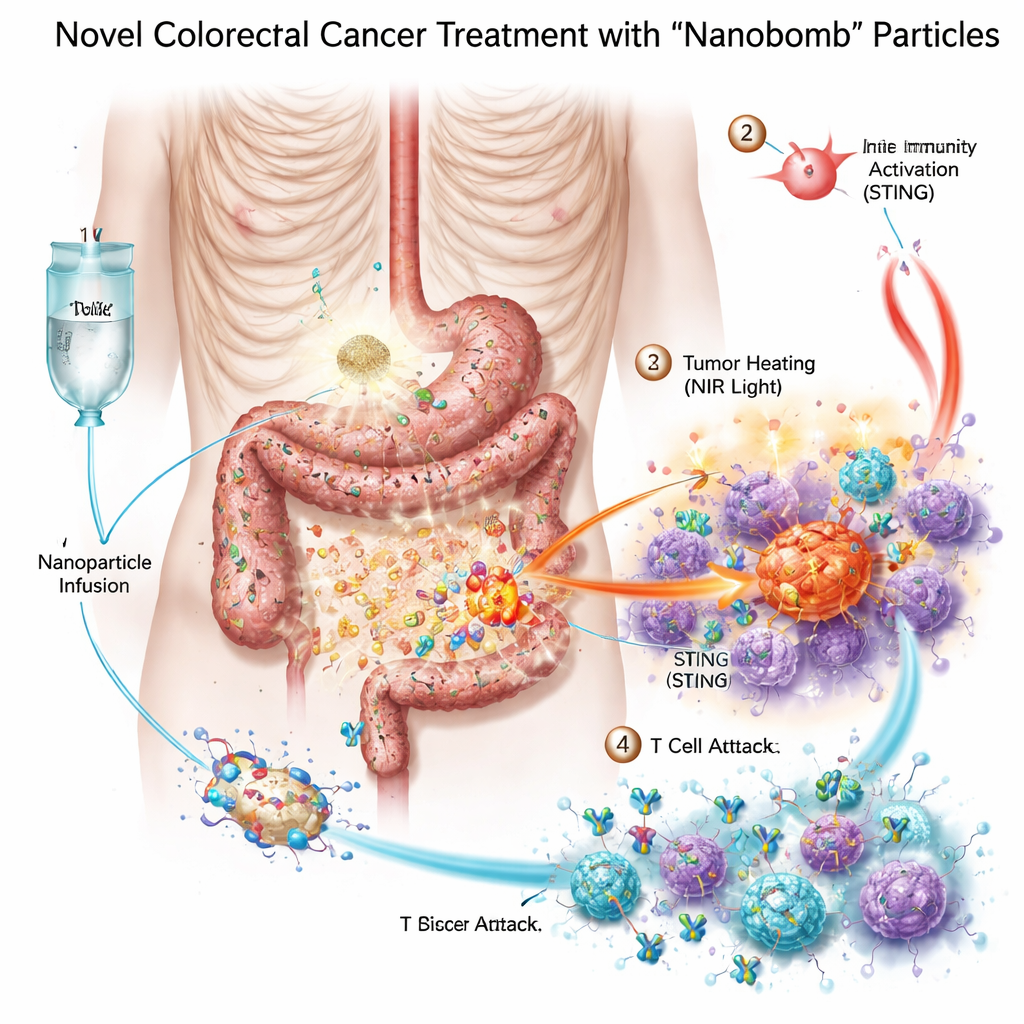
Три оружия в одной крошечной «нанобомбе»
Исследователи создали биметаллическую нанобомбу — в научном обозначении MnO2/Co‑DA@BiTE/HPT — которая объединяет три режима лечения в одной частице. Во‑первых, ядро содержит марганец и кобальт — металлы, способные активировать внутриклеточную систему тревоги, называемую путём STING, который помогает организму ощущать опасность и привлекать иммунные клетки. Во‑вторых, поверхность частицы покрыта биспецифическим T‑клеточным энгейджером, который соединяет T‑клетки с раковыми клетками. В‑третьих, материал поглощает ближний инфракрасный свет, что позволяет нагревать опухоль извне в виде фототермальной терапии. Чтобы нанобомбы направленно попадали в клетки рака толстой кишки, команда добавила короткую цепочку ДНК — аптамер, распознающий PD‑L1, молекулу, часто обильно выраженную на этих опухолях. Попав в опухоль, частицы разрушаются под действием природных ферментов в ткани, высвобождая свой груз непосредственно там, где он нужен.
Нагревание, тревога и привлечение иммунной армии
В лабораторных условиях нанобомбы убивали клетки рака толстой кишки эффективнее, чем любой из отдельных компонентов по отдельности. При облучении ближним инфракрасным светом частицы нагревались, вызывали стресс и повреждение опухолевых клеток и способствовали образованию реактивных форм кислорода — сильно реактивных молекул, дополнительно повреждающих клетки опухоли. Этот стресс разрывал ДНК клеток и вызывал видимую форму гибели, сопровождающуюся выделением «сигналов опасности». Близлежащие иммунные клетки, особенно дендритные клетки, поглощали погибший опухолевый материал и с помощью высвобождённого марганца и кобальта активировали путь STING. В результате они продуцировали интерфероны и другие провоспалительные медиаторы, которые способствовали созреванию и притоку T‑клеток. Одновременно биспецифический энгейджер на нанобомбе физически соединял T‑клетки с PD‑L1‑положительными опухолевыми клетками, улучшая активацию T‑клеток и разрушение опухоли даже в ранее холодных опухолях.
От сжатия опухоли до длительной иммунной памяти
В нескольких моделях на мышах — включая подкожные опухоли толстой кишки, опухоли с двух сторон тела, метастазы в лёгких и модель рецидива после операции — нанобомбы в сочетании со светом существенно замедляли или почти останавливали рост опухоли. В обработанных опухолях оказалось значительно больше убивающих рак CD8 T‑клеток и меньше регуляторных T‑клеток, которые обычно подавляют иммунный ответ. Дендритные клетки в опухолях и лимфоузлах демонстрировали признаки созревания, а в крови повышались уровни иммуностимулирующих цитокинов. Важно, что мыши, которые избавились от опухолей после лечения нанобомбой, были лучше защищены при повторном введении рака и имели меньше метастазов в лёгких, что указывает на формирование длительной иммунной памяти, а не лишь разового сокращения опухоли.
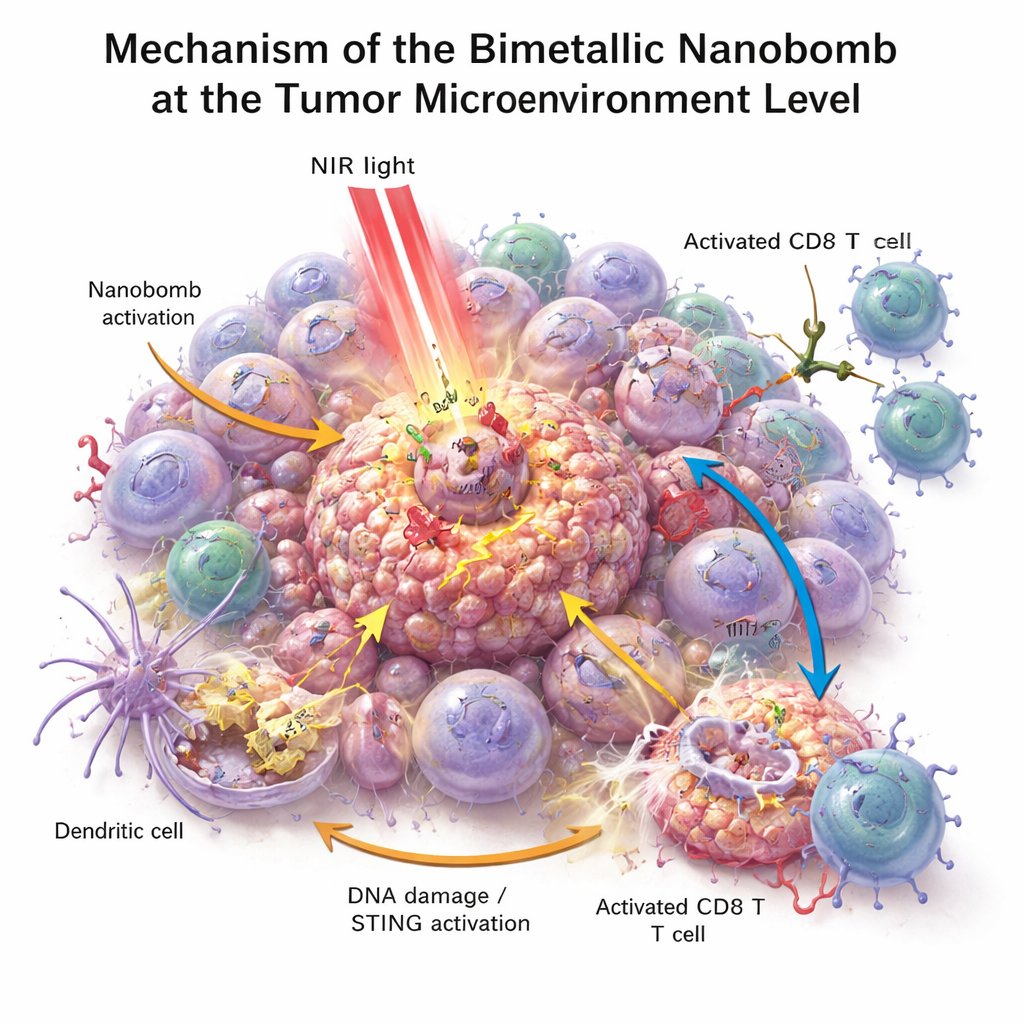
Что это может значить для будущей онкологической помощи
Эта работа представляет «тройную» наномедицину, которая нагревает опухоль, включает внутренний сигнал тревоги и направляет T‑клетки прямо к раковым клеткам — всё в одной целевой частице. На мышах такой подход не только превращал холодные опухоли толстой кишки в воспалённые «горячие» очаги, но и помогал предотвращать рецидивы и распространение. Хотя до клинического применения ещё далеко — масштабирование производства, долгосрочная безопасность и испытания на людях остаются серьёзными задачами — это исследование даёт шаблон для будущих терапий, которые объединяют умные материалы и иммунные препараты, чтобы обеспечить пациентам более мощный и продолжительный противораковый ответ.
Цитирование: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Ключевые слова: рак толстой кишки, иммунотерапия, наночастицы, путь STING, биспецифический T‑клеточный энгейджер