Clear Sky Science · ru
Персонализированная фармакокинетико‑фармакодинамическая терапия с использованием платформы мульти‑органоидов, полученных из индуцированных плюрипотентных стволовых клеток, при раке молочной железы с мутацией NF1
Почему это исследование важно для пациентов
Многие пациенты с раком получают препараты, которые эффективны у одних, но не у других, и часто вызывают тяжёлые побочные эффекты. Это исследование описывает новый способ тестирования противораковых методов вне организма с помощью лабораторно выращенных мини‑органов, созданных из клеток самого пациента. Работа посвящена трудноизлечимому варианту рака молочной железы, вызванному изменениями в гене NF1, и демонстрирует, как сочетание стратегии исправления гена и таргетного препарата может привести к более безопасной, эффективной и по‑настоящему персонализированной терапии.
Создание мини‑версии организма пациента
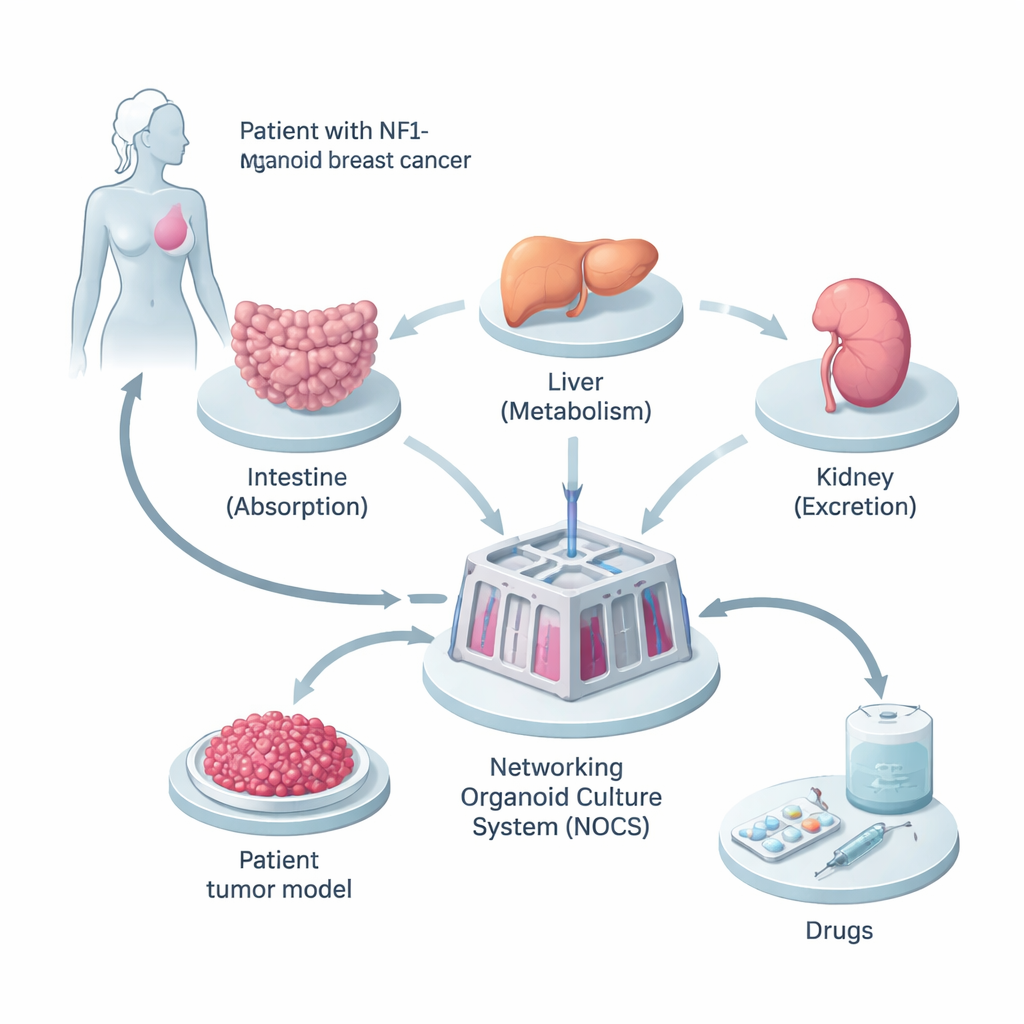
Исследователи начали с ткани от женщины, у которой рак молочной железы был связан с наследственной мутацией в гене NF1. Они перепрограммировали её обычные клетки кожи в индуцированные плюрипотентные стволовые клетки, способные превращаться почти в любой тип клеток организма. Из них вырастили три типа мини‑органов — тонкую кишку, печень и почку — поскольку именно эти органы играют ключевую роль в всасывании, переработке и выведении препаратов. Параллельно они создали трёхмерные опухолевые «сфероиды» из её раковых клеток, сохранив состав клеток и генетические изменения, характерные для исходной опухоли.
Живой контур для тестирования лекарств
Чтобы мини‑органы работали ближе к реальному организму, команда соединила их в устройстве, заполненном жидкостью, под названием Networking Organoid Culture System (NOCS). В этой системе питательная среда циркулирует между отсеками тонкой кишки, печени, почки и опухоли, имитируя кровообращение. Препараты можно вводить так, как будто глотают таблетку или делают инъекцию, а датчики и насосы контролируют скорость движения «крови» и частоту её обновления. Это позволило учёным отслеживать, сколько препарата всосалось, как быстро он разрушается и насколько сильно воздействует на опухоль — всё в модели, специфичной для пациента и основанной на человеческих тканях.
Исправление повреждённого гена с помощью пропуска экзона
В опухоли пациента была повреждающая мутация NF1, которая поддерживает активность сигнальных путей роста и делает многие стандартные препараты неэффективными. Команда разработала короткие фрагменты генетического материала — антисмысловые олигонуклеотиды — чтобы заставить механизмы обработки РНК клетки «пропустить» дефектный участок (экзон 2) гена NF1. С помощью вирусной системы доставки, действующей в течение нескольких дней, они индуцировали стабильный «пропуск экзона» в раковых клетках пациента. В результате образовался укороченный, но функциональный белок NF1, снизилась гиперактивность сигнальных путей роста и опухолевые клетки стали более чувствительны к лечению.
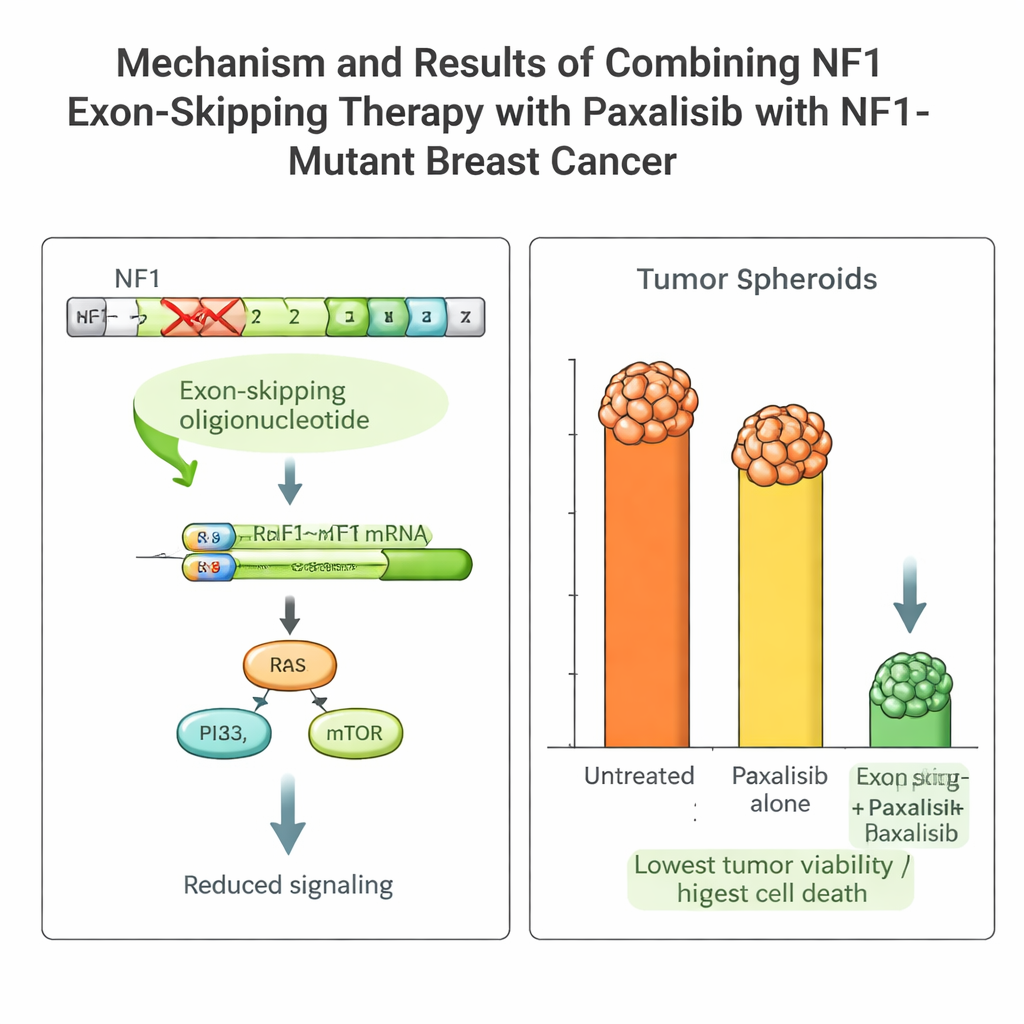
Выбор правильного таргетного препарата с учётом PK/PD
Используя эту платформу, команда сравнила несколько современных препаратов, блокирующих путь PI3K–mTOR, находящийся ниже по цепочке от NF1. Они измеряли фармакокинетику (как организм обрабатывает препарат) и фармакодинамику (как препарат действует на опухоль) как в мышах, так и в NOCS. Один препарат, пахалисиб (Paxalisib), выделился: он хорошо всасывался в кишечнике, сохранялся в системе на полезных уровнях и демонстрировал схожее поведение в животных и в органоидном устройстве. В сочетании с пропуском экзона NF1 у пахалисиба значительно возросла способность убивать клетки опухоли пациента — наблюдалось сильное снижение роста и явные признаки запрограммированной гибели клеток как в NOCS, так и в мышах с трансплантированной опухолью пациента.
Баланс пользы и риска для разных органов
Поскольку модели кишечника, печени и почки были частью одного контура, исследователи также могли наблюдать ранние признаки повреждения органов. Пахалисиб вызывал стрессовые ответы и незначительное ослабление барьерной функции в моделях кишечника и почек, а также признаки напряжения в печени, но без значительной потери жизнеспособности клеток при исследуемой дозе. Такой общий взгляд на организм с использованием человеческих тканей позволяет сравнивать варианты лечения не только по степени уменьшения опухоли, но и по потенциальному воздействию на здоровые органы до того, как препарат попадёт пациенту.
Что это может значить для будущего лечения рака
Проще говоря, это исследование показывает, что стало возможным вырастить упрощённый, индивидуализированный «мини‑организм на чипе», который может тестировать, как разные препараты — и даже подходы по коррекции генов — будут вести себя и взаимодействовать. Для этой пациентки с NF1‑мутацией оптимальной стратегией оказалось сочетание терапии пропуска экзона NF1 и орального препарата пахалисиба, которое замедлило рост опухоли гораздо сильнее, чем каждый из подходов по отдельности. При дальнейшем развитии и проверке на большем числе пациентов такие платформы могут направлять врачей к схемам лечения, адаптированным к генетике и биологии каждого человека, повышая шансы на успех и снижая ненужную токсичность.
Цитирование: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Ключевые слова: персонализированная онкология, рак молочной железы, органоиды, мутация NF1, таргетная терапия