Clear Sky Science · ru
Использование липид-управляемых иммунометаболических путей в оментальных метастазах для усиления иммунотерапии у пациенток с раком яичников
Почему жир вокруг живота важен при раке яичников
Рак яичников часто распространяется на жировой фартук в брюшной полости, называемый оментумом. Эта область богата адипоцитами и иммунными клетками и оказывается гораздо более активным участником процесса, чем просто пассивная среда. В настоящем обзоре показано, что то, как иммунные клетки используют и перерабатывают жир в этих оментальных очагах, помогает объяснить, почему лишь небольшая доля пациенток получает пользу от современных иммунотерапий. Исследование также предлагает новые сочетания препаратов и тесты на основе визуализации, которые могут сделать эти терапии эффективными для большего числа пациенток.
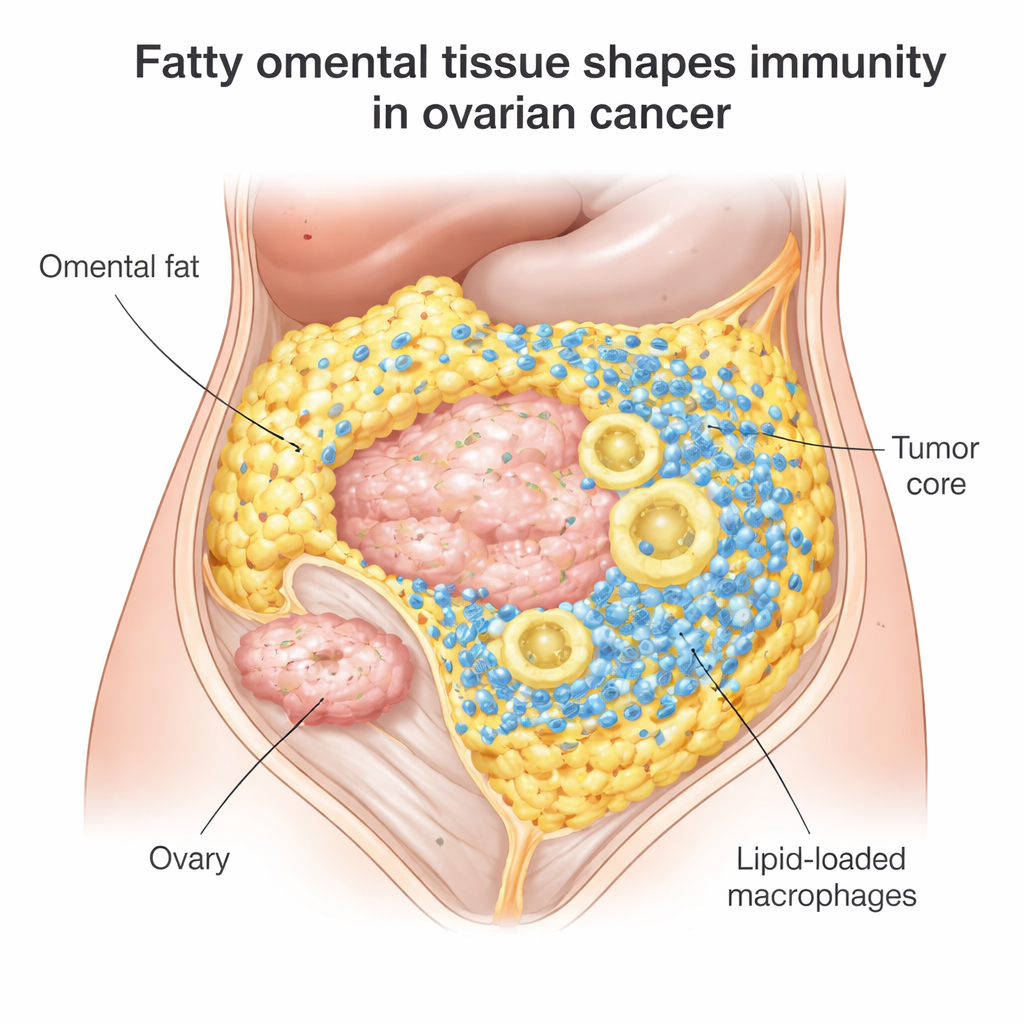
Скрытая поле битвы в брюшном жире
Большинство женщин с эпителиальным раком яичников первоначально реагируют на хирургическое вмешательство и химиотерапию, но у 70–80% заболевание возвращается, а ингибиторы контрольных точек иммунитета, такие как ниволумаб или пембролизумаб, помогают лишь примерно 10–15%. Исследователи сосредоточили внимание на оментальных метастазах, обычном месте, где опухоль укореняется среди жировых клеток. При изучении более чем 100 образцов опухолей они обнаружили, что оментальные опухоли переполнены иммунными клетками: киллерными Т-клетками, способными атаковать рак, и крупными «полевыми» клетками — макрофагами. Но был нюанс. Эти Т-клетки склонялись к скоплениям на границе, где опухоль соприкасается с жиром, вместо того чтобы проникать в глубь опухолевого ядра, где они наиболее нужны.
Жир, который питает одни иммунные клетки и подавляет другие
Углубляясь в проблему, команда показала, что Т-клетки в этих жировых опухолях приспосабливаются к местной среде, поглощая липиды из соседних адипоцитов. Это, по-видимому, поддерживает их метаболическую «фитность»: профили экспрессии генов и лабораторные испытания продемонстрировали их способность распознавать и уничтожать собственные опухолевые клетки пациентки. В то же время многие опухоле-ассоциированные макрофаги в оментуме были перегружены жировыми каплями. Эти макрофаги, наполненные липидами, демонстрировали признаки высокого окислительного стресса — химического износа, связанного с реактивными формами кислорода — и смещались в иммуноподавляющее, поддерживающее опухоль состояние. Иными словами, та же богатая жиром среда, которая может подпитывать эффективные Т-клетки, одновременно переворачивает макрофаги в вредоносный режим, ослабляющий общий иммунный ответ.
Перепрограммирование «перекормленных» макрофагов существующими препаратами
Учёные затем спросили, можно ли вернуть этих напряжённых макрофагов на сторону защиты организма. Используя свежие фрагменты опухолей, выращенные в лаборатории, они опробовали два подхода. Первый — маравировок, противовирусный препарат для ВИЧ, блокирующий CCR5, рецептор для иммунного сигнала CCL5, который изобилует на границе опухоль–жир. Второй подход блокировал CD36, ключевой «скрабберный» рецептор, позволяющий макрофагам импортировать жирные кислоты. Оба лечения уменьшали жировую нагрузку внутри макрофагов, снижали маркёры окислительного стресса и повреждающей липидной пероксидации и вызывали всплески провоспалительных сигналов. Существенно то, что эти вмешательства позволяли киллерным Т-клеткам размножаться и перемещаться с жирного края в ядро опухоли, усиливая местную иммунную активность без введения дополнительных внешних иммунных клеток.
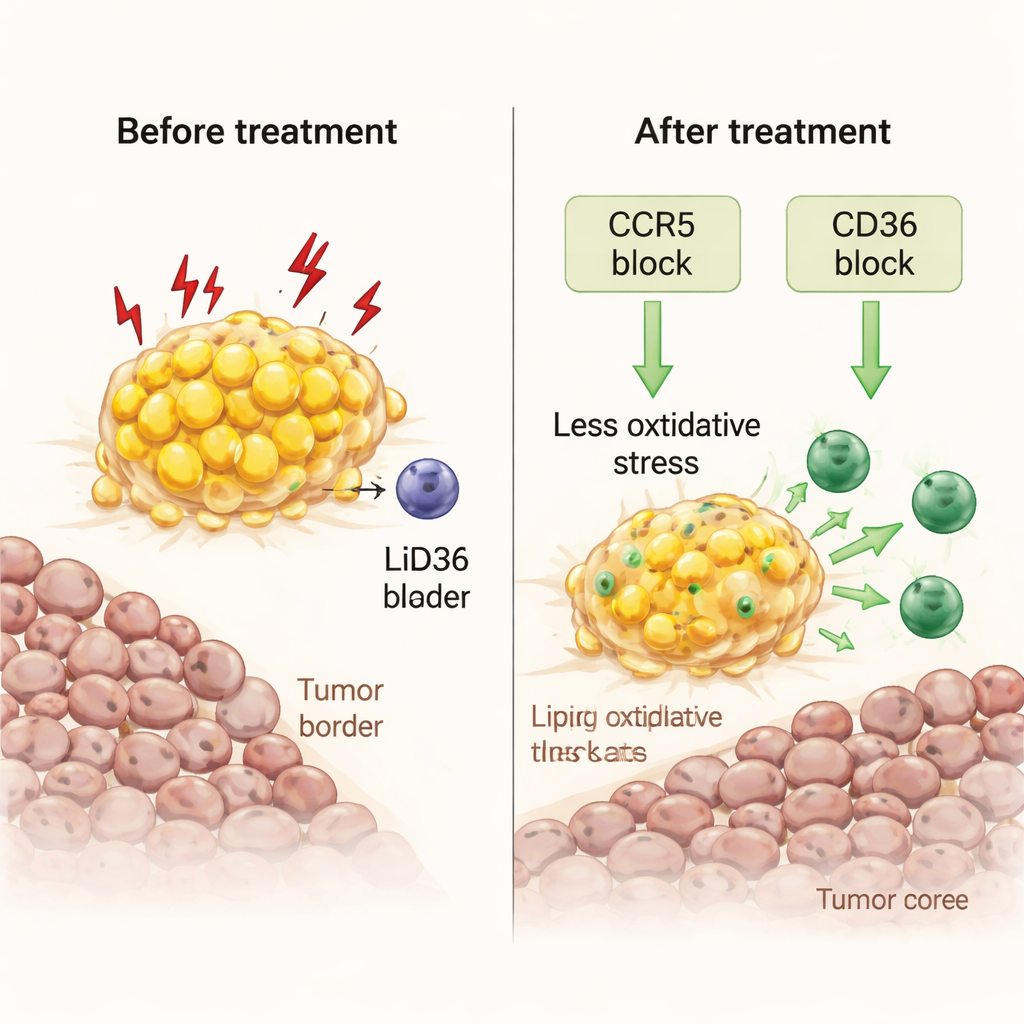
От клеточных путей к моделям и пациентам в реальном мире
Чтобы проверить эти идеи в более реалистичной обстановке, команда использовала гуманизированных мышей с иммунной системой, близкой к человеческой, и имплантировала им человеческую опухоль молочной железы в ткань, богатую жиром. Лечение маравировоком перепрограммировало человеческие макрофаги в этих животных аналогично наблюдаемому в образцах от пациенток: уменьшилась липидная и стрессовая сигнатура, выросло производство цитокинов и усилилась поддержка путей, связанных с Т-клетками. В клинической части исследования исследователи переосмыслили японское клиническое исследование ниволумаба при химиорезистентном раке яичников. Каждая пациентка, получившая пользу от препарата, имела оментальные метастазы, видимые в хирургических образцах. С помощью КТ или МРТ в сочетании с анализом распределения жировой ткани на основе машинного обучения они построили дерево решений, способное неинвазивно помечать пациенток, чьи опухоли, вероятно, расположены близко к висцеральному жиру — и в одном проспективном случае этот метод верно предсказал пациентку, которая затем ответила на ниволумаб.
Что это может значить для будущего лечения
Для неспециалиста ключевая мысль такова: «где» растёт рак яичников в теле и как прилегающий жир перестраивает иммунные клетки, может сильно влиять на то, сработает ли иммунотерапия. Богатые липидами оментальные отложения кажутся местом, где уживаются энергичные Т-клетки и «перекормленные», напряжённые макрофаги, которые притормаживают атаку. Облегчив липидную нагрузку в этих макрофагах и снизив их окислительное напряжение — с помощью блокаторов CCR5, таких как маравировок, агентов, нацеленных на CD36, или сопутствующих стратегий — возможно превратить частично блокированный иммунный ответ в полномасштабное наступление на опухоль. Одновременно меры визуализации оментального вовлечения могут помочь врачам выбрать пациенток, которые с наибольшей вероятностью получат пользу от ингибиторов контрольных точек, обеспечивая более персонализированный и потенциально более эффективный подход к лечению рака яичников.
Цитирование: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Ключевые слова: рак яичников, оментальная жировая ткань, иммунотерапия, макрофаги, ассоциированные с опухолью, липидный метаболизм