Clear Sky Science · ru
GPR54 регулирует развитие немелкоклеточного рака лёгкого через дофа-декарбоксилазу
Почему эта история о раке лёгкого важна
Рак лёгкого остаётся одним из самых смертельных видов рака, и большинство случаев приходится на форму, называемую немелкоклеточным раком лёгкого (НМРЛ). У многих пациентов со временем исчерпываются эффективные варианты лечения, потому что опухоли приспосабливаются или развивают устойчивость к действующим препаратам. В этом исследовании выявлена ранее недооценённая система регуляции внутри клеток рака лёгкого, в центре которой — рецептор GPR54 и фермент дофа-декарбоксилаза (DDC). Поняв, как эти молекулы помогают опухолям расти и обеспечивать себя энергией, учёные указывают на новые способы замедлить или даже уменьшить НМРЛ.
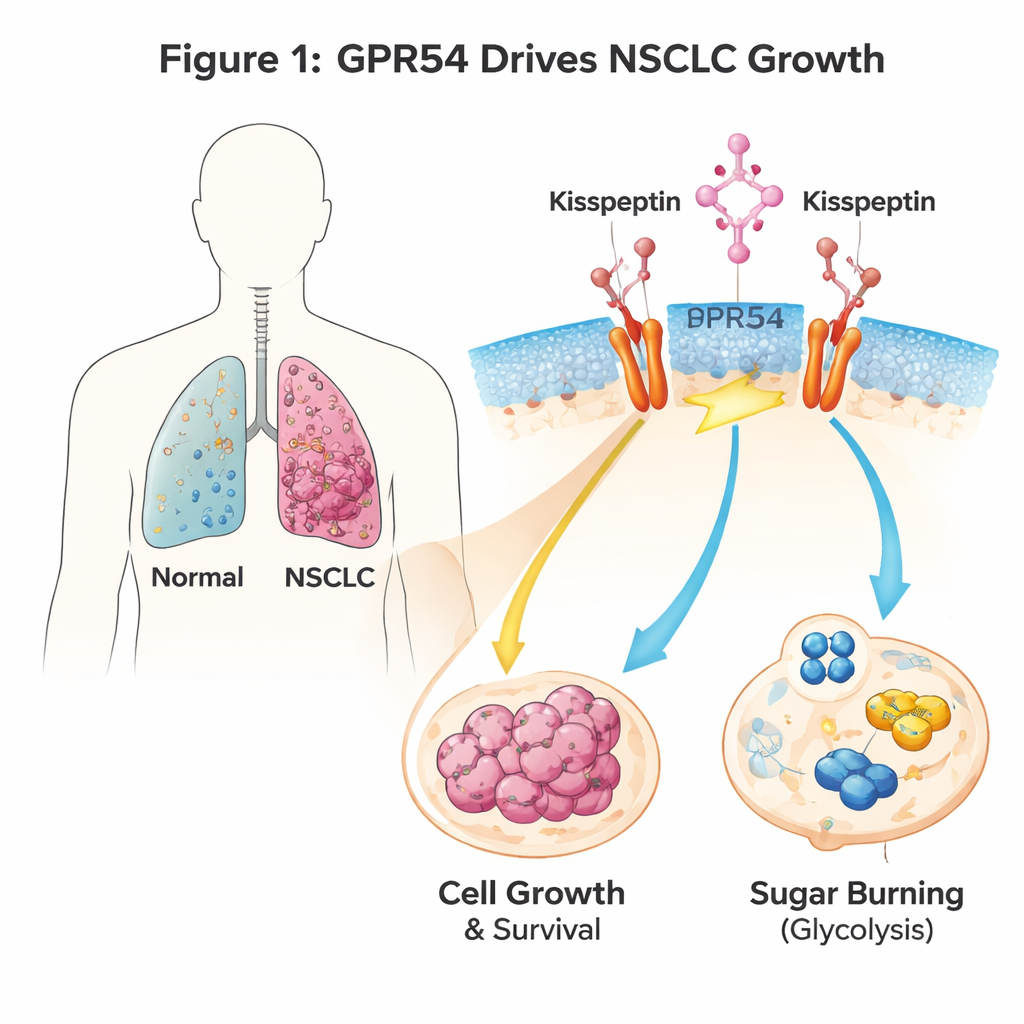
Сигнальный переключатель на клетках рака лёгкого
GPR54 — это датчик на поверхности клетки, который реагирует на природный сигнал, называемый кисепептином. Он известен прежде всего ролями в периоде полового созревания и репродукции, но также встречается во многих видах рака. Авторы использовали генетически модифицированных мышей, у которых развивается НМРЛ при включении онкогенного гена Kras в клетках лёгкого. При удалении гена Gpr54 у этих животных продолжительность жизни увеличивалась, образовывалось меньше и меньше по размеру опухолей лёгкого, а раковые клетки демонстрировали явные признаки самоуничтожения (апоптоза). Линии человеческих клеток НМРЛ подтвердили ту же картину: при снижении уровня GPR54 опухолевые клетки росли медленнее, образовывали меньше колоний и легче умирали, независимо от их конкретных генетических мутаций.
Как GPR54 поддерживает выживание опухолевых клеток
Копнув глубже, исследователи выяснили, какими внутриклеточными цепями пользуется GPR54. Они обнаружили, что GPR54 влияет на два основных пути роста внутри клетки — AKT и ERK. Оба являются распространёнными «узловыми линиями», которые побуждают раковые клетки делиться и сопротивляться гибели. Когда GPR54 блокировали или удаляли, активность AKT и ERK падала, и клетки становились более склонны к апоптозу. Восстановление сильных сигналов AKT или ERK частично спасало клетки, что подтверждает: GPR54 помогает клеткам НМРЛ выживать, опираясь на эти сигнальные цепи.
Перепрограммирование использования сахара в опухоли
Раковые клетки часто перенастраивают использование питательных веществ, предпочитая быстрый распад сахара (гликолиз) для получения энергии и роста. Профилирование экспрессии генов в опухолях мышей без Gpr54 показало, что многие гены, вовлечённые в утилизацию сахара и производство энергии, были подавлены. В клетках рака лёгкого, обработанных кисепептином для активации GPR54, измерения потребления кислорода и продукции кислоты — прокси для энергетического обмена — показали, что GPR54 стимулирует гликолиз. Блокада пути GPR54 на разных этапах (переключатель Gαq/11, PI3K, AKT или mTOR) снижала потребление глюкозы и образование лактата и сдвигала клетки в сторону апоптоза. Проще говоря, GPR54 помогает клеткам НМРЛ сжигать сахар быстрее и эффективнее, поддерживая их ускоренный рост.
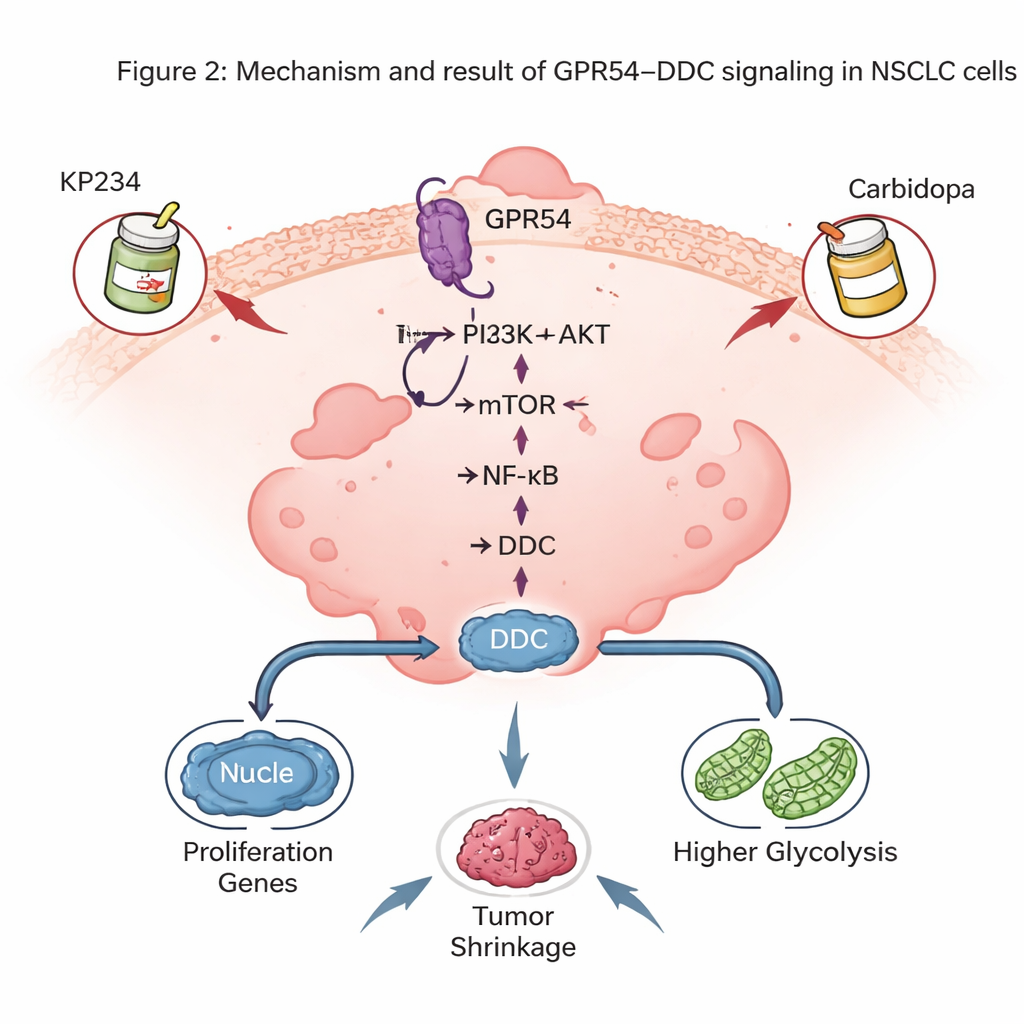
Неожиданная роль фермента, связанного с мозгом
Одним из самых впечатляющих открытий было то, что GPR54 контролирует уровни DDC — фермента, наиболее известного по синтезу мозговых нейромедиаторов дофамина и серотонина. В опухолях мышей уровни DDC тесно коррелировали с количеством GPR54: меньше GPR54 означало меньше DDC. В человеческих опухолях НМРЛ и клеточных линиях также наблюдали повышенный уровень DDC по сравнению с нормальной тканью лёгкого, а у пациентов с высоким уровнем DDC выживаемость была ниже. Подавление DDC в клетках рака лёгкого замедляло рост опухолей у мышей, снижало деление клеток в культурах и вызывало больше апоптоза. На молекулярном уровне DDC помогала поддерживать активность пути NF-κB — главного регулятора, который способствует выживанию раковых клеток и воспалению — а также поддерживала высокий гликолитический статус опухолей.
Проверка стратегии комбинирования препаратов
Поскольку DDC уже является мишенью в лечении болезни Паркинсона препаратом карбидопой, авторы проверили, можно ли объединить блокатор GPR54 (KP234) с карбидопой, чтобы атаковать НМРЛ с двух сторон. В культурах клеток и в моделях у мышей, где человеческие клетки НМРЛ выращивали в лёгком, двойная терапия сильнее подавляла рост опухолей, чем каждый препарат по отдельности, и увеличивала гибель раковых клеток без заметной потери веса у животных. Эти сочетания также показали перспективу при использовании вместе с некоторыми современными таргетными препаратами, направленными против мутантных генов RAS, что предполагает возможность наложения сигнального блока GPR54–DDC на существующие персонализированные терапии.
Что это значит для будущего лечения рака лёгкого
Для непрофессионала главный вывод таков: клетки НМРЛ зависят от ранее недооценённого взаимодействия между поверхностным переключателем (GPR54) и метаболическим ферментом (DDC), чтобы оставаться живыми и быстро «сжигать» топливо. Нарушение этого взаимодействия ослабляет опухоли, замедляя их рост и повышая склонность к гибели в экспериментальных моделях. Хотя до клинического применения остаётся много работы, это исследование выделяет GPR54 и DDC как потенциальные биомаркеры агрессивного НМРЛ и как перспективные мишени для новых комбинированных подходов, которые могут улучшить исходы у пациентов, чьи опухоли сейчас ускользают от стандартных терапий.
Цитирование: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Ключевые слова: немелкоклеточный рак лёгкого, GPR54, допа-декарбоксилаза, метаболизм опухоли, таргетная терапия